
【题目】将1.80g氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,过滤后得到溶质质量分数为20.0%的溶液5.85g。已知氯化铜与氢氧化钠溶液反应的化学方程式为:CuCl2+2NaOH =Cu(OH)2↓+2NaCl
求:(1)样品中氯化铜的质量_____;
(2)加入氢氧化钠溶液的质量_____。
【答案】1.35g 5.48g
【解析】
氯化铜与一定量的氢氧化钠溶液恰好完全反应,所得溶液为氯化钠溶液,根据得到溶溶质质量分数为20.0%的溶液5.85g,计算出反应生成氯化钠的质量,根据反应的化学方程式,由氯化钠的质量可计算样品中氯化铜的质量及所消耗氢氧化钠溶液中氢氧化钠的质量和生成氢氧化铜的质量,及一步求解样品中氯化铜的质量和加入氢氧化钠溶液的质量。
解:(1)由题意得,生成NaCl的质量为5.85g×20.0%=1.17g,设样品中CuCl2的质量为x,生成氢氧化铜的质量为y,
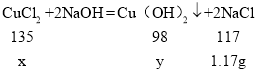
![]() x=1.35g,
x=1.35g,
![]() y=0.98g,
y=0.98g,
(2)NaOH溶液的质量为:5.85g+0.98g-1.35g=5.48g,
答:(1)样品中CuCl2的质量为1.35g;
(2)NaOH溶液的质量为5.48g。


科目:初中化学 来源: 题型:
【题目】人体缺少钙元素会影响健康,因此每日需摄入足够的钙.某补钙剂包装盒上的说明如图所示,请完成下列问题:

(1)葡萄糖酸钙的相对分子质量为___________
(2)葡萄糖酸钙中氢元素与氧元素的质量比为_______
(3)葡萄糖酸钙中钙元素质量分数为___________
(4)按说明书服用该钙片时,每天能补充的钙为___________g(保留到小数点后两位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组同学发现在面包制作过程中加入了一些白色粉末,使面包变得松软。同学们对白色粉末的成分进行探究。
(查阅资料)①经调查,市场上有以下3种主要产品。
商品名称 | 小苏打 | 食臭粉 | 混合碱性膨松剂 |
主要成分 | 碳酸氢钠 | 碳酸氢铵 | 碳酸氢钠和碳酸氢铵 |
②2NaHCO3![]() Na2CO3+H2O+CO2↑;NH4HCO3
Na2CO3+H2O+CO2↑;NH4HCO3![]() NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
(实验准备)同学们选用下列实验装置,经组合进行实验:
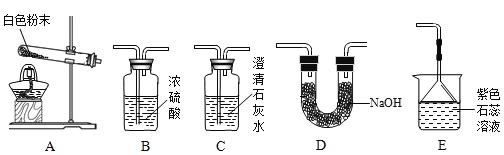
(实验记录)
实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
实验1 | 选用A、B、C | C中澄清石灰水变浑浊 | 有CO2生成,C中反应的化学方程式是_____ |
实验2 | 选用A、_____和E | E中紫色石蕊溶液变_____色 | 有NH3生成 |
(实验分析)
根据上述实验,甲同学认为该粉末的主要成分为食臭粉,乙同学认为上述实验不能确定该粉末为食臭粉。为进一步确认其组成及含量,同学们设计了如下定量实验:
实验序号 | 实验目的 | 实验装置 | 数据记录 | 实验结论 |
实验3 | 测定生成CO2的质量 | 选用A、B、D | 装置D增重ag | 该粉末为“混合碱性膨松剂” |
实验4 | 测定生成NH3的质量 | 选用A、D、B | 装置B增重1.7g |
(1)实验3中装置B的作用是_____。
(2)实验3中测得装置D增重ag,则a>_____g。
(3)若测得a为92.4,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t2℃时,将90g固体甲、乙(均不含结晶水)分别放到盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答:
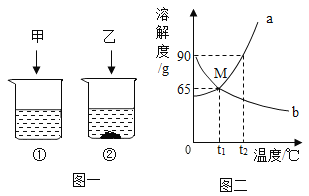
(1)固体乙对应的溶解度曲线是____(填“a”或“b”)。
(2)甲中含有少量乙,提纯甲的方法是_____。
(3)若向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体析出。你认为“固体先全部溶解”的原因是_____。
(4)将t2℃时①、②两烧杯中的物质分别降温至t1℃时,所得溶液的有关说法不正确的是_____(填字母序号)
a两溶液均为饱和溶液 b两溶液质量相等
c溶液中溶质的质量分数甲>乙 d①中析出25g 固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固态物质的饱和溶液中溶质质量分数与温度关系如图所示。
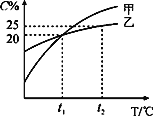
(1)甲、乙两种物质的溶解度随温度升高而_________(填“增大”或“减小”)。
(2)t1℃时,乙固体的溶解度为:________。
(3)25g乙物质完全溶于100g水所需的最低温度是_____。
(4)t2℃100g乙饱和溶液,稀释成10%乙溶液用到的玻璃仪器有_____________。
(5)根据图形分析,下列说法正确的是_____。
A t1℃甲、乙两种物质饱和溶液中溶质质量相等
B 将t1℃甲、乙饱和溶液升温至t2℃,所得溶液溶质质量分数相等
C t2℃,若从甲、乙两物质饱和溶液中析出等质量固体,蒸发较多水的是甲饱和溶液
D 甲中混有少量乙,提纯甲固体,可采用降温结晶的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取 8g氢氧化钠固体,在空气中露置一段时间后,加入足量稀盐酸。充分反应后,下列说法正确的是()
A.氢氧化钠固体在空气中放置时间越久,反应中消耗的 HCl的质量越少
B.反应生成氯化钠的质量一定等于11.7g
C.氢氧化钠固体在空气中放置时间越久,固体中氧元素的质量分数越小
D.加入稀盐酸后,一定立即产生气泡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某CaCO3和CaO的混合粉末中钙元素与氧元素的质量比为2:1,现取一定量的混合粉末高温煅烧,充分反应后得到固体5.6g,则生成气体的质量与下列最接近的是()
A.0.32gB.0.4gC.0.44gD.0.55g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某金属加工厂生产过程中,产生的废液含有少量硝酸银和硝酸铜。为回收利用金属和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,有无色气体放出。则下列有关说法正确的是( )
A.滤渣中一定含有银和铜,也可能含有铁
B.滤渣质量可能等于加入铁粉的质量
C.向滤液中加入少量稀盐酸,无明显现象
D.滤液一定为无色
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置,根据下图回答下列问题:
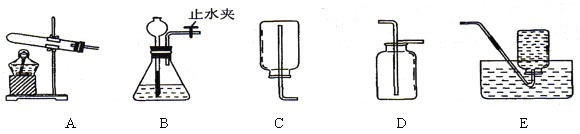
(1)关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则B装置是否漏气?_____(填“漏气”、“不漏气”或“无法确定”)。
(2)选用E装置收集氧气,收集的氧气不够纯,其原因可能是_____(写出一点)。
(3)小枫同学用加热氯化铵和氢氧化钙的固体混合物来制取氨气,他应选择的发生装置是_____,若收集氨气的装置只能用C,由此可知氨气所具有的性质是_____(写出一点)。
(4)NH3是一种碱性气体,干燥时不能选用下列干燥剂中的_____(填序号)。
A 固体氢氧化钠 B 浓硫酸 C 生石灰
(5)小雯同学将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是集气瓶内的水面上升,而且水变_____(填一种颜色)。
(6)下图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物。胃液中含有适量的甲,可帮助消化。图中“—”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物已略去。
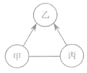
Ⅰ写出甲的化学式_____。
Ⅱ①若乙在常温下为液体,丙可用来改良酸性土壤,则乙的化学式为_____,丙的化学式为_____。
②若乙在常温下为气体,且可由甲与大理石反应得到,则乙的化学式为_____,丙能与①中的丙发生复分解反应,其化学方程式为_____(写出一个即可)。
③写出①中的乙和②中的乙发生化合反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com