
【题目】取 8g氢氧化钠固体,在空气中露置一段时间后,加入足量稀盐酸。充分反应后,下列说法正确的是()
A.氢氧化钠固体在空气中放置时间越久,反应中消耗的 HCl的质量越少
B.反应生成氯化钠的质量一定等于11.7g
C.氢氧化钠固体在空气中放置时间越久,固体中氧元素的质量分数越小
D.加入稀盐酸后,一定立即产生气泡
【答案】B
【解析】
根据氢氧化钠变质生成碳酸钠,以及氢氧化钠和碳酸钠都能与盐酸反应进行分析解答即可。
A、假设氢氧化钠全部变质,则根据反应的化学方程式可以看出:2NaOH+CO2═Na2CO3+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑,NaOH--HCl,即最终消耗的盐酸的量是不变的,错误;
B、8g氢氧化钠中钠元素的质量为8g×![]() ×100%=4.6g,反应生成氯化钠的质量一定等于:
×100%=4.6g,反应生成氯化钠的质量一定等于: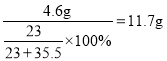 ,正确;
,正确;
C、假设氢氧化钠全部变质,最终变成碳酸钠,氢氧化钠中氧元素的质量分数为:![]() ×100%=40%,而碳酸钠中氧元素的质量分数为:
×100%=40%,而碳酸钠中氧元素的质量分数为:![]() ×100%≈45.3%,故氧元素的质量分数是增大的,错误;
×100%≈45.3%,故氧元素的质量分数是增大的,错误;
D、由于可能含有氢氧化钠,故加入盐酸不一定立即产生气泡,错误;
故选:B。


科目:初中化学 来源: 题型:
【题目】钢铁是人类利用得最多的金属材料.
(1)工业上常用赤铁矿来炼铁,其反应原理是_____(用化学方程式回答).
(2)若比较铝、铁、铜三种金属的活动性强弱,可以选择下列试剂组_____(填序号).
A Al、Fe、Cu、20%稀盐酸 B Al、Cu、FeSO4溶液
C Al、Fe、CuSO4溶液 D Fe、Cu、Al2(SO4)3溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按照“西气东输”计划,很多城区居民已用上天然气。天然气是一种无色无味的气体,密度小于空气。天然气泄漏后,遇火、静电易发生爆炸,输送天然气时,在其中混入了一种具有强烈刺激性气味的气体(硫醇)。请回答下列问题:
(1) 天然气的主要成分是CH4,它属于____(填“有机物”或“无机物”);
(2) CH4在空气中完全燃烧的化学方程式为____;
(3) 在输送的天然气中混入硫醇的目的是____;
(4) 室内发生天然气泄漏时,要立即关闭阀门,开窗通风,一定不能做的事情是_____(任填一项)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组将等质量的锌、铁、铜三种金属粉末分别加入等质量、相同质量分数的稀硫酸中,观察到铜与稀硫酸无反应,测得锌、铁与稀硫酸反应产生气体体积与时间的关系如下图所示,关于该小组的实验有下列说法,其中正确的是( )
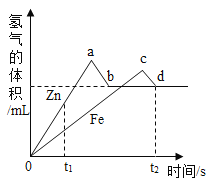
A.从t1时间就可以得出金属活动性:Zn>Fe>Cu
B.一定时间内气体体积从a降到b说明装置气密性不好
C.a>c是说明Zn生成的氢气比Fe多
D.反应结束后Fe一定剩余,Zn可能剩余
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将1.80g氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,过滤后得到溶质质量分数为20.0%的溶液5.85g。已知氯化铜与氢氧化钠溶液反应的化学方程式为:CuCl2+2NaOH =Cu(OH)2↓+2NaCl
求:(1)样品中氯化铜的质量_____;
(2)加入氢氧化钠溶液的质量_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)俗称摩尔盐,可用于净水和治疗缺铁性贫血。工业上常利用机械加工行业产生的废铁屑(含有少量杂质 Fe2O3)为原料制备(如图)。
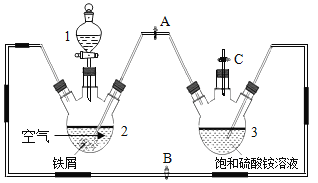
某化学兴趣小组拟用下列方案制备硫酸亚铁铵并进行相关探究。 查阅资料:
(1)FeSO4易被氧气氧化为Fe2(SO4)3,影响硫酸亚铁铵的等级。
(2)在FeSO4溶液中加入(NH4)2SO4固体可制备硫酸亚铁铵晶体,该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
(3)在0~60℃时,硫酸亚铁铵的溶解度比硫酸铵、硫酸亚铁的溶解度小,冷却混合液至室温便析出硫酸亚铁铵。
(探究一)用如上图所示装置制备硫酸亚铁铵。实验步骤如下:
①制备 FeSO4溶液:先关闭止水夹 A,再打开止水夹 B和 C,从分液漏斗滴加稀硫酸至三颈烧瓶2中,此装置中发生的化学反应主要有(用化学方程式表示)______、_______和![]() 。该过程中氢气的作用是______。
。该过程中氢气的作用是______。
②待装置中的铁屑快反应完时,关闭止水夹_______,打开止水夹_______,观察到的现象是_______。实验时为防止三颈烧瓶2中剩余铁屑通过导管进入三颈烧瓶3中,可采取的措施 是_______。
③放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵晶体,从中获得硫酸亚铁铵晶体的主要实验操作为过滤、洗涤、干燥。为洗涤(NH4)2SO4·FeSO4·6H2O 粗产品,下列方法中最合适的是______。
A 用冷水洗 B 先用冷水洗,后用无水乙醇洗
C 用 30%的乙醇溶液洗 D 用 90%的乙醇溶液洗
(探究二)探究硫酸亚铁铵样品的纯度取5g硫酸亚铁铵晶体溶于50mL水配成溶液,等分成两份,分别进行实验。
方案一:![]()
(1)实验中加入过量BaCl2溶液的目的______。
(2)利用方案一测得的数据,计算该硫酸亚铁铵样品的纯度(列出具体计算步骤)。((NH4)2SO4·FeSO4·6H2O的相对分子质量:392)__________
方案二:如图所示,向另一份中加入过量的NaOH溶液,充分反应后得到NH3
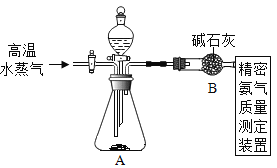
(3)(NH4)2SO4与NaOH反应的化学方程式为_______。
(4)实验中需不断通入高温水蒸气,其作用是_______。
(5)在实际测量中,利用方案二测得的样品纯度总是低于方案一测得的数值,可能的原因是______。
(探究三)对硫酸亚铁铵((NH4)2SO4·FeSO4·6H2O)晶体进行热重分析,温度与TG%的关系如下图所示
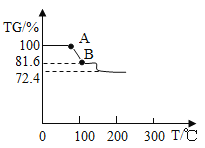
已知:温度低于 200℃,只有结晶水失去。
已知:TG% =![]()
TG%从 100%降低为 72.4%时,发生反应的化学方程式是_______ 。试计算AB段物质的化学式______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属及金属材料由于具有优良的性能,在生产和生活中发挥着极其重要的作用,种类繁多的金属材料已成为社会发展的重要物质基础。
(1)人类文明与金属材料的发展应用关系密切,下列三种金属中,使用年代最久远的是_____填序号)。
①铁 ②铝 ③铜
(2)铁是全世界目前应用最为广泛的金属,如汽车、轮船的外壳都是铁制品,但每年因钢铁生锈造成的损失约占钢铁生产总量的三分之一,请写出一种防止钢铁生锈的措施__________。
(3)生铁的主要成分是铁,通常还含有2%-4.3%的杂质碳,请判断生铁属于_____(填“复合材料”、“合金”、“有机高分子材料”“硅酸盐材料”之一)。
(4)取5.8克生铁样品于烧杯中,加入10%硫酸溶液充分反应,生成气体与加入硫酸溶液的质量关系如下图所示,计算当加入硫酸溶液98g时,所得不饱和溶液中溶质的质量__________ (生铁中的杂质不与硫酸反应,也不溶于水)
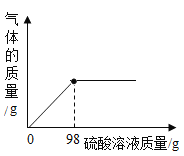
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某固体混合物X中,可能含有CuSO4、NaCl、NH4NO3、FeCl3四种物质中的两种或多种。欲探究其组分,按如图所示进行探究实验,出现的现象如图中所述:(设过程中所有发生的反应都恰好完全进行)
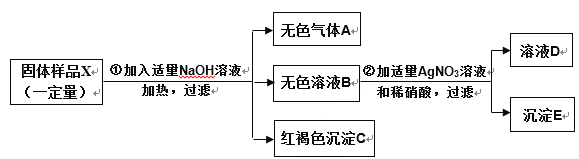
试根据上述实验信息,回答下列问题:
(1)将气体A通入无色酚酞试液,溶液呈_________色。
(2)沉淀C的化学式是________。
(3)固体样品X中,上述四种物质中,一定存在的物质是(写化学式)___________,一定不存在的物质是(写化学式)____________。
(4)实验证明,在溶液D中,肯定存在的酸根离子是(写离子符号)________________。
(5)写出步骤②中发生反应的一个化学方程式:______________。
(6)固体样品X中,仍不能确定的物质是(写化学式)___________,你的理由是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】玩转盘是同学们喜闻乐见的游戏。在如图所示的转盘中,序号①~④分别代表碳酸钠、硫酸铜、氢氧化钙、硫酸四种物质中的一种,其中③和④发生的是中和反应。请在相应的序号后填入它们的化学式,使其相邻的物质间能够相互反应:
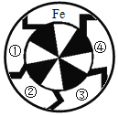
(1)写出氢氧化钙的一种用途:_____。
(2)①_____;④_____。
(3)其中②+③反应的化学方程式为:_____。
(4)能替代转盘上铁的物质是_____(填标号)
A 汞 B 镁 C 氢氧化钠 D 氯化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com