
| 实验方法 | 实验现象 | 实验结论 |
| 取少量黄色金属块并置于试管中,再向试管中滴加少量的盐酸 | 若有少量气体产生 若无气体产生 | 原试样为黄铜 原试样为黄金 |
分析 (1)根据金属活动性顺序中氢前金属可以和酸反应生成氢气,而氢后金属不会与盐酸反应,可知金不会与盐酸反应;而铜锌合金中锌会与盐酸反应,所以铜锌合金加入盐酸中会有气泡产生.
(2)①根据铜绿受热分解的反应写出反应化学方程式;
②根据质量守恒定律分析判断回答.
解答 解:(1)根据金属活动性顺序可知金位于氢之后,不会与盐酸反应,而铜锌合金中锌位于氢之前,所以铜锌合金加入盐酸中会有气泡产生.所以实验方法、现象和结论为:
| 实验方法 | 实验现象 | 实验结论 |
| 取少量黄色金属块并置于试管中,再向试管中滴加少量的盐酸 | 若有少量气体产生 若无气体产生 | 原试样为黄铜 原试样为黄金 |
点评 本题考查金属活动性顺序及其应用,同时要求正确书写实验方案.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸难挥发,可以敞口放置 | B. | 高锰酸钾与有机物可以放在一起 | ||
| C. | 剩余的BaCl2残液倒入下水道中 | D. | 酒精可以密封在无色试剂瓶中 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水的实验中不变的量只有原子个数 | |
| B. | 过滤可以除去水中所有的杂质 | |
| C. | 澄清的矿泉水是纯水 | |
| D. | 在生活中,常用煮沸来降低水的硬度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
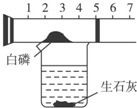 某同学用如图所示装置粗略地测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一可滑动的活塞,活塞左端管内有密封的空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度为5cm处.(提示:生石灰与水反应放出大量的热,白磷是足量的)回答下列问题:
某同学用如图所示装置粗略地测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一可滑动的活塞,活塞左端管内有密封的空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度为5cm处.(提示:生石灰与水反应放出大量的热,白磷是足量的)回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4P+5O2═2P2O5 | B. | Cu+2AgNO3═2Ag+Cu(NO3)2 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | NaOH+HCl═NaCl+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
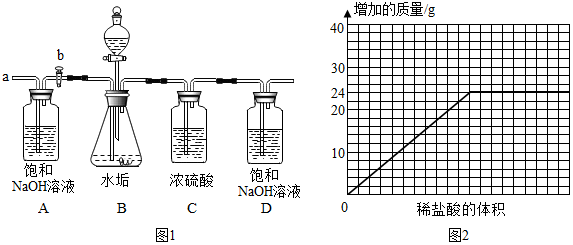
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com