
【题目】如图1是以石灰石为原料制备高纯超细碳酸钙的工艺流程图:

(1)流程中操作A的名称_____。实验室里该操作用到的玻璃仪器有烧杯、_____和_____。
(2)主要反应原理:
①“煅烧”步骤:主要反应的化学方程式为_____,反应基本类型为_____反应。
②“浸出”步骤:CaO+2NH4Cl=CaCl2+H2O+2NH3↑。
③“碳化”步骤:CO2+2NH3+H2O+CaCl2=CaCO3↓+2 NH4Cl。
(3)煅烧石灰石得到的固体中,除含CaO外,还含有少量MgO、FeO等杂质,在“浸出”过程为保证铁、镁等杂质不被浸出,需要适当提高溶液的pH.根据反应②计算出的钙铵比(参加反应的氧化钙和氯化铵的质量比)为_____,而实际流程中最佳钙铵比要稍高于这一比值,原因是_____。
(4)用上述流程可循环使用的物质除了H2O、CO2和NH3之外,还有_____。
(5)实验室在如图2装置中模拟上述流程制备高纯超细碳酸钙:

①搅拌的作用是_____。
②制备CaCl2溶液时需要对装置加热,主要作用是_____。
A 加快反应速率 B 促进氨气逸出
③已知在常温和一个标准大气压下,CO2和NH3在100g水中分别能溶解0.169g和52.9g。制备CaCO3时应先通入氨气后通入二氧化碳,理由是_____。
④浸取一步中NH4Cl溶液的溶质质量分数直接影响着生成CaCl2溶液溶质质量分数。已知0﹣100℃时NH4Cl的溶解度如下表:
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解(g) | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
如果用200g 80℃时NH4Cl的饱和溶液与纯氧化钙恰好完全反应,计算充分反应后得到CaCl2的质量_____。(写出计算过程,保留一位小数。)
【答案】过滤 漏斗 玻璃棒 CaCO3![]() CaO+CO2↑ 分解 56:107 控制为碱性环境 NH4Cl 加速反应 AB 增加二氧化碳的溶解和反应能力 82.2g
CaO+CO2↑ 分解 56:107 控制为碱性环境 NH4Cl 加速反应 AB 增加二氧化碳的溶解和反应能力 82.2g
【解析】
(1)流程中操作A实现了固体和液体分离,为过滤。实验室里该操作用到的玻璃仪器有烧杯、漏斗和玻璃棒;
(2)①“煅烧”步骤:是碳酸钙在高温下分解为氧化钙和二氧化碳,对应的化学方程式为 CaCO3![]() CaO+CO2↑,该反应是由一种生成两种物质,属于分解反应;
CaO+CO2↑,该反应是由一种生成两种物质,属于分解反应;
(3)煅烧石灰石得到的固体中,除含CaO外,还含有少量MgO、FeO等杂质,在“浸出”过程为保证铁、镁等杂质不被浸出,MgO、FeO能与酸性物质反应,需要适当提高溶液的pH,根据反应②计算出的钙铵比(参加反应的氧化钙和氯化铵的质量比)![]() 即钙铵比为 56:107,实际流程中最佳钙铵比要稍高于这一比值,原因是控制为碱性环境;
即钙铵比为 56:107,实际流程中最佳钙铵比要稍高于这一比值,原因是控制为碱性环境;
(4)NH4Cl在“浸出”步骤中是反应的反应物,在“碳化”步骤中是反应的生成物。在用上述流程可循环使用的物质除了H2O、CO2和NH3之外,还有 NH4Cl;
(5)①搅拌的作用是加速反应;
②制备CaCl2溶液时需要对装置加热,目的加快反应速率和促进氨气逸出。故选AB;
③一个标准大气压下,CO2和NH3在100g水中分别能溶解0.169g和52.9g。制备CaCO3时应先通入氨气后通入二氧化碳,理由是增加二氧化碳的溶解和反应能力;
④如果用200g 80℃时NH4Cl的饱和溶液中氯化铵的质量=![]() ;
;
设:充分反应后得到CaCl2的质量为x。
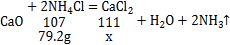
![]() x=82.2g。
x=82.2g。


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
【题目】氨气(NH3)是一种重要的化工原料。
(1)氨气属于_____(填序号)。
A 混合物 B 纯净物 C 化合物 D 氧化物
(2)在高温和催化剂的条件下,可由氨气获得氢气,其反应类型与水电解制氢气相同。该反应的化学方程式为_____。
(3)尿素(CO(NH2)2)可以制氨气,反应的微观示意图如下:

该反应生成物甲和乙的分子个数比为_____;该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下。
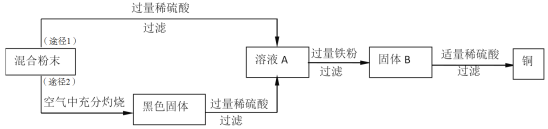
请根据流程图,回答下列问题:
(1)稀硫酸的溶质是H2SO4,其中硫元素的化合价为_________。
(2)固体B所含的物质是________(填物质化学式),溶液A加入过量铁粉的化学方程式是_________(任写一个)。
(3)检验得到的铜是否含铁粉的的操作是__________。
(4)途径2与途径1比较,途径2优点是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活离不开化学,生活之中处处有化学,请你根据现有的化学知识和生活经验完成下列各个题。
(1)长期饮用硬度过大的水,会损害人体健康,生活中将硬水软化的方法是______。
(2)倒开水时,为了防止瓶塞沾上其他物质,取下瓶塞时应______放。
(3)现在许多城市家庭都用上了天然气,天然气主要成分燃烧的化学方程式为______。
(4)自行车作为常用代步工具,既轻便灵活,又符合环保要求。
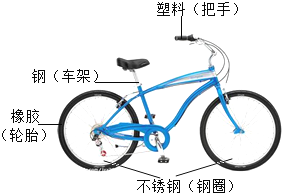
①上图所标物质中属于金属材料的是______。(填一种即可)
②车架表面刷油漆主要是为了防锈,其原理是______。
(5)烧菜时,锅内的油着火时,最简单的灭火方法是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氰氨基化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为CaCO3+2X=CaCN2+CO↑+H2↑+CO2↑.该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物B. 反应后气体质量减少
C. X的化学式为HCNOD. X溶液的![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月5日,国产大型客机C919首飞成功(如图所示),实现中国航空工业重大历史突破。回答下列问题:

(1)图中标示的材料中,橡胶属于______________(填“合成材料”或“金属材料”)。
(2)国产大型客机C919的综合监视电子系统的核心部件是其中的电子芯片,制备该电子芯片的主要材料是硅。硅单质与金刚石结构相似,则构成硅单质的粒子是_________________(填序号)。
①原子 ②分子 ③离子
(3)锂原子(Li)结构示意图为![]() ,易失去最外层的一个电子,则锂离子符号是________。
,易失去最外层的一个电子,则锂离子符号是________。
(4)在空气中,铝比铁具有更好的抗腐蚀性,原因是____________________(填化学方程式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一不纯的Na2CO3样品,杂质可能是K2CO3、FeCl3、CaCO3和NaCl中的一种或几种,取该样品10.6克,加入足量的稀盐酸完全反应得到无色溶液,同时产生4.48克气体,下列判断正确的是( )
A. 杂质一定有FeCl3和CaCO3
B. 杂质一定没有NaCl
C. 杂质可能是K2CO3、CaCO3和NaCl组成
D. 杂质可能是K2CO3和NaCl组成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中无时不在进行着氧气、二氧化碳、水的循环,使地球充满勃勃生机.
(1)地球大气中二氧化碳含量增多,会产生_____,导致全球变暖。
(2)对维持大气中二氧化碳气体含量相对稳定,最重要的反应是______
ACO2+H2O=H2CO3 BCO2+NaOH=Na2CO3+H2O
CCO2+ C ![]() 2CO D6CO2 +6H2O
2CO D6CO2 +6H2O![]() 6C6H12O6+6O2
6C6H12O6+6O2
(3)饮用硬度过大的水都不利于人体健康.可通过_____方法来降低水的硬度。
(4)相同条件下气体体积之比等于分子数之比,则空气中氧分子与氮分子总质量之比为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com