
【题目】“细菌冶金”的原理是利用氧化铁硫杆菌促使黄铁矿(主要成分![]() )氧化成硫酸铁和硫酸,并能为
)氧化成硫酸铁和硫酸,并能为![]() 和
和![]() 合成有机物提供能量。流程如图,下列说法错误的是( )
合成有机物提供能量。流程如图,下列说法错误的是( )
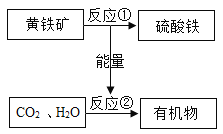
A.整个流程提高了能量的利用率
B.图中有机物一定不含氧元素
C.反应①:![]() ,X为
,X为![]()
D.氧化铁硫杆菌在反应①中起催化作用
【答案】BC
【解析】
氧化铁硫杆菌促使FeS2氧化成硫酸铁和硫酸释放的能量供给二氧化碳和水的反应,提高了能量的利用率;二氧化碳和水反应生成有机物时,部分或全部氧元素转化到有机物;根据化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数都不变;氧化铁硫杆菌在反应①中,能够促使FeS2氧化成硫酸铁和硫酸,起催化作用。
A、借助利用氧化铁硫杆菌促使FeS2氧化成硫酸铁和硫酸释放的能量供给二氧化碳和水的反应,提高了能量的利用率,故A正确;
B、二氧化碳和水反应生成有机物时,部分或全部氧元素转化到有机物中,故B不正确;
C、由![]() 可知,反应前后铁原子都是4个,硫原子都是8个,反应后氧原子是32个,反应前应该是32个,其中2个包含在2X中,反应后氢原子是4个,反应前应该是4个,包含在2X中,因此X为
可知,反应前后铁原子都是4个,硫原子都是8个,反应后氧原子是32个,反应前应该是32个,其中2个包含在2X中,反应后氢原子是4个,反应前应该是4个,包含在2X中,因此X为![]() ,故C不正确;
,故C不正确;
D、氧化铁硫杆菌在反应①中,能够促使FeS2氧化成硫酸铁和硫酸,起催化作用,故D正确。故选BC。


科目:初中化学 来源: 题型:
【题目】(5分)在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示。
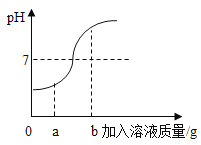
(1)该反应的化学方程式为 。
(2)该实验操作是将 滴加到另一种溶液中。
(3)当加入溶液的质量为a g时,所得溶液中的溶质为 (写化学式)。
(4)当加入溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包混有少量Na2CO3和CaCO3的NaCl固体,为除去其中的杂质,设计流程如图,请回答下列问题:
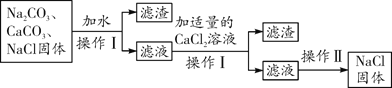
(1)在操作Ⅰ前加入水的目的____________。
(2)操作II名称是__________,其中玻璃棒的作用是__________
(3)写出除杂过程中发生的化学方程式__________。该反应属于____________(填写基本反应类型)。
(4)求出Na2CO3中碳元素的化合价:______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是常见酸、碱、盐之间的相互转化关系.
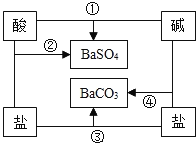
(1)写出图中相应物质的化学式:酸_____________碱____________
(2)图中反应②的化学方程式:___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在利用红磷燃烧测定空气中氧气含量的实验中用传感器记录集气瓶中压强、温度随时间的变化情况如图所示,其中a是打开止水夹的时刻。下列说法不正确的是( )
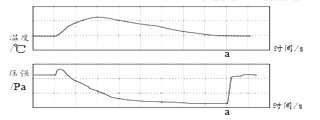
A. a时处的压强等于大气压B. 反应开始压强增大是因为温度升高
C. a时的温度已经接近室温D. a时以后气压增大是由于水倒吸入集气瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿矾(![]() )是硫酸法生产钛白粉的主要副产物,可用于制备
)是硫酸法生产钛白粉的主要副产物,可用于制备![]() ,复印用
,复印用![]() 粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
Ⅰ制备![]()
(资料一)
①无水硫酸铜遇水变成蓝色的硫酸铜晶体。
②绿矾(![]() )高温分解产生一种金属氧化物和几种气态非金属氧化物。
)高温分解产生一种金属氧化物和几种气态非金属氧化物。
③![]() 是无色有窒息性臭味的有毒气体,能使品红溶液褪色。
是无色有窒息性臭味的有毒气体,能使品红溶液褪色。
甲同学用如下装置制备![]() 并验证绿矾受热分解的其他产物;
并验证绿矾受热分解的其他产物;
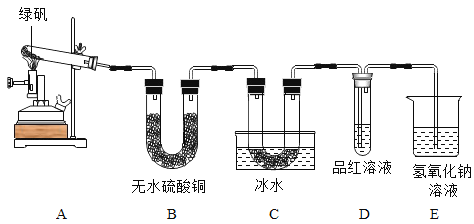
(1)实验过程中发现:A中有______色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体(![]() )析出,D中品红溶液褪色,装置E的作用是______,E的反应的化学方程式为______。绿矾高温分解的化学方程式为______。
)析出,D中品红溶液褪色,装置E的作用是______,E的反应的化学方程式为______。绿矾高温分解的化学方程式为______。
Ⅱ制备Fe3O4
乙同学模拟生产复印用![]() 粉的实验流程如下:
粉的实验流程如下:
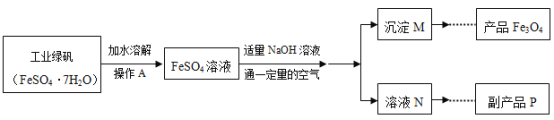
(资料二)①![]() 是一种白色难溶于水的固体,在空气中易被氧化成
是一种白色难溶于水的固体,在空气中易被氧化成![]() 。
。
(1)![]() 溶液中加入NaOH溶液,反应的化学方程式依次为①______,②____。由沉淀M获得
溶液中加入NaOH溶液,反应的化学方程式依次为①______,②____。由沉淀M获得![]() 的化学方程式为:
的化学方程式为:![]()
(2)控制“一定量空气”的目的是控制![]() 的转化率,沉淀M中
的转化率,沉淀M中![]() 和
和![]() 的最佳质量比为______。
的最佳质量比为______。
(3)副产品P是![]() 晶体,从溶液N获得该晶体的操作顺序是b→______→______→d
晶体,从溶液N获得该晶体的操作顺序是b→______→______→d
a过滤 b加热浓缩 c冷却结晶 d加热至完全失去结晶水
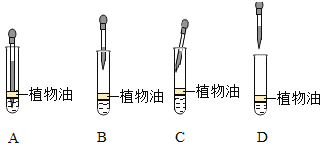
(4)若制取![]() ,采取的实验操作是:向盛有5mL新制
,采取的实验操作是:向盛有5mL新制![]() 溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶
溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶![]() ),胶头滴管的正确使用方法是______(填字母)。
),胶头滴管的正确使用方法是______(填字母)。
Ⅲ制备还原铁粉
制备还原铁粉的工业流程如下:
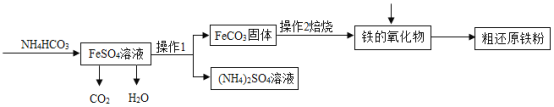
(1)操作1的名称是______, ![]() 和
和![]() 溶液反应的化学方程式为______。
溶液反应的化学方程式为______。
(2)若将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量![]() )在氧气流中完全反应,得到0.22g
)在氧气流中完全反应,得到0.22g![]() ,将相同质量的粗还原铁粉与足量稀硫酸反应,得到048g
,将相同质量的粗还原铁粉与足量稀硫酸反应,得到048g![]() (
(![]() 与稀硫酸不反应)。试通过计算确定
与稀硫酸不反应)。试通过计算确定![]() 的化学式(请写出计算过程)______。
的化学式(请写出计算过程)______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室部分装置如图所示,请回答下列问题.

(1)选择发生和收集O2的装置,填写在下表中(填字母).
选用药品 | 发生装置 | 收集装置 |
H2O2溶液、MnO2 | ______ | ______ |
KMnO4 | ______ |
(2)如果用MnO2与浓H2SO4加热制备O2,可选用的发生装置是______(填字母).
(3)选用F装置收集气体时,下列实验操作正确的是______(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是______.若需制备3.2g O2,至少需要消耗______gKMnO4(已知KMnO4的相对分子质量为158)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】闪锌矿(主要成分为ZnS)经焙烧得锌焙砂,锌焙砂主要含Zn、![]() ,以及少量FeO、CuO,工业上用其制备金属锌,具体过程如图所示:
,以及少量FeO、CuO,工业上用其制备金属锌,具体过程如图所示:

(1)操作X的名称是________;
(2)进行反应①时,要将锌焙砂粉碎成细小颗粒,目的是________;
(3)![]() 可看作是由两种氧化物结合而成它与稀
可看作是由两种氧化物结合而成它与稀![]() 反应生产两种盐,分别是
反应生产两种盐,分别是![]() 和________(填化学式)。
和________(填化学式)。
(4)参加反应②的物质为![]() 和________(填化学式);
和________(填化学式);
(5)写出反应③的化学方程式:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲乙两种固体物质溶解度曲线如图所示;
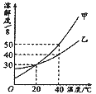
(1)20℃时,甲和乙溶解度关系是___;
(2)20℃时,等质量的甲、乙分别溶于水形成饱和和溶液,再升温至40℃,溶液中溶质的质量分数的大小关系是___;
(3)将40℃70g乙的饱和和溶液降温到20℃,可析出晶体质量为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com