
【题目】A、B、C、D、E、F六种物质都是初中化学内容中涉及的化合物,转化关系如下图,其中D是最常见的溶剂。

(1)根据上图推断,A是_____,D是______,E是______(填写化学式);
(2)写出反应④的化学方程式:_____________________________;
(3)写出A物质的一种用途______________。
【答案】CaCO3 H2O Ca(OH)2 Na2CO3+ Ca(OH)2= CaCO3↓+2NaOH 作建筑材料(合理均可)
【解析】
根据题干提供的信息进行分析,D是最常见的溶剂,则D是水;A高温分解生成的C能与氢氧化钠反应生成水,则C是二氧化碳,生成的F是碳酸钠;A是碳酸钙,B是氧化钙;氧化氧化钙能与水反应生成氢氧化钙,故E是氢氧化钙;氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,据此解答。
(1)A是碳酸钙,D是水,E是氢氧化钙,故填:CaCO3;H2O;Ca(OH)2。
(2)反应④氢氧化钙能与碳酸钠反应生成氢氧化钠和碳酸钙,故填:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
(3)A是碳酸钙,是石灰石或大理石的主要成分,可以用作建筑材料等;故填:作建筑材料。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】(1)化学用语是国际通用语言,是学习化学的重要工具。请用化学用语填空:
①3个铝原子__________________;
②氯离子__________________;
③2个氢分子__________________;
④钾元素__________________;
⑤标出二氧化碳中碳元素的化合价__________________。
(2)在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。下图是四种粒子结构示意图。
A  B
B  C
C  D
D 
①D中的X=_______________。
②A、B、C、 D中属于同种元素的粒子是____________ (填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是( )
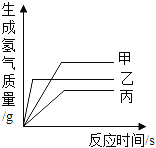
A. 金属活动性:乙>甲>丙 B. 生成氢气的质量:甲>乙>丙
C. 相对原子质量:乙>丙>甲 D. 消耗硫酸的质量:甲>乙>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知NaHCO3受热分解生成Na2CO3,![]() 。把12克NaHCO3和Na2CO3的混合物样品加热至完全反应,剩余固体的质量为8.9克。下列说法正确的是( )
。把12克NaHCO3和Na2CO3的混合物样品加热至完全反应,剩余固体的质量为8.9克。下列说法正确的是( )
A. 反应生成的CO2质量为4.4克B. 样品中Na2CO3的质量分数为30%
C. 样品中NaHCO3的质量为8.6克D. 样品中钠元素的质量分数为43.3%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据以下粒子结构示意图,其中说法不正确的是( )
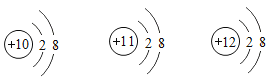
A.它们表示的是同一种元素
B.它们的核外电子数相同
C.它们都具有相对稳定的结构
D.它们依次表示原子、离子、离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习酸碱中和反应时,同学们做了稀硫酸和氢氧化钠溶液反应的实验。
(1)甲组在实验过程中测定了其中一种溶液的 pH 变化,由图可知,该小组同学测定的是_____溶液的 pH 变化,该反应的化学方程式为_____。

实验过程中,同学们取了如图中 A 点所得溶液,加入试剂_____(填序号),观察到有蓝色沉淀生成。
I、BaCl2 溶液 II. Fe2(SO4)3 溶液 III. CuSO4 溶液
结论:酸碱没有恰好中和,A 点溶液中的溶质为_____。
(2)乙组向滴有酚酞的氢氧化钠溶液中滴加稀硫酸,可观察到_____。结论:酸碱可能恰好中和,也可能硫酸过量。
为了进一步确定反应后所得溶液中是否含有硫酸,乙组同学设计了如下两种方案:
方案一:取反应后溶液于试管中,滴加碳酸钠溶液,若观察到_____,则硫酸过量;
方案二:取反应后溶液于试管中,滴加氢氧化钡溶液,若产生白色沉淀,则硫酸过量。
你认为上述两种方案,哪种不合理?并说明理由_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小组同学发现如图所示的两个试管中没有明显现象。为判断两支试管中是否发生了反应,小组同学进行了以下探究。

探究一.探究稀盐酸与氢氧化钠溶液是否发生了化学反应
[实验1]取少量氢氧化钠溶液于试管中,向其中滴加少量______溶液,然后再滴加足量的稀盐酸,观察到溶液颜色发生变化的情况是:先变红,然后_____。
[结论]稀盐酸和氢氧化钠溶液发生了反应。
探究二.探究稀盐酸和硫酸镁溶液是否发生了化学反应
小明决定通过探究试管②溶液中所含有的离子种类来判断反应是否发生。(将试管②的溶液分成两份)
[实验2]
实验 | 现象 | 结论 |
(1)测试管②中溶液的pH | pH<7 | 试管②中溶液含有氢离子 |
(2)向一份试管②的溶液中,加入足量的氢氧化钠溶液 | _________ | 试管②中溶液含有: _______ |
(3)向一份试管②的溶液中加入足量氯化钡溶液 | 产生白色沉淀 | 试管②中溶液含有: _____ |
(4)向(3)所得溶液中加入硝酸银溶液 | 产生白色沉淀 | 试管②中溶液含有氯离子 |
[结论]稀盐酸与硫酸镁溶液没有发生化学反应。
[交流与评价]小亮认为小明的实验不够严谨,其理由是______。为此小亮提出应将小明实验中某一步加入的试剂调整为另一种盐溶液,按照小亮的修改方案,最终得出“稀盐酸与硫酸镁溶液没有发生化学反应”的结论。小亮的修改方案是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫化钠是重要化工产品,主要用于皮革、毛纺、高档纸张、染料等行业。工业上利用工业尾气硫化氢(H2S)制得产品硫化钠固体。其工业流程示意图如下图:
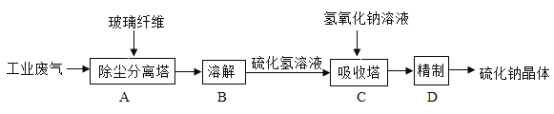
(1)图中A操作利用玻璃纤维作除尘分离塔的滤材,玻璃纤维的作用是过滤,该操作在实验室里要使用玻璃棒的作用为_____。
(2)硫化氢中硫元素的化合价为_____。硫化氢气体能溶于水,其水溶液呈酸性,称为氢硫酸,则其pH_____(填“<”、“>”或“=”)7。
(3)目前采用氢氧化钠溶液吸收工业尾气中的硫化氢,可减少空气污染。吸收塔中氢氧化钠溶液与硫化氢溶液发生硫化钠和水,写出该反应的化学方程式为_____,其基本类型为_____。
(4)产品硫化钠的物质类别属于_____(“酸”、“碱”、“盐”或“氧化物”)。硫化钠固体在空气中易氧化并易溶于水,保存硫化钠的正确方法为_____。
(5)硫化钠的溶解度随着温度升高明显增大。D操作中精制过程,从硫化钠的饱和溶液中分离出硫化钠晶体,采用的结晶方法是_____(填“蒸发溶剂”或“降温结晶”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:

(1)A点的含义是_____。
(2)若乙中混有少量甲,最好采用_____的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(3)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com