
【题目】依据下列20℃时的实验和数据回答问题。
已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g.

(1)①~⑤所得溶液属于饱和溶液的是______________________。
(2)下列关于①~⑤所得溶液的说法不正确的是______________________。
A.溶质质量:①<② B.溶液质量:②<④
C.溶质质量分数:①=③ D.⑤中溶质与溶剂的质量比为9:10
【答案】②⑤ D
【解析】
(1)由题意知20℃时,100g水中最多溶解36g氯化钠,溶液就达到饱和状态,所以②为饱和溶液,①为不饱和溶液,由题意知20℃时,100g水中最多溶解88g硝酸钠,溶液就达到饱和状态,所以⑤为饱和溶液,③④为不饱和溶液,故填②⑤;
(2)
A、由前分析可知①为氯化钠的不饱和溶液,溶质质量为30g,②为氯化钠的饱和溶液,溶质质量为36g,溶质质量①<②,故不符合题意;
B、由前分析可知②为饱和溶液,溶液质量=36g+100g=136g,溶液④为不饱和溶液,溶液质量=60g+100g=160g,溶液质量②<④,故不符合题意;
C、由上分析可知①③都是不饱和溶液,溶质、溶剂质量相等,溶质质量分数也相等,故不符合题意;
D、由前分析可知⑤为20℃时的饱和溶液,溶质质量∶溶剂质量=88g∶100g=22∶25,故符合题意;故填D。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:
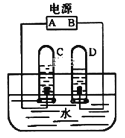
【题目】如图是简易电解水装置图,试回答问题水接通直流电可以分解,正极收集到的气体是_____(写化学式);负极收集到的气体是______(写化学式),这两种气体的体积比为_______,这一化学变化的化学方程式是 ____,此反应为______(写基反应类型)。在此过程中,我们要加入适量的氢氧化钠或硫酸钠为什么?______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题:
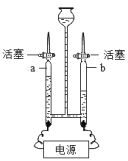
(1)从宏观上观察:电极上产生气泡快的是_____管(填“a”或“b”),a 中产生的气体是_____(填化学式)。
(2)从微观上正确的说法是_____(填字母)。
A.水由氢气和氧气组成
B.水由氢原子和氧原子构成
C.每个水分子是由 2 个氢原子和 1 个氧原子构成
(3)从符号上表示,电解水的化学方程式为_____。
(4)宏观与微观的联系:18g 水中约含_____个氢原子。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生产、生活中有着广泛的用途。请回答下列有关问题:
(1)黄铜是铜锌合金,其硬度比纯铜______(填“大”、“小”或“相同”),市面上的假金多为铜锌合金,可以采用______的方法鉴定真假金,对应化学反应方程式为______。
(2)长期露置于空气中的金属M表面会被锈蚀。经检测锈蚀物中除含有M外,还含有C、H、O三种元素,根据质量守恒定律,推测与金属M发生反应生成锈蚀物的物质:
推测Ⅰ:锈蚀物中的H来自空气中的______(填化学式,下同),C来自空气中的______,因此这两种物质肯定参加了反应。
推测Ⅱ:锈性物中的O有多种来源,因此不能确定空气中的O2是否参加了反应。
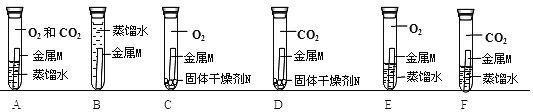
(3)某同学为了验证空气中的O2是否参加了反应,设计了如下系列实验,你认为其中必须要做的实验是______(填实验编号)。
说明:①所用蒸馏水都是经煮沸迅速冷却的;②干燥剂N只吸收水分,不吸收CO2和O2。
(4)假如要进行实验E,从实验E中得到的结论是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
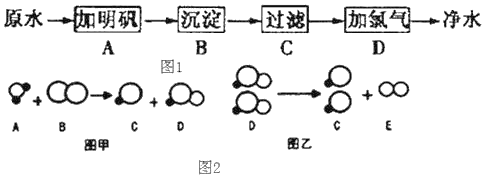
【题目】原水(未经处理的水)中含有泥沙悬浮物和细菌等杂质,可用次氯酸杀死细菌。氯气溶解于水时,可生成盐酸和次氯酸。某水厂生产自来水的净化步骤如图1所示:
(1)A步骤中加明矾的作用为_____。
(2)该厂生产的自来水是_____。(填“纯净物”或“混合物”)
(3)能消毒杀菌的步骤为_____(填标号)。自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用如图2表示:(![]() 表示氧原子;
表示氧原子;![]() 表示氢原子;
表示氢原子;![]() 表示氯原子)
表示氯原子)
①图乙所示反应的基本反应类型为_____反应;
②上述物质中,属于氧化物的有_____(填化学式);
③根据图甲微观示意图得出的结论中,正确的是_____。
A.反应前后各元素的化合价都不变
B.化学反应的实质就是原子的重新组合
C.反应前后分子种类不变
D.该反应中C和D的分子个数比1:1
(4)日常生活中使用硬水会带来许多麻烦,家庭生活中常用来降低水硬度的方法_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高锰酸钾在生产、生活中有广泛的应用。实验小组同学查阅资料得知,草酸(H2C2O4)可使滴有硫酸的高锰酸钾溶液褪色,但不同条件下褪色时间不同,即反应的速率不同。小组同学进行了如下探究。
(提出问题)影响该反应反应速率的因素有哪些?
(作出猜想)影响该反应反应速率的因素有温度、催化剂、硫酸的浓度等。
(查阅资料)硫酸锰(MnSO4)可作该反应的催化剂。
(进行实验)取A、B、C、D 4支试管,每支试管中分别加入4mL 0.08% 的KMnO4 溶液、0.4 mL 的硫酸、1mL 0.09% 的 H2C2O4 溶液。

(实验记录)
序号 | 所滴硫酸浓度 | 温度 | 催化剂 | 高锰酸钾完全褪色时间 |
A | 98% | 室温 | 无 | 72s |
B | 65% | 室温 | 无 | 129s |
C | 65% | 50℃ | 无 | 16s |
D | 65% | 室温 | MnSO4 | 112s |
(解释与结论)
(1)草酸使高锰酸钾溶液褪色反应的化学方程式如下,请在横线上补全方程式。
2KMnO4 + 5H2C2O4 + 3H2SO4 == K2SO4 + 2MnSO4 + 10_______+ 8H2O
(2)4支试管中作为对照实验的是_______(填序号,下同)。
(3)设计实验A和B的目的是 ______________________________。
(4)对比实验B和C可得出的结论是_____________________________。
(5)探究催化剂对该反应反应速率影响的实验是____________________________。
(反思与交流)
(6)影响该反应反应速率的因素除温度、催化剂、硫酸的浓度外,还可能有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图示实验所得出的结论中,不正确的是()
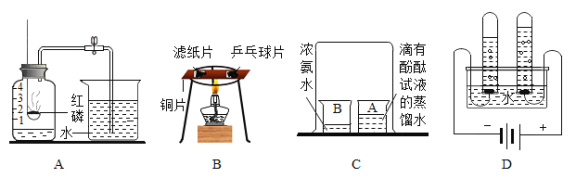
A. 氧气约占空气体积的1/5 B. 燃烧条件之一:温度需达到可燃物的着火点
C. 氨气分子在不断的运动 D. 水是由氢气和氧气组成的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁在日常生活中有着重要作用。请回答:
(1)铁生锈实际上是铁与空气中的氧气和______(填名称)发生反应的结果,生活中可以采用______(写一种方法即可)的方法防止铁制品生锈。
(2)铁在高温下与水蒸气反应生成四氧化三铁和氢气。该反应的化学方程式为:______,该反应属于______反应(填基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学中常见的五种物质。其中A、D是黑色固体,B、C、E是无色气体,B的相对分子质量小于气体C,化合物D含有地壳中含量居第二位的金属元素。它们在一定条件下的转化关系如图所示(→表示转化)。请回答下列问题: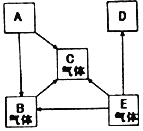
(1)写出物质的化学式A______,D______;
(2)评价物质B的“利”与“弊”(各写一例)利:______,弊:______;
(3)写出下列反应的化学方程式:B→C______;
(4)写出物质C的一种用途______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com