
| A、36% | B、32% | C、90% | D、40% |
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:
 某研究性小组做了如下的实验:取50g石灰石样品(杂质不溶于水,不发生化学反应,也不含钙元素)放入锥形瓶中,并加入足量稀盐酸.实验装置如下图所示,已知锥形瓶连同瓶中石灰石样品和稀盐酸以及瓶口棉花起始时的总质量为300.0g.实验数据记录如下表:
某研究性小组做了如下的实验:取50g石灰石样品(杂质不溶于水,不发生化学反应,也不含钙元素)放入锥形瓶中,并加入足量稀盐酸.实验装置如下图所示,已知锥形瓶连同瓶中石灰石样品和稀盐酸以及瓶口棉花起始时的总质量为300.0g.实验数据记录如下表:| 时间/min | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
| 电子天平示数/g | 294.5 | 290.0 | 286.0 | 284.0 | 283.0 | 282.4 | M | 282.4 |

查看答案和解析>>
科目:初中化学 来源: 题型:
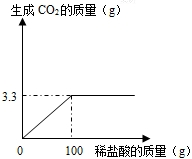 某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取样品10g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应,也不分解),向其中加入足量的稀盐酸,根据实验测得的数据绘制下图.
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取样品10g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应,也不分解),向其中加入足量的稀盐酸,根据实验测得的数据绘制下图.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
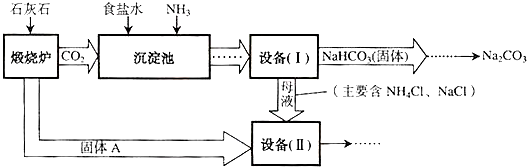
| ||
| ||
| 反应时间 | T0 | T1 | T2 | T3 | T4 | T5 | T6 |
| 反应后固体的质量 | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com