
【题目】用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.

内容 步骤 | (实验1)研究燃烧条件 | (实验2)研究氧气性质 |
Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导 管口放置一小块白磷,塞 紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭 点燃木炭后,迅速将燃烧 匙伸入瓶中,塞紧瓶塞 |
Ⅱ | 推入适量H2O2 溶液 | 推入适量H2O2 溶液 |
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为_____.
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是_____; 推入H2O2溶液后,观察到烧杯中的现象是_____.
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_____;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.该实验中,集气瓶内压强的变化过程是_____.
【答案】2H2O2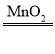 2H2O+O2↑ 燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触 导管口有气泡冒出,白磷燃烧 助燃性 先变大,一段时间后变小
2H2O+O2↑ 燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触 导管口有气泡冒出,白磷燃烧 助燃性 先变大,一段时间后变小
【解析】
(1)H2O2稀溶液与MnO2接触时生成水和氧气;
(2)根据燃烧的条件分析;燃烧的条件是:物质具有可燃性、与氧气接触、达到着火点;
(3)根据信息:推入H2O2溶液后,观察到木炭燃烧得更剧烈,分析解答。
(1)H2O2稀溶液与MnO2接触时生成水和氧气,反应的方程式是:2H2O2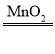 2H2O+O2↑;
2H2O+O2↑;
(2)根据燃烧的条件可知,燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触;推入H2O2溶液后,生成氧气,氧气通过导管进入烧杯,所以观察到烧杯中的现象是导管口有气泡冒出,水中的白磷接触到氧气也会燃烧;
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是助燃;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶;该实验中,木炭燃烧放热,集气瓶内压强增大,木炭熄灭后冷却一段时间,由于消耗氧气,集气瓶内压强减小,该实验过程中,压强的变化过程是,先变大,一段时间后变小,因为生成的二氧化碳被氢氧化钠溶液吸收了。
故答案为:(1)2H2O2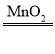 2H2O+O2↑;(2)燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触;导管口有气泡冒出,白磷燃烧;(3)助燃性;先变大,一段时间后变小.
2H2O+O2↑;(2)燃烧匙中白磷不燃烧是因为未达到白磷的着火点,烧杯中白磷未燃烧是因为没有与O2接触;导管口有气泡冒出,白磷燃烧;(3)助燃性;先变大,一段时间后变小.


科目:初中化学 来源: 题型:
【题目】化学使世界更美好,通过学习,我们有很多的收获。
收获一:世界万物都是由元素组成的,请用适当的化学符号填空:
①正三价的铝元素__________;
②硝酸钾中的原子团__________;
③人体中含量最多的物质:__________;
④植物光合作用的原料___________;
⑤海水中除了水之外,含量最丰富的物质是________。
收获二:我们学会了从宏观和微观的角度认识物质世界。
①在水、铜和氮气三种物质中,__________(填化学式)是由原子直接构成的;
②“O”和“●”表示不同元素的原子,以下图示表示单质的是__________(选填编号);
A 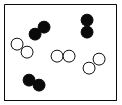 B
B 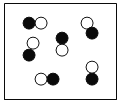 C
C 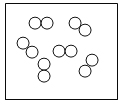 D
D 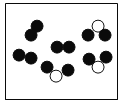
③食品中常加入防腐剂——苯甲酸钠![]() 。该防腐剂由_________;种元素组成,摩尔质量为__________;0.1mol的苯甲酸钠中约含有__________个氧原子。
。该防腐剂由_________;种元素组成,摩尔质量为__________;0.1mol的苯甲酸钠中约含有__________个氧原子。
收获三:生活中处处有化学,“家”就是一个化学小世界,蕴含丰富的化学知识。
①某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指_________(选填“元素、原子、单质”)。
②下表为几种家用清洁剂的功能及有效成分:
名称 | 功能 | 有效成分 |
漂白精 | 快速漂除衣物污渍 | HC1 H2O |
洁厕灵 | 有效清除污垢与异味 | HC1 NaClO |
活氧彩漂 | 漂洗使衣物色彩鲜艳 | NaClO H 2O 2 |
I.这些清洁剂属于_________(选填“混合物”或“纯净物”),若不小心把“洁厕灵”打翻在大理石地面上,会出现__________的现象;
Ⅱ.![]() 中氢、氧元素质量比为________;
中氢、氧元素质量比为________;
Ⅲ.“洁厕灵”与“漂白精”不能混用,二者混合易产生一种有毒气体X。反应原理为: ![]() ,则X的化学式为________。
,则X的化学式为________。
③玻璃中的主要成分![]() 属于__________(选填“金属氧化物”或“非金属氧化物”)。
属于__________(选填“金属氧化物”或“非金属氧化物”)。
④塑料诞生一百年来风光无限,它的发明者贝克兰也因此荣获“塑料之父”的美誉,而今由于人们使用不当而直接引发的一大环境问题是________(选填编号)。
A 沙尘暴 B 水土流失 C 温室效应 D 白色污染
⑤天然气的主要成分是甲烷![]() ,一个甲烷分子的质量约为_______克(只列式,不用计算结果)。
,一个甲烷分子的质量约为_______克(只列式,不用计算结果)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】密闭容器中,下列各组物质在一定条件下充分反应后,冷却至室温,密闭容器中的气态物质为纯净物的是( )
A.分子数比为1:1的![]() 和
和![]() B.物质的量比为4:3的
B.物质的量比为4:3的![]() 和
和![]()
C.质量比为1:5的![]() 和
和![]() D.质量比为3:8的
D.质量比为3:8的![]() 和
和![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜(铜和锌的合金)因性能优良,被广泛用于制作钱币、饰品和生产中,铜的质量分数在59%﹣65%之间的黄铜性能优良。兴趣小组为了解某黄铜螺母的材料性能进行如下实验:取多个黄铜螺母放入烧杯中,另取80克19.6%的稀硫酸,分四次等质量加入,每次均充分反应,实验过程数据记录如表。
实验次数 | 1 | 2 | 3 | 4 |
稀硫酸的用量/克 | 20 | 20 | 20 | 20 |
剩余固体的质量/克 | 20.0 | 17.4 | 14.8 | 13.5 |
分析上述数据,请回答下列问题:
(1)第4次实验结束后溶液的pH_____7(选填“>”“=”或“<”)。
(2)配制80克溶质质量分数为19.6%的稀硫酸,需98%的浓硫酸(密度为1.84克/厘米3)________毫升?(精确到小数点后一位)
(3)通过计算说明该黄铜螺母的材料性能是否优良。________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝元素与人类关系密切.
(1)铝是地壳中含量最高的_____元素.
(2)元素周 期 表中 铝 元素 的 信 息如图所示,其原子的核外电子数为_____.
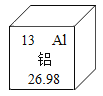
(3)铝元素在自然界中主要以Al2O3存在,Al2O3属于_____(填字母序号).
A 单质 B 氧化物 C 碱 D 盐
(4)工业用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O3 4Al+3O2↑,该反应属于基本反应类型中的_____反应.
4Al+3O2↑,该反应属于基本反应类型中的_____反应.
(5)铝可制成蒸锅,主要利用铝的延展性和_____性.
(6)药品“氢氧化铝[Al(OH)3]”片剂能与胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,该反应的化学方程式为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镍(Ni)是一种用途广泛的金属,常用于电镀工业和制造电池。硫酸镍溶液显绿色,氢氧化镍为难溶于水的绿色固体,在这些化合物中镍元素都显+2价。
(1)氢氧化镍的化学式为______。
(2)将硫酸镍溶液加入试管中,再滴加足量氢氧化钠溶液,充分振荡后静置。
① 反应的化学方程式为______。
② 预测反应现象:______。
(3)用氯化亚钯(PdCl2)可测定空气中微量的一氧化碳。常温下,氯化亚钯溶液与一氧化碳反应,生成灰黑色的金属钯(Pd)沉淀,还生成二氧化碳和盐酸,该反应的化学方程式为_____。
(4)某同学看见有人向养鱼的水中撒一种黄色固体能产生气泡,咨询得知,这种固体的主要成分是过氧化钙(CaO2),是为了解决水中氧气不足的问题,他回家查阅资料知过氧化钠(Na2O2)与水反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑,且CaO2与Na2O2的化学性质相似。据此请写出CaO2与水反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】美国两位科学家利用碘元素,借助放射学进行了“G蛋白偶联受体”研究,揭开了“细胞如何感知周围环境”之谜,获得了2012年诺贝尔化学奖.如图一是碘元素在元素周期表中的部分信息及碘原子的结构示意图.请回答:
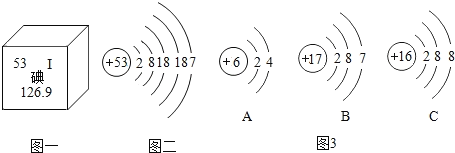
(1)由图一可知碘元素属于_______ (填“金属”或“非金属”)元素, 碘元素的相对原子质量是_________,碘元素的质子数_________;
(2)根据图二中的信息可知,碘原子在化学反应中易___________(填“得”或“失”)电子而形成碘离子,碘离子属于______(填“阴”或“失”)离子,其符号是 ______。
(3)如图3中微粒与碘元素化学性质相似的是__________(填字母),属于稳定结构的是 ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学对一久置于空气中的烧碱样品(质量为15g)的成分进行了探究。下列说法正确的是
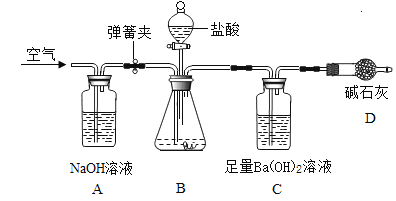
A.小组同学将样品溶于水后滴加了几滴酚酞试液,发现溶液变红,认为烧碱未完全变质
B.小明同学认为D装置的作用为了防止空气中的二氧化碳和水进入C装置
C.装置C中产生的沉淀经过一系列正确操作后,称得质量为19.7g,小组同学经过计算得出样品中氢氧化钠的质量为4.4g
D.小红同学认为将实验中的盐酸换成稀硫酸更好
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“三效催化转换器”可将汽车尾气中的有毒气体处理为无毒气体,该反应前后的微观示意图如图所示。
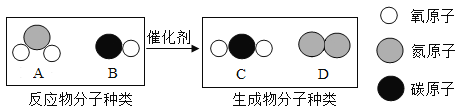
请回答下列问题:
(1)C的相对分子质量是__________。
(2)A分子、B分子、C分子的相同点是都含有氧___________(填“分子”“ 原子”或“元素”)。
(3)A物质中氮元素与氧元素的质量比是____________________。
(4)写出该反应的化学方程式_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com