
| A. | 甲>丙>乙 | B. | 乙>甲>丙 | C. | 甲>乙>丙 | D. | 丙>乙>甲 |
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:解答题
| 实验序号 | 氯酸钾质量 | 其它物质质量 | 待测数据 |
| ① | 1.5g | ||
| ② | 1.5g | CuO 0.5g | |
| ③ | 1.5g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 A、B、C三种物质的溶解度曲线如图所示,下列叙述正确的是( )
A、B、C三种物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | A的溶解度为110g | |
| B. | 40℃时60g A物质放入50g水溶解后升温至60℃时,由饱和溶液变为不饱和溶液 | |
| C. | 60℃时A、B、C三种物质的等质量饱和溶液,降温至40℃时析出晶体最多的是A | |
| D. | 60℃时A、B、C三种物质的溶液中A物质的溶液中所含溶质的质量最多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
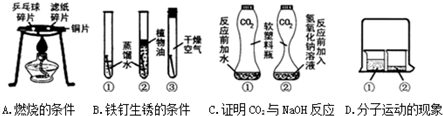
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | .1:12:28 | B. | .1:6:14 | C. | .1:6:28 | D. | .1:3:14 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量 | 8g | 35g | 5g | 8g |
| 反应后质量 | 2g | X | 5g | 42g |
| A. | X=7g | B. | 在该反应中,丙物质一定做催化剂 | ||
| C. | 该反应是分解反应 | D. | 在该反应中,甲是生成物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一个“亮菌甲素”分子中含有12个C原子10个H原子和5个O原子 | |
| B. | 78克“亮菌甲素”充分燃烧(生成H2O和CO2)时消耗48克氧气 | |
| C. | “亮菌甲素”中C、H、O三种元素的质量比为12:10:5 | |
| D. | “亮菌甲素”分子中电子数为234 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com