
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:Fe2O3能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)I.Fe2O3是反应的催化剂,反应前后__;
II.Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
III.Fe2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变.
(查阅资料)Fe2O3属于碱性氧化物,能够与稀盐酸反应生成氯化铁;氯化铁溶液显棕黄色.
(实验)用天平称量 0.3gFe2O3,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
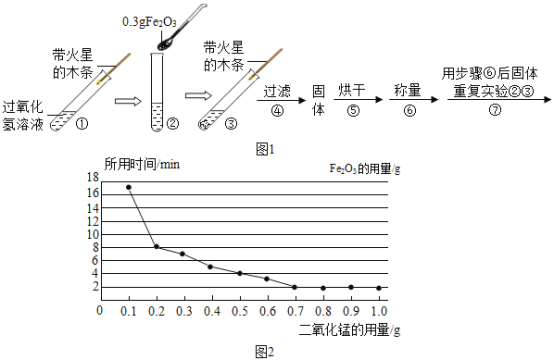
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
__,带火星的木条复燃. | __ | 溶液中有气泡放出, __ | 猜想I成立; 猜想II、III不成立. |
(2)步骤①的目的是__.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__.
(4)过氧化氢能被Fe2O3催化分解放出O2的化学方程式为__.
(拓展)
(1)要探究步骤⑤做过催化剂的Fe2O3其它化学性质,还应补做的实验是__(写一种).
(2)该同学为了探究Fe2O3的用量对H2O2分解速率的影响.每次均用30mL 10%的H2O2溶液,使用不同质量的Fe2O3作催化剂,测定每次收集到500mL O2所用的时间.结果如图(其他实验条件相同),由图可知,Fe2O3的用量对H2O2分解速率影响的规律是:
①__;
②Fe2O3的用量超出一定范围后,其用量再增大,反应速率不再继续加快.
【答案】质量和化学性质都不变 有气泡放出 Fe2O3质量仍为0.3g(或固体质量仍为0.3g) 带火星木条复燃 与步骤③对比,检验加入Fe2O3前后H2O2的分解速度有无变化 玻璃棒 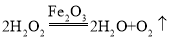 用稀盐酸(或稀硫酸)溶解固体,观察是否生成棕黄色溶液 在一定范围内,MnO2的用量越大,H2O2分解速率越快
用稀盐酸(或稀硫酸)溶解固体,观察是否生成棕黄色溶液 在一定范围内,MnO2的用量越大,H2O2分解速率越快
【解析】
[猜想]I.催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;
[实验](1)氧化铁对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以氧化铁的质量仍为0.3g,即步骤⑥、⑦的结果中的氧化铁的质量不变;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以步骤⑦的现象是溶液中有气泡放出,带火星的木条复燃;
(2)步骤①的目的是与步骤③对比,检验加入Fe2O3前后H2O2的分解速度有无变化;故填:与步骤③对比,检验加入Fe2O3前后H2O2的分解速度有无变化;
(3)过滤操作中需要的仪器是铁架台(带铁圈)、漏斗、烧杯、玻璃棒;
(4)过氧化氢在氧化铁的催化作用下生成水和氧气;学方程式为: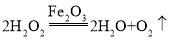 ;
;
[拓展](1)氧化铁是一种金属氧化物能与酸反应生成黄色的铁盐溶液;要探究步骤⑤做过催化剂的Fe2O3其它化学性质,还应补做的实验是用稀盐酸(或稀硫酸)溶解固体,观察是否生成棕黄色溶液;
(2)据二氧化锰的用量和收集等体积氧气所用时间的长短的图象可知:反应中二氧化锰的质量在0.1g~0.7g之间时,用量越大,过氧化氢的分解速率越快,当二氧化锰的用量超过0.7g时,反应速率速率不再随二氧化锰的用量增加而加快。由图可知,Fe2O3的用量对H2O2分解速率影响的规律是:在一定范围内,MnO2的用量越大,H2O2分解速率越快。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:
【题目】有Zn、Cu、Ag、Zn(NO3)2溶液、Cu(NO3)2溶液、AgNO3溶液几种物质。
(1)Zn(NO3)2溶液中的溶质是_____。
(2)上述六种物质之间相互可以发生_____个置换反应。若要验证Zn、Cu、Ag三种金属的金属活泼性强弱,可选择上述物质中的Zn、Ag及_____溶液,也可以选择Cu及_____两种溶液。
(3)向含有AgNO3和Cu(NO3)2两种溶质的溶液中加入一定量的Zn,充分反应后过滤、洗涤,分别得到滤渣和滤液。若向滤渣中加入稀盐酸有气泡产生,则滤液中的溶质是_____;若向滤液中滴加稀盐酸,有白色沉淀生成,则此滤液中含有_____种溶质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组利用下列装置进行气体的制取,请回答:
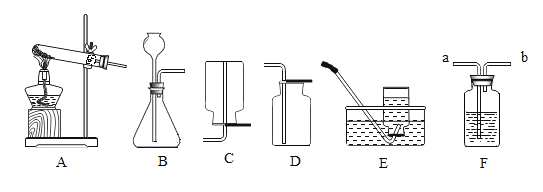
(1)选用A装置制取氧气的化学方程式是____________。
(2)A、E连接制取氧气,收集的氧气不纯的原因是____________(写一点即可)。
(3)若用过氧化氢溶液制取一瓶干燥的氧气,需要用到装置F,则装置F中应加入的物质是_______,气体应从________端通入(填“a”或"b”)。
(4)实验室制取二氧化碳选择的发生装置和收集装置是________(填序号),选择该发生装置的依据是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天然水净化为自来水的主要流程如下:
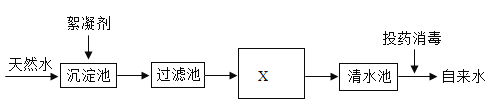
(1)过滤池的作用是除去_______________杂质。
(2)X为活性炭___________池。
(3)如果作为水源的天然水是硬水,向所得的自来水中加入少量肥皂水,振荡,观察到出现较多_________。
(4)目前不少自来水用液氯作为消毒剂,液氯注入水后发生反应的示意图如下:

该反应前后不变的粒子是__________(填化学符号);化合价发生改变的元素有_________种(填“1”、“2”或“3”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是学习化学的基础,请分别回答下列问题.
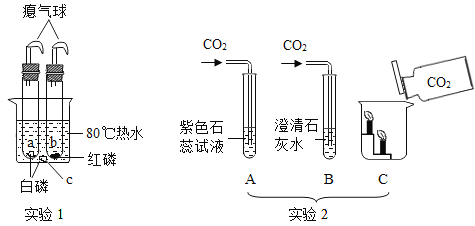
(1)通过实验1可以探究燃烧的条件.烧杯中有热水,a、b、c三个位置分别放有药品,可以观察到a处的现象是:白磷燃烧,产生大量__,放出热量.实验1中气球的作用是__.__与__(填编号)对比,说明燃烧需要的条件是可燃物需要与氧气接触;__与__(填编号)对比,说明燃烧的条件是温度要达到可燃物的着火点.
(2)实验2包括A、B、C三个小实验.
A:往紫色石蕊试液中通入干燥的CO2,可以观察到的现象是__.
B:往澄清石灰水中通入干燥的CO2,可以观察到的现象是__,该反应的化学方程式为__.
C:把二氧化碳气体慢慢倒入放着燃着的蜡烛的烧杯中,低的蜡烛先熄灭,高的蜡烛后熄灭,说明二氧化碳具有__、不能燃烧和不支持燃烧的性质.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质王国举行一场足球游戏。游戏规则是:“队员”之间能相互反应可有效传球;“守门员”与“队员”之间能反应,射门成功。“足球队”由铁、稀盐酸、氢氧化钙、硫酸铜四名“队员”组成,游戏中,由“A队员”硫酸铜发球,传球路线和射门如图所示,“守门员”是个灭火“能手”。
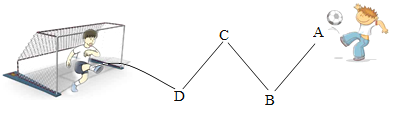
(1)“守门员”是__(填化学式,下同);
(2)若“D队员”成功射门,则“B队员”是__;写出传球过程中任一反应的化学方程式________,反应的基本类型为__反应。
(3)A队员也可传球给__(选填“C”或“D”)“队员”,快速射门。
(4)下列“队员”可替补“守门员”,使“D队员”能成功射门的是___(填序号)。
①SO2 ②Fe2O3 ③Na2CO3 ④NaOH。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小政同学在复习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其它物质间相互反应的关系如图(图中“﹣﹣”表示相连的两种物质能发生反应)。

(1)若X是与其它三种不同类别的化合物,则X可以是_____。
(2)根据图所示的物质间关系,写出其中两个化学方程式:
①_____; ②_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)2015年5月12日,海西高速公路网的重要组成部分:福建省最长跨海大桥——泉州湾大桥正式通车。大桥的建设及通行涉及到许多的化学知识。

(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,钢属于 (选填“金属”或 “无机非金属”)材料。
(2)工人给大桥钢铁器件喷上油漆,目的是为了防止铁与 和 发生反应而生锈。
(3)大桥施工过程中用乙炔(C2H2)燃烧的火焰来焊接金属,乙炔在空气中完全燃烧生成二氧化碳和水,该反应的化学方程式为 ;乙炔燃烧时将 能转化为热能和光能。
(4)大桥的建成,把隔海相望的泉州环湾城市群连成一片,驱车跨跃泉州湾只需8分钟,有利于节约化石燃料的使用,从而有利于减缓 (填序号)。
①雾霾天气 ②温室效应 ③赤潮的形成 ④酸雨的形成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丙醇在很多情况下可代替沸点较低的乙醇用作有机溶剂,如图是丙醇的分子结构图,其化学式为C3H7OH。下列有关丙醇的说法正确的是:
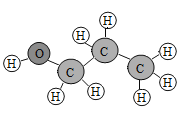
A.丙醇是由碳、氢、氧三种原子构成的
B.丙醇中碳、氢、氧的质量比为3∶8∶1
C.丙醇中氢元素的质量分数最大
D.丙醇不属于氧化物,但属于有机化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com