
【题目】乙醇,俗称酒精,在人们的生活中扮演着重要的角色。
(1)我国传统酿酒工艺中的重要操作是蒸馏。从微粒角度分析,将液态酒精变成气态时,变化的是分子的_____。
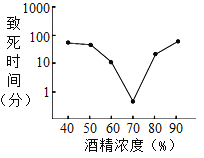
(2)75%的酒精溶液可用于消毒,其溶剂为_____。如图为常温下,某科研小组测量不同浓度的酒精溶液杀灭金黄色葡萄球菌所需时间的实验结果。分析图得到的结论是_____。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】请沿用科学家认识事物的方式认识“空气”。
(1)从分类角度:空气属于 (填“混合物”或“纯净物”)。
(2)从微观角度:用“![]() ”表示氮原子,“
”表示氮原子,“![]() ”表示氧原子。
”表示氧原子。
①用“![]() ”可表示的微粒是 (填名称)。
”可表示的微粒是 (填名称)。
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图3可表示空气微观模型的是 (填标号)。

(3)从变化角度:
已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是 。将该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是 。
(4)从应用角度:利用空气制取氮肥的流程如图4所示。

①Ⅰ中参加反应的单质甲为 。
②Ⅱ中反应的化学方程式为 。
③物质所含元素化合价发生变化的反应称为氧化还原反应。反应Ⅲ (填“属于”或“不属于”)氧化还原反应。
(5)从环保角度:下列保护空气措施合理的是 (填标号)。
A.工厂通过加高烟囱直接排放废气 B.推广使用乙醇汽油代替普通汽油
C.提倡步行、骑自行车等“低碳”出行方式
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】每年因金属腐蚀造成的经济损失远超所有自然灾害造成的损失总和。给金属“穿防 护服”是一种常见的防腐手段。
Ⅰ.铁质零部件表面发蓝
工业上常将铁质零件进行发蓝处理,使其表面形成一层致密的蓝黑色氧化膜。过程如下:
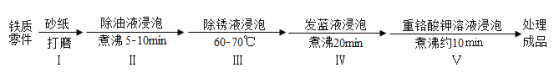
(1)步骤Ⅰ“砂纸打磨”过程发生的是_____(填“物理变化”或“化学变化”)。
(2)步骤Ⅱ~Ⅴ都在加热条件下进行,加热的作用是___;步骤Ⅲ处理时,用除锈液 (稀硫酸)浸泡时间不宜太长,原因是_____(用化学方程式表示)。
(3)为检验步骤Ⅳ处理后的质量是否合格,常往成品表面滴上 5%的硫酸铜溶液,若表面未形成致密的氧化膜,一段时间后将观察到的现象为______。
Ⅱ.铜质数据线表面镀锡
(4)选用铜作导线的主要原因是______,然而铜生锈将增加电阻,缩短使用寿命;锡在空气中表面会形成致密的二氧化锡(SnO2),二氧化锡能与盐酸发生反应,反应的化学方程式为_______。
(5)金属锡和铝的部分信息。
价格 | 熔点 | 氧化物熔点 | |
锡 | 133000 元/吨 | 232℃ | 1127℃ |
铝 | 12770 元/吨 | 660℃ | 2054℃ |
由表中信息可知,锡的价格远高于铝,选择在铜表面镀锡而非铝,主要因为锡的熔点更低,对于数据线的生产来说,熔点低的优势在于_______。
(6)剪取某废旧数据线,准确称取一定量样品放入足量盐酸中浸泡,观察到____,溶液仍为无色。完全反应后将剩余固体取出,洗净、____、称量。三次实验结果记录如下,导线中金属铜的质量分数为_________(计算结果保留到百分号内小数点后一 位)。
实 验 | 1 | 2 | 3 |
样品质量/g | 0.5529 | 0.5659 | 0.5860 |
剩余固体质量/g | 0.5291 | 0.5419 | 0.5604 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体的溶解度曲线如下图所示。下列说法中,不正确的是
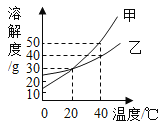
A.20℃时,甲、乙两种物质的溶解度相等
B.40℃时,甲的饱和溶液中溶质和溶剂的质量比为1:2
C.升高温度可以将甲、乙的饱和溶液转化为不饱和溶液
D.40℃时,向100g水中加入50g乙,所得溶液溶质质量分数为33.3%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文
某北方地区用萝卜叶酱菜制作流程如下:
原料→挑选→切碎→清洗→沥水→腌渍Ⅰ→腌渍Ⅱ→脱盐→酱制→调味→真空包装→杀菌→冷却→成品。
萝卜叶的腌制过程属微生物的发酵过程,蛋白质在微生物蛋白酶和肽酶作用下,会产生一些氨基酸、肽类等风味物质。腌制过程由于微生物的生长代谢消耗了萝卜叶的蛋白质,从而使蛋白质含量下降。酱制、调味后的样品中蛋白质含量增高,其蛋白含量主要来源于酱制和调味过程加入的酱油及味精。酱油中含有蛋白质,味精属谷氨酸钠盐,使成品萝卜叶酱菜中的蛋白质增高。
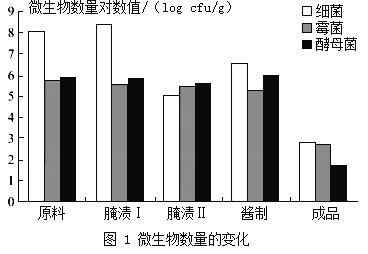
选取原料、腌渍Ⅰ、腌渍Ⅱ、酱制和成品五个工序的样品,进行细菌、霉菌和酵母菌的测定,其实验结果如图1所示。腌渍Ⅰ阶段主要以乳酸菌发酵为主导,乳酸菌正处于对数期,迅速增长;腌渍Ⅱ阶段主要是腌制过程中的盐分产生的高渗透压及发酵所产生乳酸等物质抑制部分微生物的生长。
酱菜中含有乳酸菌,能够调节肠胃功能,有助于儿童、中老年人消化。另外,酱腌中蛋白质、维生素C含量普遍较高,其中含有的乳酸钙还能促进儿童的成长发育。一些蔬菜本来含钙、铁的量较高,经过腌制后得到浓缩,钙、铁含量更为丰富。因此,适量食用酱菜对人体健康有益。
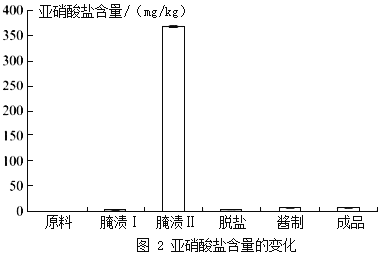
但是,酱菜制作过程中也会产生较高的亚硝酸盐。亚硝酸盐与胃酸反应,产生亚硝酸(HNO2)和氯化物。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。酱菜制作过程中亚硝酸盐含量变化如图2所示。
依据文章内容回答下列问题。
(1)钙、铁含量较高的蔬菜,经过腌制成为酱菜,钙、铁含量会更为丰富,这里的“钙、铁”是指_____(填“分子”“原子”“元素”)。
(2)酱制、调味后的酱菜样品中蛋白质含量增高,主要来源是_____。
(3)亚硝酸钠(NaNO2)是常见的亚硝酸盐,亚硝酸钠与胃酸反应的化学方程式为_____。
(4)下列说法正确的是_____。
A 萝卜叶的发酵过程属于物理变化
B 酱菜制作过程中,亚硝酸盐含量在发酵后期达到一个峰值后又迅速下降
C 酱菜制作过程中,霉菌和酵母菌的数量整体呈下降的趋势,细菌数量整体呈上升趋势
D 霉菌和酵母菌在整个腌制、酱制过程中波动较小
(5)有人说儿童不适合吃酱菜,请写一写你的观点,并说明理由:_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现代工业常以氯化钠、二氧化碳、氨气(NH3)为原料制备碳酸钠,主要流程如下:
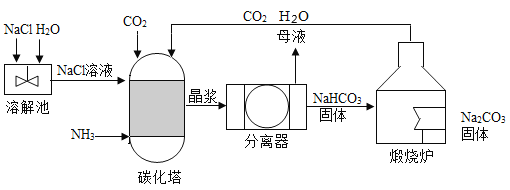
注:晶浆中主要含有NaHCO3固体、NaCl溶液、NH4Cl溶液;母液是含有NaCl、NH4Cl的溶液。
(1)溶解池中,NaCl溶于水的过程中需不断搅拌,其目的是_____。
(2)煅烧炉中发生反应的基本反应类型为_____。
(3)整个流程中,可以循环使用的物质有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾和氯化钠的溶解度曲线如图所示。
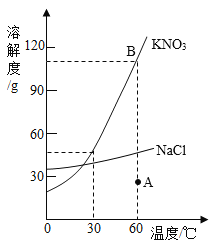
(1) 30℃时,氯化钠的溶解度___________(选填“大于”“等于”或“小于”)硝酸钾的溶解度。
(2) 60℃时,120g硝酸钾与100g水充分混合可以形成___________ (选填“饱和”或“不饱和”)溶液。
(3)硝酸钾中混有少量氯化钠,则提纯硝酸钾可采用的方法是________________。
(4)将A点的硝酸钾溶液转化为B点的该溶质的溶液,可以采取的方法是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水在生产、生活中有广泛的应用。
(1)水是常用的溶剂。农业上用10%~20%的NaCl溶液来选种。现要配制16%的NaCl溶液50kg,需要水的质量是_____。
(2)加湿器可以增加室内的湿度。电加热式加湿器是通过电加热,使水沸腾变为水蒸汽。在此过程中,发生变化的是_____(填字母序号)。

A 水分子种类B 水分子间间隔C 水分子运动速率
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图所示,某河旁甲、乙、丙、丁四座化工厂排放的工业废水中分别含有碳酸钠、氯化铜、氢氧化钠、盐酸中的一种.某同学对①、②、③、④处水质监测时记录了以下现象.根据现象推断,甲、乙、丙、丁四座化工厂排放工业废水的成分,错误的是( )
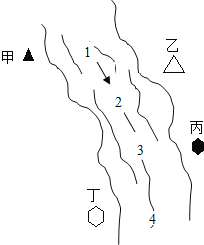
① | ② | ③ | ④ | |
记录现象 | 无色溶液 | 蓝色浑浊 | 浑浊消失 | 产生气泡 |
A.甲:碳酸钠 B.乙:氯化铜 C.丙:盐酸 D.丁:碳酸钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com