
【题目】下列实验方案不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 配制50 g 6%的氯化钠溶液 | 称取3 g氯化钠固体溶于47 mL水中 |
B | 鉴别硬水和软水 | 加入肥皂水,振荡,观察现象 |
C | 除去铜粉中少量的木炭 | 将混合物在空气中灼烧 |
D | 除去NaOH溶液中少量的Na2CO3 | 加入适量的Ca(OH)2溶液,充分反应后过滤 |
A.AB.BC.CD.D
【答案】C
【解析】
A、配制50 g 6%的氯化钠溶液,需要氯化钠固体质量=50g×6%=3g,需要水的质量为50g-3g=47g,需要水的体积=![]() 47mL;故选项正确,但不符合题意;
47mL;故选项正确,但不符合题意;
B、鉴别硬水和软水分别加入肥皂水,振荡,浮渣多,泡沫少的是硬水,反之是软水;故选项正确,但不符合题意;
C、除去铜粉中少量的木炭,将混合物在空气中灼烧,木炭燃烧产生二氧化碳气体,但铜在空气中灼烧产生氧化铜,有效成分发生改变;故选项错误,但符合题意;
D、除去氢氧化钠溶液中少量的碳酸钠,加入适量的氢氧化钙溶液,氢氧化钙能与碳酸钠反应产生碳酸钙沉淀和氢氧化钠,充分反应后过滤后,滤液中只含有氢氧化钠;故选项正确,但不符合题意;
故选:C。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】(1)三大化石燃料是指煤、____________和天然气,它们都是不可再生能源。天然气的主要成分是甲烷,其燃烧的化学方程式为_______________.
(2)可燃物燃烧的条件之一是____________________(任写一条即可,下一空同样),灭火的原理就是任意破坏一个燃烧的条件,所以生活中扑灭油锅着火的方法有______________________。
(3)水蒸气与炽热的炭反应可生成一氧化碳和氢气,其反应的化学方程式为:________,基本反应类型是________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水晾晒可得粗盐,粗盐中除NaCl 外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。为了得到纯净的氯化钠,实验操作流程如下:
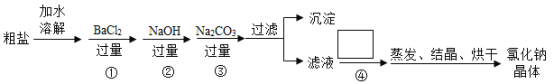
(1)操作②中,选择除杂试剂时,不能用KOH代替NaOH的理由是什么?__________
(2)过滤后得到的沉淀的成分有哪些?__________
(3)操作④方框内加入的试剂和目的是什么?__________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t℃时,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是
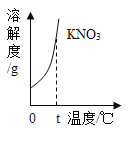
A.t℃时,KNO3 的溶解度为30g
B.乙溶液的质量分数为30%
C.适当降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下图装置测定空气中氧气含量,实验步骤如下(装置气密性良好,部分操作已略去,因导管产生的误差忽略不计):
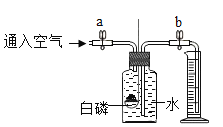
(1)打开止水夹a、b,向集气瓶中缓慢通入一定量的空气,通入集气瓶内空气的量应该满足的条件是____,测得进入量筒中水的体积为V1。
(2)关闭止水夹a、b,用强光照射引燃白磷,发生反应的化学方程式是_______。
(3)白磷熄灭并冷却至室温,打开b,看到的现象是________,测得量筒内水的体积是V2。根据实验记录V1、V2,得出空气中氧气的体积分数的计算式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,水与人类的生活息息相关。
(1)为了人类的生存和发展,人类必须保护水资源。下列做法不利于保护水资源的是______(填字母)。
A 生活污水直接排放
B 提倡使用节水器具
C 工业上的冷却水重复利用
D 园林浇灌采用滴灌、喷灌的方式
(2)硬水会给生产和生活带来许多不便,生活中常用_____的方法来降低水的硬度。家用净水器在净化水的过程中,常用____吸附水中的色素和异味。
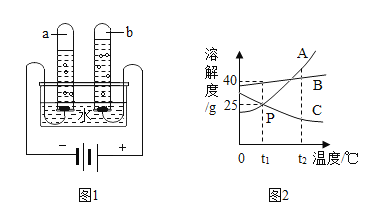
(3)图1是电解水的实验装置图,实验时往水中加入少量氢氧化钠的目的是_______。a试管内产生的气体是____(填化学式)。
(4)高铁酸钠(Na2FeO4)可用于自来水的净化消毒,其原理为![]() ,反应物R的化学式为_______。
,反应物R的化学式为_______。
(5)图2为A.B.C三种固体物质的溶解度曲线图。将t1°C时A.B.C三种物质的饱和溶液升温到t2°C,所得溶液中溶质的质量分数最大的是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(1)20℃时,NaCl的溶解度是__g.
(2)根据表内数据可知,KNO3和NaCl溶解度相等的温度取值范围是__.
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:
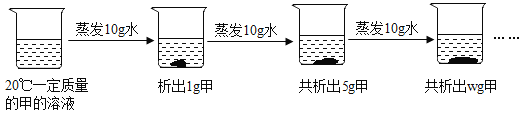
①蒸发前原溶液是__(填“饱和”和“不饱和”)溶液.
②w的数值是__.
③依据上述实验,你认为甲的溶解度随温度变化的趋势是__(填编号).
A随温度升高而增大 B随温度升高而减小 C无法判断
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是利用石灰石,食盐水,氨气进行工业生产纯碱的流程示意图(部分条件及物质未标出)。
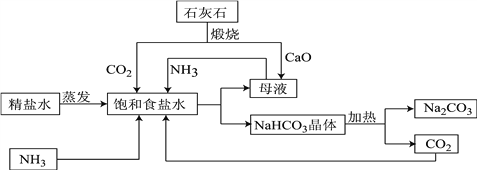
(1)粗盐精炼成精盐的过程中,要经过溶解、______、蒸发等操作,其中都必需用到的一种玻璃仪器为_______,
(2)图中母液含有一定量的NaHCO3,该溶液为该温度下NaHCO3的_________(填“饱和”或“不饱和”)溶液;
(3)流程中要通入CO2和NH3,应先通入NH3,理由是______________________________;精盐水经过氨化和二氧化碳酸化后生成碳酸氢钠和一种氮肥,请写出相应的化学方程式:_____。
(4)整个生产过程中可循环利用的物质为__________________(填化学式)。
(5)所得产品纯碱中含有少量碳酸氢钠,如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为(加热前固体的质量为m1,加热后为m2):_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
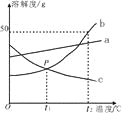
(1)P点表示在t1℃两物质的溶解度关系为b c(填“>”、“<”或“=”)。
(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为 。
(3)t2℃时,50 g b物质加入到50 g水中充分溶解后,所得溶液的质量为 。
(4)b中含有少量的a,若要提纯b,可采用 结晶的方法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com