
����Ŀ����ͼ�Ǽס������ֹ������ʣ������ᾧˮ�����ܽ������ͼ�������������Ϣ�ش����⣺ 
��1��t2��ʱ����30�˹���׳���ܽ���100��ˮ�У����γ���Һ���������ˣ�
��2��t1��ʱ����30�˹����ҳ���ܽ���100��ˮ�У����γ���Һ���������ܼ����������� ��
��3����t2��ʱ�ҵIJ�������Һ���µ�t1��ʱǡ�ôﵽ����״̬�����ʵ�����������������䡱�������С������
��4����t2��ʱ�������ļס��ұ�����Һ���µ�t1�棬�������������϶��������ס����ҡ���
���𰸡�
��1��130
��2��1��5
��3������
��4����
���������⣺��1��t2��ʱ����30�˹���׳���ܽ���100��ˮ�У����γ���Һ������=30g+100g=130g�����Դ��ǣ�130����2��t1��ʱ����30�˹����ҳ���ܽ���100��ˮ�У����γ���Һ���������ܼ���������=20g��100g=1��5�����Դ��ǣ�1��5����3����t2��ʱ�ҵIJ�������Һ���µ�t1��ʱǡ�ôﵽ����״̬�����ʵ����������Dz��䣬��Ϊ���º�û�й���������ˮҲû�м��٣����Դ��ǣ����䣻��4����t2��ʱ�������ļס��ұ�����Һ���µ�t1�棬�������������϶���Ǽף���Ϊ���ܽ�����¶ȵ����߱仯���Ҵ����Դ��ǣ��ף�
�����㾫����������Ŀ����֪���������ù����ܽ�����������ú����ʵ������������ܽ��Ժ��ܽ�ȵĹ�ϵ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ����1������ָ���¶�ʱ���ʵ��ܽ�ȣ��������ܽ���ж��ܽ��ԣ�2���Ƚ���ͬ�¶�ʱ����һ���¶ȷ�Χ�ڣ���ͬ�����ܽ�ȵĴ�С��3���ȽϺ�ȷ�����ʵ��ܽ�����¶�Ӱ��ij̶ȣ����ݴ�ȷ�����ʽᾧ����������ᴿ�ķ�����4��ȷ����Һ��״̬�������벻���ͣ��������������� =��������/��Һ����*100% ���ܽ��=��������/�ܼ�����*100g (����ѡȡ������Һ������Һ����=��������(��)+�ܼ�����(��) �����ڱ�����Һ,��Һ��������w = S/(S+100)�������ܽ��S = 100/(1/w-1)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ϡ����������Ϊ98�����ܶ�Ϊ1.84g/ mL����Ũ���ᣬ����500 mL��������Ϊ20����ϡ���ᣨ�ܶ�Ϊ1.14g/ mL����ϡ��ʱ���õ�ˮ�����ԼΪ �� ��
A��436.8 mL B��453.7mL C��456.0 mL D��458.3mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧΪ�˲ⶨͭþ�Ͻ���Ʒ��ͭ��������������100gϡ�����2�μ��뵽ʢ��5g����Ʒ���ձ��У��������������������˵���д�����ǣ� ��
���� | ʵ��ǰ | ��1�� | ��2�� |
����ϡ���������/g | 0 | 50 | 50 |
ʣ����������/g | 5 | 3 | 2 |
A.��1�μ���ϡ�����ʣ������л���þ
B.��2���������ϡ����δ��Ӧ��
C.ÿ50gϡ�����1gþǡ����ȫ��Ӧ
D.�Ͻ���Ʒ��ͭ����������Ϊ40%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����۩���۩����š����ر����ǻ�ѧ���صı�ʾ���ʼ���仯�ķ���������ͼʾ����������⣺ 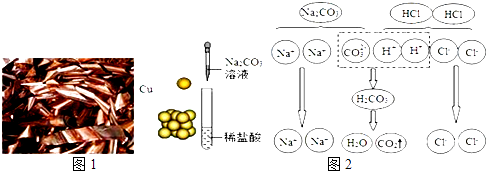
��1��ͼ1�У���Cu����ʾ������Ϣ�����ʾͭԪ�ء�����ͭ���ʣ����ܱ�ʾ��
��2�������ĽǶ�˵��ͼ2��Ӧ��ʵ������
��3����ͼ3��ʾ����һ�������£�A��B��Ӧ����C��D���÷�Ӧ�Ļ�ѧ����ʽΪ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ɹ�������Ļ�ѧʽ(HO)��õ���Ϣ�У���ȷ����
A. ����������������Ӻ������ӹ��ɵ�
B. ������������2����Ԫ�غ�2����Ԫ����ɵ�
C. ÿ��������������2����ԭ�Ӻ�2����ԭ�ӹ��ɵ�
D. ������������������������ɵĻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⶨ������һЩ���ʵ�pH�������ͼ������˵��������ǣ� �� 
A.ʳ��������ȥ��ˮ��
B.���������к����������ƣ�����ϴ¯���ϵ�����
C.θ�������˲��˶������
D.����֭ˮ��ʹ��ɫʯ����Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ���߱������Ļ�ѧʵ�鼼����ѧϰ��ѧ�ͽ��л�ѧ̽����Ļ����ͱ�֤��������ͼ�ش����⣺ 
��1��ͼ����c������������ ��
��2����������a��d����ʱ��ʹa�����ײ���d�Ĵ�ʩ����
��3��ͼ����ʾʵ���еĴ����� �� ��ȡ�Ȼ��Ƶ�ʵ������Ϊg��
��4������װ�ñ���O2���õķ�Ӧ��Ϊ�������ƣ����÷�Ӧ�Ļ�ѧ����ʽΪ ��
��5��ͼ�������巢��װ�û�����һ���IJ��㣬Ҫʹװ���ܿ��Ʒ�Ӧ���ʣ���ѡ��ͼ���е���ѡ����ĸ��ţ�����ͼ���еij���©����
��6����ͼ2��ij��ʵ���װ��ͼ����ѹ��ͷ�ιܺ�a������������b����Ӧ�Ļ�ѧ����ʽ������װ��β��������ʵ��˵��CO2���е������������һ�����ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ1��ʾ�����������ġ�С�����ǡ�������Χ��һȦ����Ϸ���ס��ҡ�����������ֱ���ϡ���ᡢ����ͭ������������Һ������̿��������̼�е�һ�֣���֪��pHС��7�� 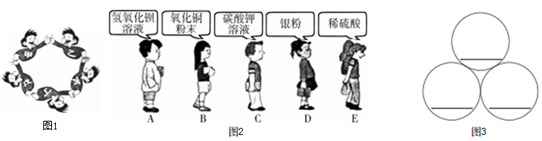
��1��������Ϸ�����ҵĻ�ѧʽ�� ��
��2��д�����붡��Ӧ�Ļ�ѧ����ʽ�� �� �������Ӧ��������Ӧ��
��3��������Ϸ����ͼ2��ѡ���������ʣ�ʹͼ3��λ��С���ѡ��ܹ�����Ϸ������ȥ�����������ʵı������ͼ3�����ϣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С�����÷�����Һ�Ʊ�K2SO4���о�CaSO42H2O���ȷֽ�IJ�� ��һ��K2SO4���Ʊ�
��1����CaCO3�гɷ�ĩ��Ŀ����
��2�����������п�ѭ��ʹ�õ�������CO2������д��ѧʽ����
��3����Ӧ����������ʵ��ܽ�����±�������Ϊ��Ӧ���ڳ�������ʵ�ֵ�ԭ����
���� | KCl | K2SO4 | NH4Cl | M |
�ܽ��/g��25�棩 | 34.0 | 11.1 | 37.2 | 19.5 |
��4������ˮ���ñ���K2SO4��Һϴ�ӷ�Ӧ�����þ����Ŀ������Ϊ����˾����Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ��Һ���ȼ�����ѡ����ţ���ͬ���������ã������ϲ���Һ�еμ� �� �۲������жϣ� a��AgNO3��Һ b��������BaCl2��Һ c��������Ba��NO3��2��Һ
��5���������о�CaSO42H2O���ȷֽ�IJ�� �������õ�CaSO42H2O����CaCO3 �� ���������ȥ���õĻ�ѧ��Ӧ����ʽ ��
��6��Ϊ�˲ⶨCaSO42H2O��CaCO3��������x��y��ʵ��С��������ͼ��ʾ��װ�ã��г�����ʡ�ԣ�����ʵ�飮 
��ʵ��ǰ����Ҫ �� ��װ����Ʒ��װ��A�������� ��
����֪CaSO42H2O��160������CaSO4 �� 1350��ʱCaSO4��ʼ�ֽ⣻CaCO3��900��ʱ�ֽ���ȫ���ֿ���Bװ���¶�900�����ʵ�鲢�ɼ����������ݣ�
a����Ӧǰ����������Ʒ������m1g b����Ӧ�������й��������Ϊm2g
c��װ��Cʵ�������m3g d��װ��Dʵ�������m4g
ijͬѧѡ��b��d��c��d����������x��y��ֵ������װ��E����ʵ��ⶨ��������ƫ����ƫС������Ӱ�족��������Ϊ����ѡ����������ѡ����ţ������������Ҳ�����x��y��ֵ��
��7��CaSO42H2O���Ȼ���ʧȥ�ᾧˮ��ȡ����CaSO42H2O����3.44g�����ڣ�5����ʵ��װ��B�н��м��ȣ��ⶨ�����������¶ȵı仯�����ͼ��ʾ����G�����Ļ�ѧʽ�� �� 
�ڽ�T2��1400���¶ȶμ��ȹ���������������ͨ������KMnO4��Һ�У���Һ��ɫ����H��I�η�����Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com