
【题目】联合国大会宣布2019年是“国际化学元素周期表年”(IYPT2019)。下图中①是钙元素在元素周期表中的信息,A、B、C、D、E是某五种微粒的结构示意图。请回答下列问题:

(1)根据周期表信息,钙元素的相对原子质量为_____;
(2)在A、B、D、E微粒中,属于离子的是_____(填离子符号);化学性质相似的微粒是_____(填字母)。
(3)B微粒对应的元素位于元素周期表中第_____周期;若C微粒表示的是离子,则X为_____;E微粒在化学变化中容易_____电子(填“失去”或“得到”)。
【答案】40.08 Ca2+ A和B 三 8 失去
【解析】
(1)根据周期表信息,钙元素的相对原子质量为40.08;
(2)质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;在A、B、D、E微粒中,D的质子数>核外电子数,为阳离子,质子数是20,为钙离子,符号为:Ca2+;化学性质相似的微粒的是AB,这是因为它们的最外层电子数相等。
(3)B微粒对应的元素是硫,原子核外电子层数是3,位于元素周期表的第三周期;C的质子数是17,为氯元素,氯原子最外层电子数是7,大于4,易得到一个电子成为带一个负电荷的氯离子, 所以若C微粒表示的是离子,则X为8;E微粒最外层电子数为2,小于4,易失去2个电子。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】.某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质。结合装置图,回答下列问题:
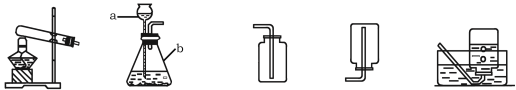
A B C D E
(1)写出图中标号仪器的名称:a ,b 。
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是 (填上图字母),可选用C装置收集氧气,其原因是 。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置
是 (填上图字母)。
(4)该小组设计了如下图所示的实验装置,既可用于制取气体,又可用于探究物质性质。
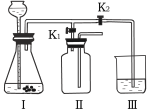
①当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是 (填字母)。
a.大理石与稀盐酸反应制取二氧化碳
b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1时,可以利用工、Ⅲ装置制得二氧化碳并验证其性质。实验室制取二氧化碳的化学方程式是 ;若要证明二氧化碳能与水发生反应,应向烧杯的水中加入 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用“多米诺骨牌效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色。请看图回答问题:
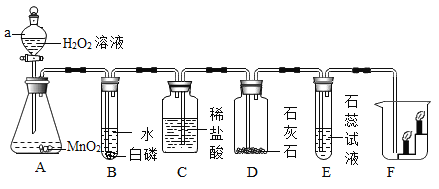
(1)写出指定仪器的名称:a_____。
(2)A中反应的化学方程式_____,A装置的主要优点是_____,MnO2的作用是_____;B中白磷不燃烧,原因是_____。
(3)C中看到的现象是_____。
(4)用化学方程式表示E中颜色变化的原因_____。
(5)F中的现象是_____,体现了该气体的物理性质是_____,化学性质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验。
实验装置 | 实验步骤及现象 |
| 步骤1:检验装置的气密性,气密性良好 步骤2:将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧。 步骤3:向A瓶中加满80°C热水,塞紧瓶塞,白磷不燃烧。 步骤4:打开K1、K2,从A口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2,此时进入量筒B中水的体积为200mL ,观察到A瓶中的白磷燃烧。 |
[实验一](已知:白磷的着火点为40°C,白磷不溶于水也不与水反应)
(1)请写出白磷燃烧的化学方程式_________;
(2)对比步骤3和4的现象可知,可燃物燃烧的条件是________;
(3)待装置冷却--段时间后,打开K2如果观察到________;说明空气中氧气的体积约占1/5。
[实验二]

(1)按图实验(集气瓶底部有少量沙子)可观察到:镁条在二氧化碳气体中剧烈燃烧,集气瓶内部有黑色的碳和白色固体氧化镁生成。请写出反应的方程式________;此反应中碳元素的化合价如何变化:____。
(2) [查阅资料]纳米铁粉在空气中会自燃。
“铁丝在空气中很难燃烧,纳米铁粉却可以在空气中自燃”,你对燃烧的条件有了哪些新的认识:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国著名化学家徐光宪院士说:“化学是不断发明和制造对人类更有用的新物质的科学”。在分子一原子层面上改变原子的排列方式就可以创造新物质。石墨在超高压和高温的条件下某些碳原子(方框中的碳原子a)受到挤压,凸出到层间的空间中,与上一层正六边形的碳原子形成正四面体的排列形式,就得到金刚石(方框中的碳原子a对应的石墨中的碳原子a)。
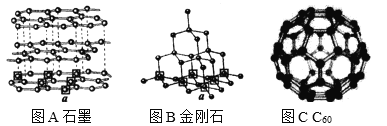
1985年,英国化学家克罗托发现C60,提出C60是由12个正五边形和20个正六边形构成封闭的完美对称的笼状分子,由于C60分子的形状和结构酷似英国式足球,所以又被形象地称为“足球烯”。C60在常温下是紫红色晶体,具有金属光泽。
1991年,日本科学家发现了碳纳米管,它是碳原子以正六边形排列而成的管状结构,直径一般为几纳米到几十纳米。碳纳米管的管状结构决定了它的弹性和弯曲性都比较优异,可制作金属催化剂载体,作为贮氢。材料制作燃料电池等,碳纳米管还可用于纳米机器人、计算机芯片等前沿领域。
2004年,英国科学家成功制得石墨烯,这种碳单质的碳原子是以正六边形紧密排列的单层结构。石墨烯具有很多优异性能:表面积大、透光率高、导电性强、机械性能优异等,使石墨烯在透明电极、太阳能电池、传感器、手机屏幕、电脑触摸屏等方面有着良好的应用前景。科学家在一定条件下可以选取石墨烯片段包裹成足球烯,也可以将片段卷起来得到碳纳米管。
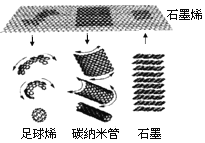
依据文章内容,回答下列问题。
(1)短文中涉及到的碳单质共有_____种。
(2)文中提到“在超高温和高压的条件下,石墨可以转变为金刚石”,这一变化是_____变化。
(3)C60在常温下是_____色晶体,猜想C60的一种化学性质可能是_____(用化学方程式表示),它与金刚石性质上存在明显差异,可能的原因是_____。
(4)碳纳米管机械加工:性能优异,弹性较好,易于弯曲,这些性质都源于它是_____结构。
(5)石墨烯具有较高的导电性和透光性,可以用来制作_____。
(6)结合本文,你认为从微观角度创造新物质的可能途径有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下列短文中的材料,回答有关问题:
催化剂
在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂。催化剂在化学反应中所起的作用叫催化作用。活化能可以用于表示一个化学反应发生所需要的最小能量。不同的化学反应所需的活化能差别很大。化学反应速率与其活化能的大小密切相关。活化能越低.反应速率越快。因此,降低活化能会有效地促进反应的进行。催化剂的作用是降低化学反应发生所需要的活化能。一种催化剂并非对所有的化学反应都有催化作用,某些化学反应也并非只有唯一的催化剂。催化剂在各行各业中广泛使用,但催化剂的活性(即催化作用)也并非一成不变,催化剂在使用过程中受种种因素的影响。会急剧地或缓慢地失去活性,称为催化剂中毒。
(1)催化剂能加快化学反应速率的原因是____________________。
(2)请你写出一个需要催化剂参与的化学反应的文字表达式____________________。
(3)在加热氯酸钾时加入少量的高锰酸钾.也能使氯酸钾分解的速率明显加快.高锰酸钾_____________________(填“是”或“不是”)该反应的催化制。
(4)汽车尾气中的一氧化碳在四氧化 三钴纳米棒的催化作用下.低温即能与氧气反应,生成空气中的一种无毒气体,该反应的文字表达式为_____________________。
(5)下列说法中,正确的是____________________。
a 催化制不能改变生成物的质量
b 催化制在化学反应的后质量和性质都不变
c 一个反应只有一种催化剂
d 催化剂中毒后会失去活性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是城市发展的基础资源和经济资源.推进污水深度处理,再生利用是促进城市发展的重要举措。下图是城市污水处理的部分流程:
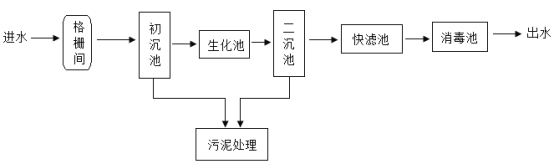
(1)污水通过”格棚”可去除较大的悬浮物,相当于基本实验操作中的________________________。
(2)生化池中通人臭氧(O3)去除水中有机物.从物质分类的角度臭氧属于________________________。(填“单质”或“化合物”)。
(3)污泥处理中部分污泥可腐熟用作肥料,肥料的腐熟属于____________________。(填“物理”或“化学”)变化。
(4)快滤池中活性炭的作用是____________________。
(5)经过以上处理得到的水是硬水,可用______________________(填试剂名称 )进行检验。
(6)我省是水资源严重短缺的省份,请你为节约用水提一条建议_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为一氧化碳还原氧化铁的装置图:
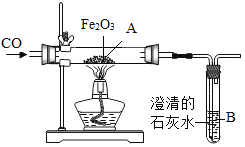
(1)图中A处的实验现象是_________,B处的实验现象是__________
(2)该装置存在的主要问题是,___________,改进的具体措施是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质中含有杂质(括号内为杂质)诸选择一种试剂将其除去。用化学方程式表示除杂时的反应原理。
(1)CO2(CO) _______________________________________;
(2)Cu( Fe) _______________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com