
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 自行车是比较常见的一种交通工具.制作自行车使用最多的金属是铁.铁在空气中往往容易生锈.人们为了防止铁制品生锈.在自行车的不同部位采取不同的防锈措施.例如:支架采取的防锈措施是刷漆,其防锈原理是隔绝氧气和水.
自行车是比较常见的一种交通工具.制作自行车使用最多的金属是铁.铁在空气中往往容易生锈.人们为了防止铁制品生锈.在自行车的不同部位采取不同的防锈措施.例如:支架采取的防锈措施是刷漆,其防锈原理是隔绝氧气和水.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
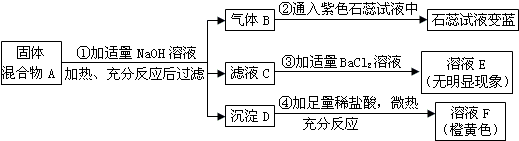
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 224mL H2(标准状况)和0.5molN2 | B. | 5.6L N2(标准状况)和5.6g CO2 | ||
| C. | 11.2L H2O(标准状况)和0.5molBr2 | D. | 10g N2和10g CO |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由2个氢原子和一个氧原子构成 | |
| B. | 矿泉水是纯天然饮品,不含任何化学物质 | |
| C. | 水在化学反应中只充当溶剂不参加反应 | |
| D. | 日常生活中的水大多是混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
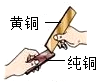 合金是重要的金属材料.
合金是重要的金属材料.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
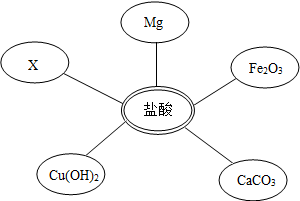
| 方案 | 加入试剂 | 提纯的方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | (选填可行或不可行) |
| 二 | 稍过量的盐酸(或稀HCl或HCl) | 蒸发结晶 | 可行 |
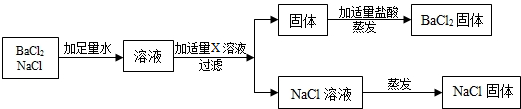
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com