
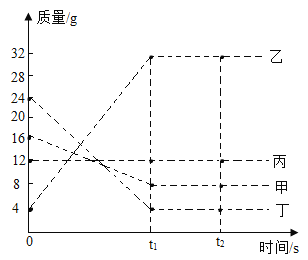
【题目】将一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质得质量如图,下列说法正确的是( )
A.该反应是分解反应
B.丙一定是催化剂
C.反应中甲和丁的质量变化之比为2:5
D.反应中甲和乙的质量变化之比为2:8
【答案】C
【解析】
由图中数据分析可知,反应前后甲的质量减少了16g-8g=8g,故是反应物,参加反应的质量为8g;同理可以确定乙是生成物,生成的质量为32g-4g=28g;丙的质量不变,可能作该反应的催化剂,也可能没有参加反应;丁的质量减少了24g-4g=20g,故是反应物。
A、该反应的反应物为甲和丁,生成物是乙,符合“多变一”的形式,属于化合反应,故选项说法错误;
B、丙的质量不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误;
C、反应中甲和丁的质量变化之比为8g:20g=2:5,故选项说法正确;
D、反应中甲和乙的质量变化之比为8g:28g=2:7,故选项说法错误。
故选C。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:
【题目】由含铜废料制铜的一种方案是:
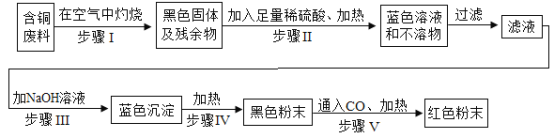
(1)写出下列步骤中的化学方程式:
步骤III:_____。
步骤V:_____。
(2)步骤II后形成的蓝色溶液中的溶质是_____。
(3)上述方案中可能造成空气污染的步骤是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是学生经常使用的交通工具——自行车,请完成下列各题:
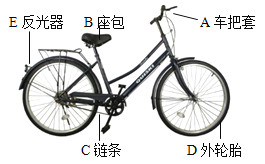
(1)自行车属于合成材料的是________ (选一种物质填序号)。
(2)车轮的钢圈在潮湿的空气中会生锈,生锈实质上是铁与空气中______发生 了一系列复杂的反应而造成的;
(3)利用铁生锈的原理在食品工业上还有应用。“纳米 Fe 粉”,可以用于食品保鲜,称之为“双吸剂”,请用 化学方法检验使用一段时间后的“双吸剂”是否完全失效,写出鉴别过程(填“操作、现象和结论”)_____________________
(4)用打气筒给轮胎打气后,轮胎内空气分子间的距离__________________ (填“大于”、“小于”、或“等于”)空气中分子之间的距离
(5)废旧的自行车不要随意丢弃,应回收利用,这样做的意义是__________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是初中化学常见物质。这些物质之间的转化关系如下图所示。
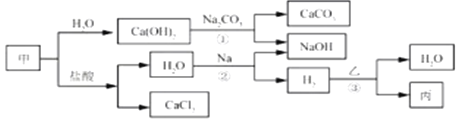
根据以上信息,请回答下列问题。
(1)写出甲的化学式__________。
(2)写出反应①的化学方程式_______________。
(3)写出反应②的化学方程式_______________。该反应属于_____反应(填基本反应类型)。
(4)反应③在一定温度下进行,若乙为Fe2O3,则丙为Fe;若丙为Cu,则乙为_______(填化学式)。
(5)请完成下列表格,证明Fe的金属活动性比Cu的强。
实验方案 | 实验现象 |
将铁片浸入_______(填化学式)溶液中 | 铁片表明析出______固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
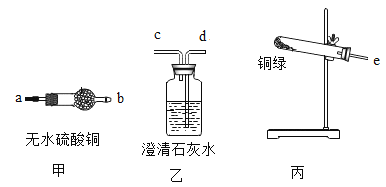
【题目】生活中铜器保存不当易生成铜锈,又称铜绿,其主要成分是碱式碳酸铜(Cu2(OH)2CO3),碱式碳酸铜是一种用途广泛的工业原料。
(1)根据铜绿的化学式推断,铜生锈的条件除了水和氧气外,还需要_________(填化学式).
(2)铜绿不稳定,在加热的条件下生成氧化铜、水和二氧化碳,写出该反应的化学方程式 ____。
(3)用甲、乙、丙三套装置组合后检验铜绿分解的生成物中有水和二氧化碳,仪器的接口顺序为e- ____— __— ___。(资料链接:无水硫酸铜遇水变蓝色)
(4)用辉铜矿(主要成分为Cu2S,还含有少量Fe2O3、SiO2 杂质)制备铜绿流程如下:
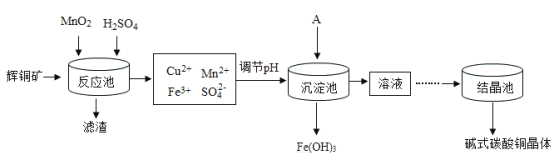
①部分金属阳离子生成氢氧化物沉淀的 pH 范围如下表所示。调节 pH,使Fe3+完全沉淀而Cu2+不沉淀,则 pH 的范围应控制在 _____。
氢氧化物 | Mn(OH)2 | Fe(OH)3 | Cu(OH)2 |
开始沉淀的pH | 8.3 | 2.7 | 4.4 |
完全沉淀的pH | 9.8 | 3.7 | 6.4 |
②(Ⅱ)因为辉铜矿中含有少量Fe2O3,Fe2O3可与稀硫酸反应,故反应池中发生的反应还有:
(Ⅰ)2MnO2+Cu2S+4H2SO4=S+2CuSO4+2MnSO4+4H2O。
_____。
③结晶池中温度须控制在 70℃-80℃,如果出现_________(填写实验现象),说明温度过高。
(5)为了从某铜绿样品中制得金属铜,同时测定碱式碳酸铜的含量。小王同学设计了如下图所示的实验装置,回答下列问题:(资料链接:无水碳酸铜遇水变蓝色)
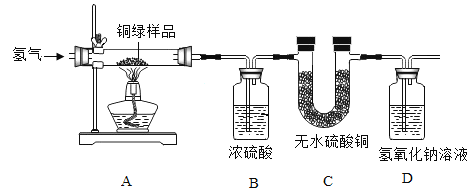
Ⅰ.实验开始时,应先_________再_________(填序号),观察到玻璃管中出现红色固体。
①通入H2 排尽空气 ②点燃酒精灯加热
Ⅱ.碱式碳酸铜晶体化学式:CuCO3·Cu(OH)2·2H2O,相对分子质量为 258。若样品为 20g,反应结束后 B、D 装置分别增重 2.7g 和 2.2g。
计算:①生成二氧化碳 _____g。
②该样品中碱式碳酸铜晶体的纯度。________(写出计算过程,保留到小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某化学反应的微观模拟示意图,下列有关该反应的说法中,不正确的是
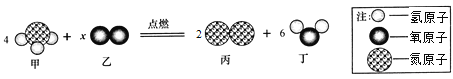
A. 反应前后氮元素的化合价发生改变 B. 该反应属于置换反应
C. 参加反应的甲、乙两物质的质量比为17:24 D. 图示中x的值为2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质a和b在一定条件下反应生成e和d的微观示意图如下:
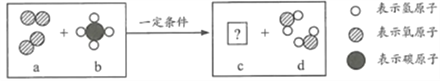
下列说法正确的是
A. 物质c是一氧化碳 B. 该反应不符合质量守恒定律
C. 该反应前后,原子的种类发生改变 D. 该反应前后,分子的个数保持不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验,回答问题。
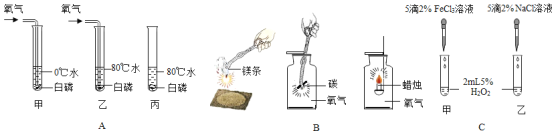
(1)A组实验中,通过对比__ 试管中的现象,可说明燃烧需要温度达到可燃物着火点。
(2)B组实验中,找出三个化学变化的一个共同点___。
(3)C组实验是探究哪种离子能促进H2O2分解的实验,现象是:甲中产生大量气泡,乙中可看到有极少量气泡出现,则加快H2O2分解的离子符号____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A—I是初中化学常见的九种物质。其中B为红色固体,E可作为干燥剂,I在溶液中是一种红褐色沉淀,它们相互转化的关系如图14所示(部分反应物、生成物及反应条件已略去)。

请回答下列问题:
(1)I物质的化学式为_______________。
(2)转化⑥的化学方程式为_______________________________________。
(3)反应④的基本反应类型为______________________。
(4)反应⑤在生产生活中的用途是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com