
【题目】某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从如图中选择装置进行了氧气的制备实验.

(1)写出仪器名称:a ,b .
(2)因为氧气不易溶于水,故可以采用 装置收集(填字母序号,下同);因为氧气的密度比空气大,故可以选用 装置收集.
(3)实验室用二氧化锰与过氧化氢制取氧气,选择的发生装置是 ,若要收集一瓶较纯净的氧气,选择的收集装置是 ,该反应的文字表达式为 .
(4)实验室用高锰酸钾制取氧气可选用的发生装置是 .为了防止高锰酸钾粉末进入导管,该装置还必须作出的一项改正是 ,该反应的文字表达式为 .
(5)该实验中有很多注意事项,如试管口要略向下倾斜;加热之前要先预热…请你另补写一条注意事项: .
(6)李时同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,李明同学发现排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
[提出猜想]猜想Ⅰ:反应生成的MnO2分解放出O2.
猜想Ⅱ:反应生成的K2MnO4分解放出O2.
猜想Ⅲ:反应生成的K2MnO4和MnO2分解都放出O2.
[实验验证]同学们分成两组,分别进行下列实验:
第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜想 错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ是正确的结论.该组同学选择的实验方法是 .
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快,请说明KMnO4在KClO3的分解反应 是否作催化剂,为什么? .
【答案】(1)a试管;b集气瓶;(2)E;C;(3)B;E;过氧化氢![]() 水+氧气;(4)A;在试管口放一团棉花;高锰酸钾
水+氧气;(4)A;在试管口放一团棉花;高锰酸钾![]() 锰酸钾+二氧化锰+氧气;(5)高锰酸钾受热分解制氧气实验完毕,先将导管移出水槽再停止加热;(6)【实验验证】Ⅰ和Ⅲ、把带火星的木条伸入试管中,木条复燃;【拓展延伸】高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
锰酸钾+二氧化锰+氧气;(5)高锰酸钾受热分解制氧气实验完毕,先将导管移出水槽再停止加热;(6)【实验验证】Ⅰ和Ⅲ、把带火星的木条伸入试管中,木条复燃;【拓展延伸】高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.
【解析】(1)根据实验室常用仪器可知:a试管;b集气瓶;
(2)因为氧气不易溶于水,故可以采用排水法收集;因为氧气的密度比空气大,故可以选用向上排空气法收集;
(3)实验室用二氧化锰与过氧化氢制取氧气,属于固液常温型,选择的发生装置是B;要收集一瓶较纯净的氧气,选择的收集装置是B;该反应的文字表达式为:过氧化氢![]() 水+氧气;
水+氧气;
(4)实验室用高锰酸钾制取氧气需加热,可选用的发生装置是A;为了防止高锰酸钾粉末进入导管,该装置还必须作出的一项改正是在试管口放一团棉花,该反应的文字表达式为:高锰酸钾![]() 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气;
(5)高锰酸钾受热分解制氧气实验完毕,先将导管移出水槽再停止加热;
(6)【实验验证】
在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,说明250℃时,二氧化锰不能分解,所以猜想Ⅰ和Ⅲ错误;取高锰酸钾在250℃条件下加热,把带火星的木条伸入试管中,木条复燃,说明猜想Ⅱ正确.故填:Ⅰ和Ⅲ;把带火星的木条伸入试管中,木条复燃.
【拓展延伸】
【实验反思】氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾分解速率大大加快,原因是高锰酸钾加热分解为锰酸钾、二氧化锰、氧气,二氧化锰可以加快氯酸钾的分解,但高锰酸钾不是催化剂.因为高锰酸钾在反应后的质量和性质发生了变化.


科目:初中化学 来源: 题型:
【题目】某校同学选用如图一装置制备二氧化碳气体,请回答下列问题:
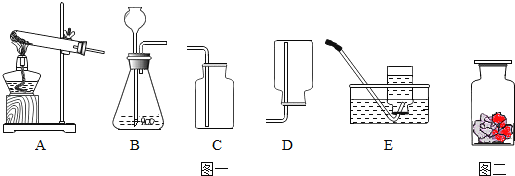
(1)实验室制取二氧化碳的化学方程式是 ;
(2)实验室制取二氧化碳应选用的发生装置是 (填字母序号),收集装置是 (填字母序号)
(3)该校同学收集一瓶二氧化碳气体,然后取来一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入集气瓶中,如图二所示,可观察到的实验现象为 ;
(4)若选用与制取二氧化碳相同的发生装置制备氧气,其反应的化学方程式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习结晶时,同学们对硝酸钾的制备产生浓厚兴趣.
(一)通过查阅资料发现硝酸钾在农业市场用途十分广泛,属于复合肥,工业上常采用硝酸钠与氯化钾反应制得硝酸钾和氯化钠(NaNO3+KCl═KNO3+NaCl).利用硝酸钾和氯化钠在不同温度下的溶解度不同可将其分离,具体流程可以表示为:

(1)溶解时需要不断搅拌,其目的是 .
(2)化学实验室蒸发操作所需的玻璃仪器除玻璃棒外还有 .
(3)过滤1操作时要趁热过滤,目的是 .
(4)滤液1一定是 的饱和溶液.
(5)冷却结晶后获得的硝酸钾晶体中还混有少量的NaCl,为获得更纯净的KNO3,还应进行的操作是洗涤、干燥,洗涤最佳的洗涤剂为 .
A.常温下的蒸馏水 B.饱和的NaCl溶液 C.饱和的KNO3溶液
(6)洗涤后的液体应该 .
A.不经处理直接排放到下水道
B.不经处理直接排放到农田
C.倒入原混合溶液中,节约资源并提高产率
(二)为测定洗涤前的粗产品中硝酸钾的质量分数,设计如下实验:取5g粗产品配成50g溶液,然后加入过量的硝酸银溶液(已知NaCl+AgNO3═AgCl↓+NaNO3,硝酸钾和硝酸银不反应),根据沉淀质量先求出NaCl质量,再确定硝酸钾的质量分数.
(7)硝酸银溶液需要过量的原因是 ,证明硝酸银已过量的方法是:静置后,在上层清液中加入硝酸银溶液,如果观察到 (填有或无)沉淀生成,则已过量.
(8)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液中的硝酸钾的质量分数 (填偏大、偏小或无影响),对所测定的粗产品中硝酸钾的质量分数 .(填偏大、偏小或无影响)
(9)经精确测定AgCl沉淀的质量为1.435g,计算该粗产品中硝酸钾的质量分数 .(请写出计算过程,相关物质的相对分子质量:NaCl 58.5,AgCl 143.5).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源是社会发展的基础,化石燃料是目前人类最重要的能源物质,请回答:
(1)下列燃料中,属于化石燃料的是 .
A汽油 B液化石油气 C柴油 D天然气;
E木炭 F焦炭 G稻草 H氢气
(2)写出天然气充分燃烧的化学方程式 .
(3)运用化学技术与方法科学改造和应用化石燃料是化学科学的使命,在石油加工过程中,依据各成分沸点不同对其进行改造的方法叫做 ,在煤的综合利用中,改变煤的组成和结构的过程属于 变化.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组设计了测定空气中氧气含量的实验,装置如图所示.该实验中,红磷需稍过量,待燃烧停止,装置冷却后,打开止水夹,观察烧杯中的水进入集气瓶,瓶内水面最终接近刻度![]() 处.由此可知,氧气约占空气总体积的
处.由此可知,氧气约占空气总体积的![]() .
.

(1)由本实验还可推知氮气的哪些性质?试写出其中的一条物理性质 和化学性质 .
(2)若将红磷换成炭粉,该实验能否成功? (填“能”或“否”).
(3)若进入瓶中的水的高度略大于![]() 刻度,则可能的原因是什么? .
刻度,则可能的原因是什么? .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用“![]() ”和“
”和“![]() ”分别代表两种不同单质A2和B2的分子,A2和B2发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )

A.该反应为置换反应
B.参加反应的A2与B2分子数之比为3:1
C.物质X含4种元素
D.在反应过程中A2和B2分子保持不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下列物质的字母序号填空:
A镁 B氧气 C氮气 D红磷 E氢氧化钙 F大理石
(1)用于急救病人的是 ;
(2)可制作照明弹的是 ;
(3)充入食品包装袋内的是 ;
(4)可制用作烟幕弹的是 ;
(5)用于实验室制CO2的原料之一是 ;
(6)石灰水的主要成分是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是
A.K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高
B.HCl、NaCl、NaOH三种溶液的pH逐渐变大
C.NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低
D.金、银、铜金属活动性顺序逐渐减弱
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一学期的化学学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请你结合图示回答问题:

(1)写出实验室用高锰酸钾制氧气的化学方程式为 ,实验完毕发现试管已经炸裂,请分析炸裂原因(答一种情况即可): ;
(2)使用装置B时,长颈漏斗需伸入液面下,原因是 ;
(3)实验室制取二氧化碳的反应方程式 ;
(4)实验室制取并收集二氧化碳的装置是 (填序号);
A.AC B.AD C.BE D.BD
(5)氨气是一种密度比空气小且极易溶于水的气体,其实验室制法的原理是NH4Cl(固)+NaOH(固)![]() NaCl+H2O+NH3↑,据此设计出的发生装置是 ,(填装置代号,下同)收集装置是 ;若用F装置进行密封收集氨气,气流应从 端(填“a”或“b”)流入气瓶.
NaCl+H2O+NH3↑,据此设计出的发生装置是 ,(填装置代号,下同)收集装置是 ;若用F装置进行密封收集氨气,气流应从 端(填“a”或“b”)流入气瓶.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com