
【题目】硫酸是一种重要的化工原料,也是实验室中常用的化学试剂,下面是对硫酸 的组成、性质、制取等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的组成
(1)在溶液中解离出的阳离子全部是氢离子的物质统称为酸,检验硫酸中的阴 离子可选择的试剂为_____。
(探究二)硫酸的性质
(2)浓硫酸的特性:用小木棍蘸取少量浓硫酸,放置一会后,可观察到_____。
(3)浓硫酸的稀释:实验室用 98%的浓硫酸配制 100 g 溶质质量分数为 20%的 稀硫酸,应加水的质量为_____g(结果精确到 0.1 g)。
(4)稀硫酸的化学性质:如图为某同学进行的相关实验:
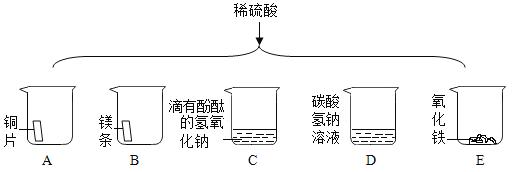
①有气泡产生的是_____(填字母序号)。
②写出烧杯 C 中发生反应的化学方程式_____。
(探究三)硫酸的工业制法
工业上以黄铁矿(主要成分为 FeS2)为原料生产硫酸的工艺流程如图所示:
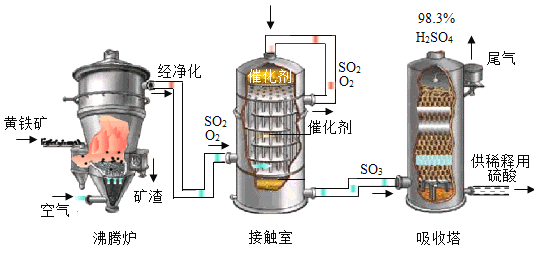
(5)黄铁矿在加入沸腾炉前要进行粉碎,其目的是_____ 。
(6)接触室中发生反应的化学方程式为_____。
(7)依据生产硫酸的工艺流程图,下列说法中正确的是_____ (填字母序号)。
A 吸收塔中得到的产品为混合物
B 催化剂能够加快 SO2 的反应速率和增大 SO3 的产量
C 沸腾炉排出的矿渣可供炼铁
【答案】硝酸钡 小木条变黑 79.6g BD H2SO4+2NaOH=Na2SO4+2H2O 增大反应物的接触面积,加快反应速率 2SO2+O2 2SO3 AC
2SO3 AC
【解析】
[探究一]硫酸的组成
(1)钡离子和硫酸根离子结合生成白色沉淀,通常采用钡离子来检验硫酸根离子,因此检验硫酸中的阴离子可选择的试剂为硝酸钡。故填:硝酸钡。
[探究二]硫酸的性质
(2)浓硫酸具有脱水性,用小木棍蘸取少量浓硫酸,放置一会后,可观察到小木条脱水后变成黑色的碳;故填:小木条变黑。
(3)设稀释前浓硫酸的质量为x。根据稀释前后的溶质质量不变可得:![]() ;解得x
;解得x![]() 20.4g;加水的质量为:100g-20.4g=79.6g。故填:79.6g。
20.4g;加水的质量为:100g-20.4g=79.6g。故填:79.6g。
(4)①烧杯A实验中铜不与稀硫酸反应,无现象;
烧杯B实验中镁和稀硫酸反应生成硫酸镁和氢气,有气泡产生;
烧杯C实验中氢氧化钠和稀硫酸反应生成硫酸钠和水,红色变成无色,无气泡生成;
烧杯D实验中碳酸钠溶液与稀硫酸反应生成硫酸钠、水和二氧化碳气体,有气泡产生;
烧杯E实验中氧化铁与稀硫酸反应生成硫酸铁和水,实验现象是红色固体溶解,溶液有无色变为黄色;
有气泡产生的实验是BD。故填:BD。
②烧杯C中氢氧化钠和稀硫酸反应生成硫酸钠和水,其反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O。故填:H2SO4+2NaOH=Na2SO4+2H2O。
[探究三]硫酸的工业制法
(5)为了使反应物充分接触,反应更快更彻底,节约时间,应将黄铁矿在加入沸腾炉前要进行粉碎,因此粉碎目的是增大反应物的接触面积,加快反应速率。故填:增大反应物的接触面积,加快反应速率。
(6)接触室中通入的是二氧化硫和氧气,在催化剂的作用下反应生成三氧化硫,其反应的化学方程式为:2SO2+O2 2SO3。故填:2SO2+O2
2SO3。故填:2SO2+O2 2SO3。
2SO3。
(7)A、吸收塔中得到的产品是浓硫酸溶液,溶液为混合物,选项说法正确;
B、催化剂能够加快SO2的反应速率,但是不能增大SO3的产量;选项说法错误;
C、沸腾炉排出的矿渣中含有大量的铁元素,可作为炼铁的原材料,选项说法正确。
故填:AC。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:初中化学 来源: 题型:
【题目】由磷元素构成的物质有多种。现有6种含磷元素的物质:H3PO4、H4P2O6、H3PO3、H3PO2、P、PH3。回答下列问题:
(1)从物质分类的角度看,P属于(_____)
A 单质 B 化合物 C 金属 D 非金属
(2)上述6种物质中磷元素的化合价为+3价的是____(填化学式)。
(3)红磷在空气中燃烧生成P2O5的化学方程式为_____。
(4)已知P2O5能与热水反应,得到磷酸 (H3PO4),请写出该反应的化学方程式____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器内,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法错误的是
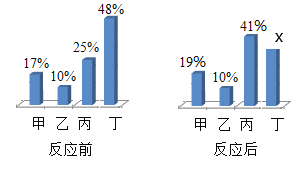
A.乙可能是该反应的催化剂
B.x=30%, 该反应符合质量守恒定律
C.生成的甲,丙两物质的质量比为19: 41
D.参加反应的丁的质量等于生成的甲和丙的质量之和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据原子结构示意图和微观示意图填空.
(1)如图A、B是两种微粒的结构示意图,回答下列问题:
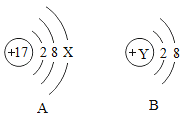
①若A表示某元素的原子,则X=_____;
②若B是某阴离子的结构示意图,则Y的数值可能是下列中的_____(填字母序号).
a 11 b 10 c 9 d 8
(2)在一定条件下,A、B能发生化学反应生成C和D,其微观示意图如图:

若D为空气中体积分数最大的气体,则该反应中生成的C和D的质量比为_____.
(3)C60的发现使人类了解到一个全新的碳世界.根据图,回答下列问题:

①C60属于_____(选填“单质”或“化合物”);
②C60这种物质是由_____(选填“分子”或“原子”)构成;
③C60与金刚石、石墨具有相似的_____(选填“化学”或“物理”)性质.
④足球可由橡胶制成.橡胶属于_____(选填“无机”或“合成”)材料.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应变化关系的是( )
A.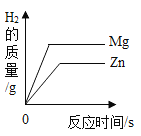 向足量的锌、镁中分别加入等质量、等浓度的稀盐酸
向足量的锌、镁中分别加入等质量、等浓度的稀盐酸
B.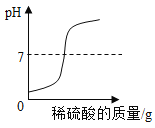 向一定量的氢氧化钠溶液中滳加稀硫酸
向一定量的氢氧化钠溶液中滳加稀硫酸
C.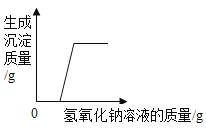 向一定量混有少量盐酸的氯化镁溶液中加入足量氢氧化钠溶液
向一定量混有少量盐酸的氯化镁溶液中加入足量氢氧化钠溶液
D.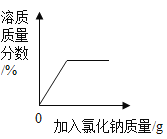 向一定溶质质量分数的不饱和氯化钠溶液中加入氯化钠固体
向一定溶质质量分数的不饱和氯化钠溶液中加入氯化钠固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是利用石灰石,食盐水,氨气进行工业生产纯碱的流程示意图(部分条件及物质未标出)。
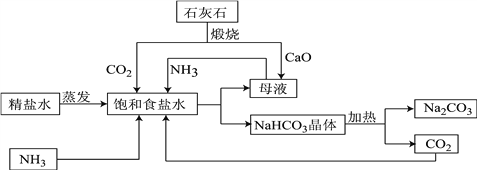
(1)粗盐精炼成精盐的过程中,要经过溶解、______、蒸发等操作,其中都必需用到的一种玻璃仪器为_______,
(2)图中母液含有一定量的NaHCO3,该溶液为该温度下NaHCO3的_________(填“饱和”或“不饱和”)溶液;
(3)流程中要通入CO2和NH3,应先通入NH3,理由是______________________________;精盐水经过氨化和二氧化碳酸化后生成碳酸氢钠和一种氮肥,请写出相应的化学方程式:_____。
(4)整个生产过程中可循环利用的物质为__________________(填化学式)。
(5)所得产品纯碱中含有少量碳酸氢钠,如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为(加热前固体的质量为m1,加热后为m2):_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据有关资料介绍:将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某科学课外小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示.请你与小组同学共同完成以下探究:
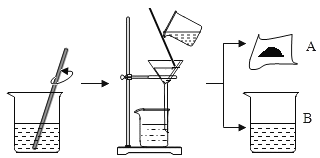
(提出问题1)固体A中的成分是什么?
(猜想与假设)甲同学:只有CaCO3;乙同学:CaCO3、Ca(OH)2
(实验与探究)甲、乙同学为了验证各自的猜想,分别进行了实验:
实验内容 | 实验现象 | 实验结论 |
甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 自己的猜 想正确 |
乙同学:取少量固体于试管中,加水充分溶解、过滤, 向滤液中滴加酚酞试液. | 溶液由无色 变为红色 | 自己的猜 想正确 |
(反思与评价)小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是_____;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
(提出问题2)溶液B中溶质的成分是什么?
(猜想与假设)丙同学:KOH、K2CO3 丁同学:KOH、Ca(OH)2
(表达与交流)结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是_____.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为_____,小组同学通过相应的实验操作最终制得了氢氧化钾.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图:“如图1”,回答有关问题.
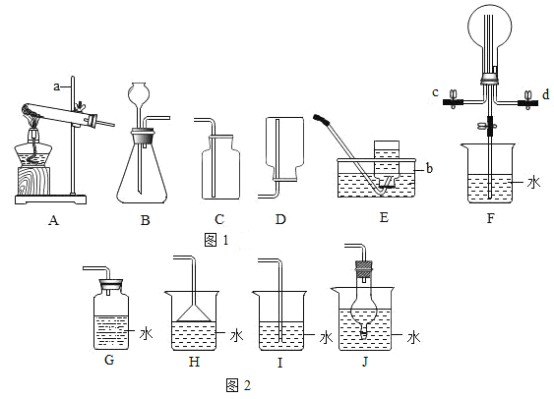
(1)写出图中标有仪器的名称:b_________;
(2)实验室用加热氯酸钾和二氧化锰的混合物制取氧气的化学方程式为____,选择的发生装置是____(填字母,下同),若得到较纯净的氧气,选择的收集装置是____;
(3)氨气是无色、有强烈刺激性气味的气体,密度比空气小,极易溶于水.实验室常用加热氯化铵和熟石灰混合物制取氨气,制取氨气的装置组合是____(填字母);
(4)某化学实验小组利用F装置收集氨气,并研究氨气的性质(部分仪器已略去)
①收集氨气时,氨气的进气口是____(填“c”或“d”) ;
②收集氨气后,进行探究氨气的性质实验,观察到烧瓶内产生了喷泉,说明氨气具有的性质是____;
③如图2为防止环境污染,G~J装置可用于吸收多余氨气的是____(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应中属于置换反应的是( )
A.C+H2O![]() CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
C.3CO+Fe2O3![]() 2Fe+3CO2D.2NaCl(熔融)
2Fe+3CO2D.2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com