
分析 结论与解释:从实验的过程可以证明铜和浓硫酸能反应,生成物中有二氧化硫和硫酸铜,其中的二氧化硫是有毒气体,不能直接排放到空气中,应该用碱液吸收.
反思与评价:浓硫酸溶于水要放出大量的热,所以浓硫酸不能倒入水中,浓硫酸中含有氢元素,生成物中也要有氢元素;
拓展与运用:考虑制取硫酸铜的方案的优缺点时,要从原料的利用率,环保,安全等方面考虑.
解答 解:[结论与解释](1)根据实验操作和现象,可以证明铜和浓硫酸在加热的时候能反应,生成物中有二氧化硫和硫酸铜,所以猜想②正确;
[反思与评价]:
(3)操作5中,从安全角度考虑不能将水倒入剩余的液体里,理由是如果浓硫酸有剩余,溶于水放热,比较危险;
浓硫酸溶于水会放出大量的热,造成液滴飞溅,所以不能把含浓硫酸的物质倒入水中.
(4)因为反应物中有氢,硫、氧、铜四种元素,根据反应前后元素的种类不变的原则,生成物中应该有氢元素,所以生成物质中除二氧化硫和硫酸铜外还有含有氢元素的物质存在.
[拓展与运用]
(5)比较这两个方案,从经济,环保,安全的角度考虑,浓硫酸使用时要注意安全,二氧化硫有毒等,通过综合考虑,利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4,浓硫酸具有极强的腐蚀性,使用不安全,有一部分硫元素转化成二氧化硫,污染空气,且造成原料的浪费,CuO与稀硫酸反应直接生成硫酸铜和水,所以方案乙比甲要好的多;
故答案为:
(1)②;
(3)从安全角度考虑不能将水倒入剩余的液体里,理由是如果浓硫酸有剩余,溶于水放热,比较危险;
(4)不正确;反应物中有氢元素,但二氧化硫和硫酸铜中都不含氢元素;
(5)甲的方案比较差,利用废铜屑和浓硫酸在加热的条件下反应制取CuSO4,浓硫酸具有极强的腐蚀性,使用不安全,有一部分硫元素转化成二氧化硫,污染空气,且造成原料的浪费;
点评 本题属于实验设计题,排在氢后的金属不与酸发生置换反应,但是可以和强氧化性的酸反应,浓硫酸具有强氧化性,完成本题,可以从题干给出的内容,提取有用的信息,分析归纳从而得出合理的答案,本考点主要出现在实验题中.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜用于制导线,是由于铜有良好的导电性 | |
| B. | 氮气常用作保护气,是由于氮气的化学性质不活泼 | |
| C. | 酒精做燃料,是由于酒精具有可燃性 | |
| D. | 氧气用于切割、气焊,是由于氧气具有可燃性 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实 验 步 骤 | 实 验 现 象 | 结 论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | 有白色沉淀产生 | 说明氢氧化钠溶液已经变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
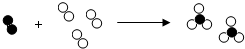 在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为
在实验室中,取140克化合物甲与30克化合物乙完全反应恰好生成170克的化合物丙.其反应的微观示意图如下,甲表示为 ,乙表示为
,乙表示为 ,丙表示为
,丙表示为 .
.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 连电源负极的管(A)中气体 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 |
| 连电源正极的管(B)中气体 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
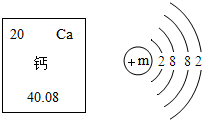 如图是钙在元素周期表中的相关信息及钙原子结构示意图,下列说法中错误的是( )
如图是钙在元素周期表中的相关信息及钙原子结构示意图,下列说法中错误的是( )| A. | m的数值是20 | B. | 钙属于金属元素 | ||
| C. | 钙元素在化合物中显+2价 | D. | 钙元素的质量是40.08g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com