
| 分析与计算 | 计算样品中碳酸钠的质量分数 | 对实验结果的评价 | 实验失败的主要原因及对结果的影响 |
| 甲组 | 79.5% | 失败 | 加入的稀硫酸没有完全将碳酸钠反应掉,且没有冷却至室温,部分二氧化碳存在于装置内,没有被C装置内的碱石灰所吸收,造成测量结果偏小 |
| 乙组 | 99.6% | 成功 |
分析 (1)根据碳酸氢钠的生产过程来分析;
(2)根据碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳这一方程式反应前后质量变化来分析.
解答 解:(1)因为NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl,所以生成的碳酸氢钠表面会沾有部分氯化钠,在加热碳酸氢钠的过程中,碳酸氢钠分解为了碳酸钠,而氯化钠不分解,故填:结晶析出的碳酸氢钠晶体表面沾有从溶液中带出的少量氯化钠;
(2)设甲族生成3.3g二氧化碳需要碳酸钠的质量为x
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 3.3g
$\frac{106}{44}=\frac{x}{3.3g}$
x=7.95g
样品中碳酸钠的质量分数为$\frac{7.95g}{10.00g}×100%$=79.5%
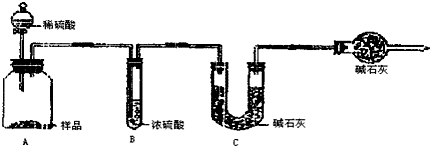
此实验中加入的稀硫酸没有完全将碳酸钠反应掉,且没有冷却至室温,部分二氧化碳存在于装置内,没有被C装置内的碱石灰所吸收,因此实验失败;
故填:79.5%;加入的稀硫酸没有完全将碳酸钠反应掉,且没有冷却至室温,部分二氧化碳存在于装置内,没有被C装置内的碱石灰所吸收,造成测量结果偏小;
取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量.反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g.设碳酸钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117
y 10.99g
$\frac{106}{117}=\frac{y}{10.99g}$
y≈9.96g
则碳酸钠样品中,碳酸钠的质量分数为$\frac{9.96g}{10.00g}×100%$=99.6%
故填:99.6%.
点评 本题充分考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力、分析解决问题的能力,难度稍大.


科目:初中化学 来源: 题型:解答题
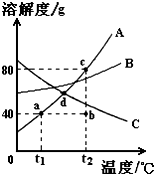 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用浓硝酸跟锌反应制氢气 | |
| B. | 用氯酸钾与木炭混合加热制氧气 | |
| C. | 用稀硫酸与大理石反应制二氧化碳 | |
| D. | 用干电池外壳的金属与稀硫酸反应制氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 |  | 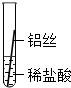 | 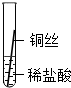 |
| 片刻后现象 | 缓慢产生少量气泡 | 无气泡 | 无气泡 |
| 几分钟后现象 | 缓慢产生少量气泡 | 快速产生大量气泡 | 无气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
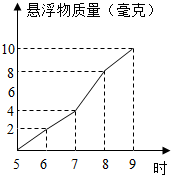 某校科学兴趣小组同学,为了具体了解当地的空气污染情况.
某校科学兴趣小组同学,为了具体了解当地的空气污染情况.| 测定次数 | 第1次 | 第 2次 | 第3次 | 第4次 |
| PH | 4.92 | 4.82 | 4.76 | 4.75 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com