
【题目】用如下图装置完成以下实验:
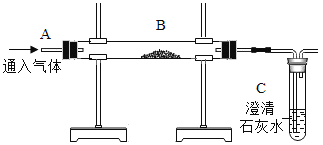
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
Ⅰ与Ⅲ对比,说明燃烧的条件之一是_____;Ⅱ与Ⅲ对比,说明燃烧的条件之一是_____。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。
Ⅰ.在A处通入一氧化碳一段时间后,B处下方用喷灯加热,B处可观察到的现象为_____,反应的化学方程式为_____,尾气处理的方法为_____。
Ⅱ.实验结束时,先_____(填“停止通入一氧化碳”、“停止加热”)。
【答案】需要氧气 温度达到着火点 红棕色固体变为黑色 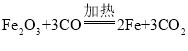 在尾气出口放一盏点燃的酒精灯 停止加热
在尾气出口放一盏点燃的酒精灯 停止加热
【解析】
(1)燃烧需要同时具备的三个条件:物质有可燃性、温度达到可燃物的着火点、与氧气充分接触;Ⅰ与Ⅲ对比,Ⅰ中没有氧气,木炭不燃烧,Ⅲ中有氧气,木炭燃烧,说明燃烧的条件之一是需要氧气;
Ⅱ与Ⅲ对比,Ⅱ中的木炭没有加热,木炭不燃烧,Ⅲ中的木炭加热了,木炭燃烧,说明燃烧的条件之一是温度达到着火点;
(2)Ⅰ、在A处通入一氧化碳一段时间后,B处下方用喷灯加热,一氧化碳和氧化铁反应生成铁和二氧化碳,B处可观察到的现象为红棕色固体变为黑色;
反应的化学方程式为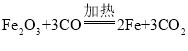 ;
;
尾气处理的方法是在尾气出口放一盏点燃的酒精灯,使一氧化碳燃烧生成二氧化碳;
Ⅱ、反应结束后应该先停止加热,防止C中的液体倒吸进B中,也可防止B中的铁再被氧化。


科目:初中化学 来源: 题型:
【题目】某碳酸钙样品中含有不和盐酸反应的杂质。某同学取12g该样品于烧杯中,再向烧杯中将100g稀盐酸分五次加入样品中,充分反应使气体全部逸出后,称得烧杯中所盛物质的总质量(不包含烧杯自身质量)如下表所示:
实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
烧杯中所盛物质的总质量/g | 30.90 | 49.80 | m | 87.60 | 107.05 |
请填空:
(1)碳酸钙和盐酸反应的化学方程式为_____;
(2)m的值为_____g;。
(3)12g石灰石样品中碳酸钙的质量分数等于_____;
(4)求反应完全后,溶液中氯化钙的质量_____(写计算过程,保留两位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。有关说法正确的是
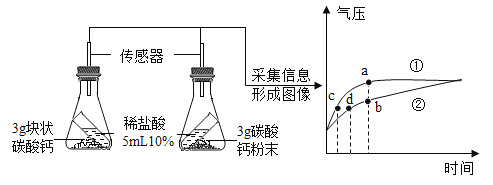
A.曲线①表示块状碳酸钙与稀盐酸反应
B.b点表示碳酸钙与盐酸反应已停止
C.等质量碳酸钙粉末比块状碳酸钙产生的CO2的质量多
D.对比分析点c、d可知,粉状碳酸钙与稀盐酸反应速率更快
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O ![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
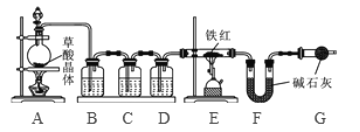
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
【实验反思】 (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对KCIO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
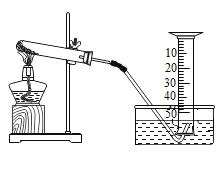
编号 | KCIO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mLO2所需时间/s |
实验1 | 5 | 一 | 一 | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是_____________。
(2)表中所列3种催化剂的催化效果最佳的是___________________。
(3)写出KCIO3分解的化学方程式:________________。
(4)由实验1和实验4可知,KC1_______________ (填“有"或“无”)催化作用。
(5)要比较KCIO3分解反应中不同催化剂的催化效果,除了测量收集50 mLO3所需时间外,还可以测量相同时间内______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是与铁的性质有关的部分实验,请回答。

(1)A中铁丝燃烧的化学方程式为_____。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可知铁钉生锈需要与_____接触。校园铁质护栏防锈可采用的一种措施是_____。
(3)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的的试剂组是_____ (填字母)。
A Mn Fe MgSO4溶液
B Mn FeSO4溶液
C Mn Fe ZnSO4溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a,b两种物质的溶解度曲线如下图所示.下列说法不正确的是
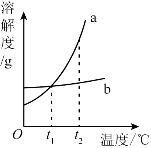
A.将![]() ℃时b的饱和溶液加水可变为不饱和溶液
℃时b的饱和溶液加水可变为不饱和溶液
B.将![]() ℃时a的饱和溶液降温至
℃时a的饱和溶液降温至![]() ℃,溶液质量不变
℃,溶液质量不变
C.![]() ℃时,两种物质的饱和溶液中溶质质量分数a
℃时,两种物质的饱和溶液中溶质质量分数a![]() b
b
D.将![]() ℃时a、b的饱和溶液分别降温至
℃时a、b的饱和溶液分别降温至![]() ℃,两溶液的溶质质量分数相等
℃,两溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)物质是由微粒构成的,请你填写构成下列物质的具体粒子的名称。
①空气中含量最多的氮气是由______构成的。
②盐水的主要成分氯化钠是由______构成的。
(2)建立适当的模型来反映和代替客观对象,可以帮助人们认识和理解一些不能直接观察到的事物.

①图甲是水分子的电解模型图,根据质量守恒定律可判断该模型图中少了______。
![]()
②图乙是水中各元素质量分数模型,请在图丙建立甲烷(CH4)中各元素的质量分数模型______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com