
【题目】二维价类图可有效帮助我们建立物质之间的联系,高效进行化学学习。
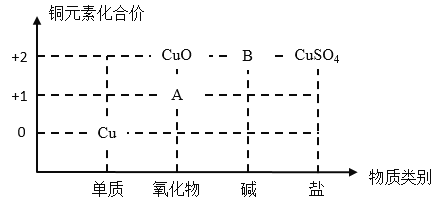
(1)铜单质常用作制电线,这体现了铜的_____性;区分铁丝和铜丝,最简单的方法是_____。
(2)图中物质A的化学式为_____;高温条件下,氧化铜会分解为A和一种常见的气体,写出该反应的化学方程式_____。
(3)图中物质B的化学式为_____,颜色为_____色。CuO可否通过一步反应,转化为CuSO4_____(填“能”或“不能”)。写出一种相对分子质量与B相等的酸与B反应的化学方程式_____,属于_____(填基本反应类型)。
(4)常用无水硫酸铜粉末检验水蒸气,该过程发生的是_____(填“物理变化”或“化学变化”)。
(5)实验室中经常用碳酸钠溶液与硫酸铜溶液制备产品——碱式碳酸铜,反应为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2_____+CO2↑。反应时若有少量3Cu(OH)2·CuCO3生成,则产品中铜元素的质量分数_____。(填“偏大”“不变”或“偏小”)
【答案】导电 观察颜色(其他答案不给分) Cu2O 4CuO![]() 2Cu2O+O2↑ Cu(OH)2 蓝 能 Cu(OH)2+H2SO4=CuSO4+2H2O(写与磷酸反应的化学方程式也给分) 复分解反应 化学变化 Na2SO4 偏大
2Cu2O+O2↑ Cu(OH)2 蓝 能 Cu(OH)2+H2SO4=CuSO4+2H2O(写与磷酸反应的化学方程式也给分) 复分解反应 化学变化 Na2SO4 偏大
【解析】
(1)铜单质常用作制电线,这体现了铜的电阻率低,导电性好;区分铁丝和铜丝的最简单方法是:观察颜色,铜丝是紫红色(或红色),铁丝是银白色;
(2)物质A属于氧化物,且铜的化合价为+1价,化学式为Cu2O;高温条件下,氧化铜会分解为氧化亚铜和氧气,该反应的化学方程式:4CuO![]() 2Cu2O+O2↑;
2Cu2O+O2↑;
(3)物质B属于碱类,化学式为Cu(OH)2,为蓝色固体。氧化铜能与硫酸反应生成硫酸铜和水,CuO能通过一步反应,转化为CuSO4。氢氧化铜的相对分子质量为98,硫酸的相对分子质量为98;氢氧化铜与稀硫酸反应产生硫酸铜和水的化学方程式:Cu(OH)2+H2SO4=CuSO4+2H2O,该反应符合“两交换、不变价”,属于复分解反应。
(4)常用无水硫酸铜粉末检验水蒸气,白色无水硫酸铜遇水产生五水硫酸铜(CuSO4·5H2O)晶体,有新物质产生,该过程发生的是化学变化。
(5)实验室中经常用碳酸钠溶液与硫酸铜溶液制备产品——碱式碳酸铜,该反应符合质量守恒定律:反应物比生成物多4个钠原子、2个硫原子和8个氧原子,则反应为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2Na2SO4+CO2↑。反应时若有少量3Cu(OH)2·CuCO3生成,3Cu(OH)2·CuCO3中铜元素质量分数大于Cu(OH)2CO3;则产品中铜元素的质量分数偏大。


 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
【题目】如图是利用石灰石,食盐水,氨气进行工业生产纯碱的流程示意图(部分条件及物质未标出)。
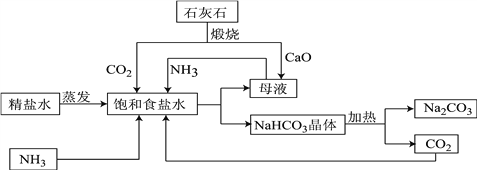
(1)粗盐精炼成精盐的过程中,要经过溶解、______、蒸发等操作,其中都必需用到的一种玻璃仪器为_______,
(2)图中母液含有一定量的NaHCO3,该溶液为该温度下NaHCO3的_________(填“饱和”或“不饱和”)溶液;
(3)流程中要通入CO2和NH3,应先通入NH3,理由是______________________________;精盐水经过氨化和二氧化碳酸化后生成碳酸氢钠和一种氮肥,请写出相应的化学方程式:_____。
(4)整个生产过程中可循环利用的物质为__________________(填化学式)。
(5)所得产品纯碱中含有少量碳酸氢钠,如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为(加热前固体的质量为m1,加热后为m2):_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜矿(主要成分 CuFeS2)经初步处理后,所得溶液中的溶质为Fe2(SO4)3、CuSO4及 H2SO4. 某同学通过废铁屑与所得溶液反应,制取还原铁粉并回收铜. 主要步骤如图所示:
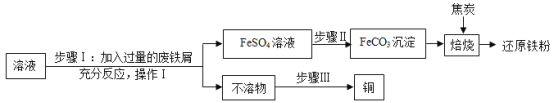
(1)Fe2(SO4)3与铁反应的化学方程式:x Fe2(SO4)3+y Fe═z FeSO4,其中 x、y、z 为化学计量数,z 的值为_____.
(2)操作Ⅰ的名称是_____,此操作中起到引流作用的仪器是_____.
(3)步骤Ⅰ中,生成铜的化学方程式:_____.
(4)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是_____.
(5)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是_____(填化学式).
(6)隔绝空气进行“焙烧”,铁元素的转化途径是FeCO3![]() FeO
FeO![]() Fe,实际作还原剂的是 CO. 写出“焙烧”过程中各步反应的化学方程式:
Fe,实际作还原剂的是 CO. 写出“焙烧”过程中各步反应的化学方程式:
①FeCO3![]() FeO+CO2↑
FeO+CO2↑
②_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
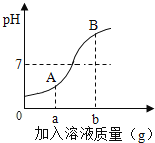
A.该反应是稀HCl滴入NaOH溶液中
B.ag是指加入氢氧化钠固体质量
C.A点溶液的溶质为HCl
D.检验B点溶液的溶质先滴加足量的Mg(NO3)2溶液,静置后再滴入少量AgNO3溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应中属于置换反应的是( )
A.C+H2O![]() CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
C.3CO+Fe2O3![]() 2Fe+3CO2D.2NaCl(熔融)
2Fe+3CO2D.2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过碳酸钠是一种多用途的新型漂白剂,化学式可表示为aNa2CO3·bH2O2,具有Na2CO3和H2O2的双重性质。过碳酸钠溶于水后分解成Na2CO3和H2O2。
(1)以下物质,会使过碳酸钠失效的是_____(填字母)。
A 二氧化锰 B 稀硫酸 C 澄清石灰水 D 氯化钡溶液
(2)测定某样品中过碳酸钠(aNa2CO3·bH2O2)的化学式,以及样品中过碳酸钠的纯度的实验步骤如下(样品中的杂质不参加反应):
步骤1:称取样品0.7g于锥形瓶中,加足量的水溶解,再滴加溶质质量分数为4.9%的稀硫酸8.000g,恰好完全反应。
步骤2:称取样品0.7g于锥形瓶中,加足量的水溶解,再加入1g二氧化锰,反应后收集得到气体67.20mL(该条件下氧气的密度为1.429g/L)。
①步骤1中发生的化学反应方程式为_____。实验室配制100g溶质质量分数为4.9%的稀硫酸,需要溶质质量分数为98%的浓硫酸_____mL(精确到0.1mL)(该条件下浓硫酸的密度为1.84g/mL);配制时需要用到的仪器有量筒、烧杯、玻璃棒_____,配制该稀硫酸应选择的量筒量程(水的密度为1g/mL)有_____(填字母)。
A 5mL B 20mL C 100mL D 200mL
②步骤2中发生的化学反应方程式为_____,如果没有冷却到室温就读取气体的体积,则过碳酸钠化学式中a∶b的测定结果将_____(填“偏大”“偏小”或“无影响”)。
③通过计算,确定该过碳酸钠化学式为_____。
④通过计算,确定该样品中过碳酸钠的纯度为_____。(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知图1中甲、乙、丙含有相同的某种元素,乙、丙为氧化物,且常温下丙为液态。
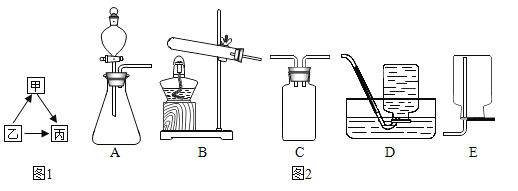
(1)写出实验室用图2中装置B制取甲的化学方程式________________________。
(2)写出一个有丙参与的化合反应________________________。
(3)已知某气体密度与空气接近且难溶于水,请在C图中补画完整该气体收集装置图并用箭头标明进气端________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述不正确的是( )
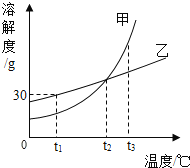
A.t1℃时,乙的饱和溶液65g中含有溶剂50g
B.t2℃时,甲的溶解度等于乙的溶解度
C.将t3℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
D.将t2℃时甲、乙的饱和溶液降温到t1℃,都有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】西藏“茶马古道”芒康县盐井是香格里拉唯一的产盐区。盐田是用紫红色粘土抹平压实的晒盐池,当地人把卤水注入盐田中经过日晒风吹,就得到上等且味道很好的红盐。为揭密红盐呈红色的原因,实验小组进行了如下探究活动。
(提出问题)红盐中存在什么物质使盐呈现红色?
(查找资料)
1、西藏紫红色粘土中含大量的氧化铁(Fe2O3)。
2、溶液中三价铁离子(Fe3+)遇到硫氰化钾(KSCN)溶液,溶液变为血红色。
(作出猜想)红盐中含少量的氧化铁使盐呈现红色;
(实验探究)小组同学从一定量的红盐中提取少量红色粉末,进行如下实验:
实验操作 | 实验现象 | 实验解释与结论 | |
实验I | 步骤①:取少量红色粉末于试管中,滴加适量稀盐酸; | 红色粉末恰好全部溶解; | 红色粉末中含有_____;步骤①涉及的反应的化学方程式_____ |
步骤②:往①所得溶液中滴入硫氰化钾(KSCN)溶液。 | 溶液变为血红色 | ||
实验Ⅱ | 步骤①:如图所示,将红色粉末与足量的黑色炭粉混合均匀,装入玻璃管中,先通一段时间氮气,再加热。
| 一定时间后,观察到澄清石灰水变浑浊,红色粉末变黑色 | 反应产生的气体为_____;红色粉末中一定含_____元素 |
步骤②:冷却后,取出玻璃管中黑色粉末,将磁铁靠近黑色粉末 | 黑色粉末部分被吸引 | 红色粉末中一定含_____元素 |
(实验结论)猜想_____(填写“正确”或“错误”)。
(实验反思)实验Ⅱ中能否用CO气体代替黑色炭粉并说明理由_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com