
【题目】请回答并完成下列计算。
(1)实验室要配制50g溶质质量分数为8%的氢氧化钠溶液,需称取______g氢氧化钠固体。
(2)向上述配制好的溶液中加入50g稀硫酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为__________。(反应的化学方程式:2NaOH + H2SO4==Na2SO4 + 2H2O)
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:
【题目】如图1为实验室常用装置。
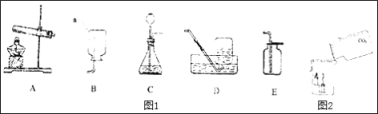
(1)仪器a的名称是_____。
(2)实验室用高锰酸钾制氧气时,试管中棉花的作用是_____,反应的化学方程式为_____。若用排水集气法收集,当气泡_____时开始收集。
(3)已知浓氨水和生石灰在常温下反应,可制得易溶于水的NH3.用该法制NH3时,应选择的发生装置是_____(填标号),收集装置是_____(填标号)。
(4)如图2所示,将二氧化碳气体慢慢倒入烧杯中,观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:①不支持燃烧;②_____;③_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )
![]()
A. 甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B. 若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C. D物质可能是气体,也可能是沉淀
D. 溶液B中的溶质一定只含有NaOH和甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用足量的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用一定量的氢氧化钠溶液完全吸收,该溶液总质量与反应时间的变化关系如图.
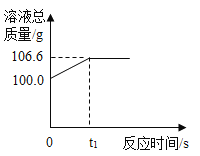
(1)上述反应产生二氧化碳的质量为________g;
(2)计算该赤铁矿石中氧化铁的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年“世界水日”的宣传主题为 "Nature for water"。
(1)爱护水资源,一方面要防治水体污染,另一方面要______________。
(2)“直饮水机”可将自来水净化为饮用水,其内部使用的活性炭主要起____________作用,生活中常用_________检验饮用水是硬水还是软水,常用___________的方法降低水的硬度,并起到消毒杀菌的作用。
(3)下图为电解水的实验装置图。通电一段时间后,玻璃管b中收集到的气体是______;该实验说明水是由___________ 组成的。
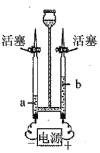
(4)C1O2是饮用水常用的消毒剂,制取C1O2的化学方程式为:C12+2NaC1O2=2C1O2+2X,X的化学式__________。
(5)下列是初中化学中常见的实验。相关说法错误的是______(填序号)。
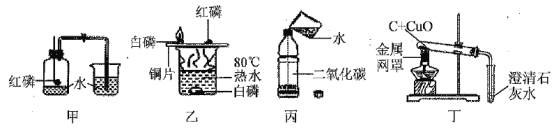
①甲实验的目的是测定空气中氧气的含量
②乙实验,水中的白磷没有燃烧,是因为温度没有达到着火点
③丙实验加水后,立即旋紧瓶盖,振荡,看到的现象是软塑料瓶向内凹陷
④丁实验,酒精灯上放的金属网罩是为了提高温度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
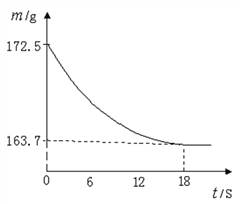
求:(1)生成CO2的质量为__________g。
(2)该纯碱样品中Na2CO3的质量分数为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验 设计 |
|
|
|
|
实验 目的 | 探究二氧化碳能与水反应 | 探究燃烧所需要的条件 | 探究铁生锈 需要氧气 | 探究空气中氧气的体积分数 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年12月28日,全球首段承载式太阳能光伏发电公路试验段在我省建成通车。高纯硅是光伏发电的重要材料,生产高纯硅的流程图如图:

(1)生产高纯硅需要对普通石英砂(含有少量Fe2O3杂质)进行提纯,其中酸洗是一个重要的步骤。请写出用盐酸除去Fe2O3的化学方程式_____。
(2)整个生产过程中必须控制无氧、无水。在HSiCl3与H2反应过程中若混入O2,可能引起的后果是_____。HSiCl3遇水能剧烈反应生成H2SiO3、H2与HCl,该反应的化学方程式是_____。
(3)为了节约资源,上述生产流程中可循环利用的物质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F均为初中化学常见的物质,已知:A、C是组成元素完全相同的化合物,C通常为液体,D为无色气体,F是白色难溶固体,其中金属元素的质量分数为40%。它们之间有如图所示的转化关系(部分物质和反应条件已略去)。
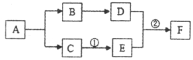
(1)A为 ,
(2)E物质在生活中的一种用途是 ;
(3)反应②的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com