
【题目】实验小组做了如下图所示实验。
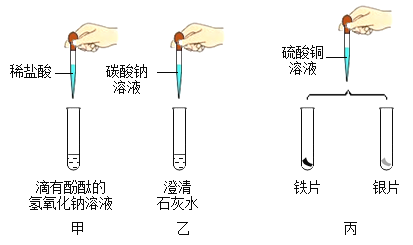
(1)能证明甲中发生反应的现象是_____。
(2)乙中可观察到的现象是_____,发生反应的化学方程式为_____。
(3)丙中观察到的现象为_____, 由该实验现象推断,三种金属活动性由强到弱为_____。
【答案】红色溶液逐渐变无色 有白色沉淀产生 ![]() 铁片上有红色固体析出,银片无明显变化 Fe>Cu>Ag
铁片上有红色固体析出,银片无明显变化 Fe>Cu>Ag
【解析】
(1)氢氧化钠溶液显碱性,使酚酞试液变红,而酸性或中性溶液不能使无色酚酞试液变色,能证明甲中发生反应的现象是红色溶液逐渐变无色;
(2)乙中可观察到的现象是有白色沉淀产生,发生反应为碳酸钠和氢氧化钙生成碳酸钙沉淀和氢氧化钠,化学方程式为![]() ;
;
(3)在金属活动顺序表中,金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。丙中观察到的现象为:铁片上有红色固体析出,银片无明显变化,说明铁能与硫酸铜反应,而银不能; 由该实验现象推断,三种金属活动性由强到弱为Fe>Cu>Ag。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】对如下图所示的实验分析不正确的是

A.甲:a吸引大头针比b多,说明电流一定时,线圈匝数越多,电磁铁磁性越强
B.乙:蜂窝煤比煤球燃烧更旺,说明反应物间的接触面积越大,反应越剧烈
C.丙:烧杯内壁出现水珠,说明甲烷的组成中含有碳元素和氢元素
D.丁:磁铁改变了小铁球的运动轨迹,说明力能够改变物体的运动状态
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,A~H是初中化学常见的物质。A和B可发生中和反应,X常用作食品干燥剂,Y为单质。根据图示回答下列问题:

(1)B的俗称为 。
(2)H的化学式为 。G必定含有的金属离子是 。(填符号)
(3)反应②的化学方程式为 。
(4)反应③的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Fe2O3、ZnO、CuO的固体混合粉末a g,在加热条件下用足量CO还原,得到金属混合物2.41 g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00 g白色沉淀,则a的数值为
A. 3.21 B. 3.59 C. 7.41 D. 2.46
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列装置回答有关问题:
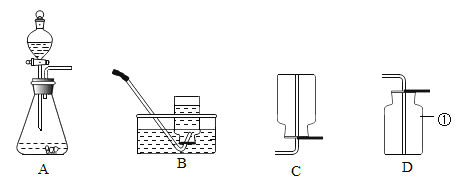
(1)仪器①的名称是_______。
(2)若要制取并收集较纯净的氧气,可从图中选择的装置组合是_____(填字母) ;组装完气体发生装置后,应先____,再添加药品。
(3)装置D收集CO2时,用_____检验气体是否集满。
(4)实验室用锌粒和稀硫酸制取氢气,__(填“能”或“不能”)选择A为发生装置。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列图示,回答问题。
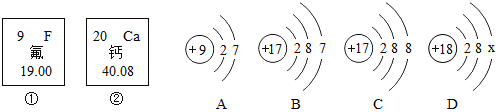
(1)氟元素的相对原子质量为__________;D中的x是______________。
(2)①和②是不同种元素,它们的最本质的区别是______________。
(3)A、B、C、D结构示意图中,属于同种元素的粒子是_____________(填序号)
(4)A粒子的化学性质与B、C、D中______________(填序号)粒子的化学性质相似。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体中的钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙晶体(Ca10(PO4)6(OH)2)形式存在,其相对分子质量为1004,牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。如图是某品牌纯牛奶包装上的部分文字说明,请认真阅读后回答下列问题:

(1)牛奶中富含的营养素为 (填一种即可)。
(2)Ca10(PO4)6(OH)2由 种元素组成。
(3)一盒牛奶含钙至少多少g?(精确到0.01)
(4)若人体每天至少需要0.6g钙,而这些钙有90%来自牛奶,则一个人每天要喝多少盒牛奶?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是实验室制取气体的常用装置。请回答下列问题。
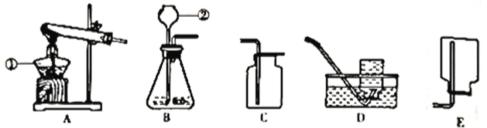
(1)A装置中仪器①的名称是______试管口略向下 倾斜的原因是___________ 。
(2)仪器②的名称是___ 该仪器的主要 作用是______________ 。
(3)实验室用加热氧酸钾制取氧气,应选择的发生装置为_______(填字母序号);若要收集较纯净的氧气,应选择的收集装置是_________ ( 填字每序号)。写出过氧化氢溶液和二氧化锰的混合物制取氧气的化学方程式___________________________ 。
(4)制取氧气和二氧化碳均可选择的发生装置和收集装置为_____________ ( 填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
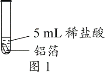
【题目】化学小组同学用图1装置探究铝与盐酸的反应。将未去除表面氧化膜的铝箔放入稀盐酸中,刚开始反应现象不明显,一段时间后反应比较剧烈,产生大量气泡,出现灰色沉淀。
(查阅资料)
①铝粉在颗粒较小时为灰黑色;铝既能与酸反应,又能与碱反应,且反应均生成氢气。
②氯化铝固体为白色颗粒或粉末,易溶于水和乙醇。
③氧化铝与盐酸反应的化学方程式为:![]() 。
。
(实验一)探究灰色固体的成分
实验序号 | 1-1 | 1-2 | 1-3 | 1-4 |
实验操作 |
|
|
|
|
实验现象 | 有微量气泡产生,固体溶解 | 有少量气泡产生,固体溶解 | ____________ | 固体部分溶解 |
(实验二)探究盐酸浓度对灰色固体产生量的影响
取0.09 g铝箔和5 mL不同浓度的稀盐酸,用图1装置进行实验。
实验序号 | 盐酸浓度 | 实验现象 |
2-1 | 4.0% | 刚开始反应现象不明显,一段时间后缓慢反应,然后反应比较剧烈,有大量气泡产生,出现灰色沉淀 |
2-2 | 2.8% | 先是看不到反应现象,一段时间后缓慢反应,然后慢慢地反应比较剧烈,有大量气泡产生,出现少量灰色沉淀 |
2-3 | 2.1% | 3~4小时后明显有气泡产生,反应慢慢地比较快些,试管底部出现少量灰色沉淀 |
2-4 | 1.4% | 反应更慢,出现极少量的灰色沉淀 |
(解释与结论)
(1)铝与盐酸反应的化学方程式为___________。
(2)图1所示实验中,刚开始反应现象不明显,一段时间后才看到有气泡产生的原因是________。
(3)由实验________(填实验序号)可以判断灰色固体中含有铝。
(4)由实验1-4可知,灰色固体中还含有氯化铝。实验1-3的现象是_________。
(5)实验二的结论是__________。
(反思与交流)
(6)为了进一步探究灰色沉淀的出现是否与盐酸中的Cl-有关,可以将稀盐酸换成______进行图1所示实验。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com