


 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֻ�÷�̪��Һ������NaCl��NaOH��HCl����ˮ��Һ |
| B��ֻ��ˮ���Լ���CuSO4��NaOH��NH4NO3���ֹ��� |
| C���÷���ˮ�������ϡ����ͱ��ͳ���ʯ��ˮ |
| D������ʹ��Ba(OH)2��Һ����(NH4)2CO3��(NH4)2SO4���ֵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��ͼ1��b��c�α�ʾ��������Ĺ��� |
| B��ͼ1��b���ֵΪ106 |
| C��ͼl��c��ʱ����Һ�е����������� |
| D��ͼ1��o��a�η�Ӧ��������Һ��pH�仯�������ͼ2��d��h�α�ʾ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
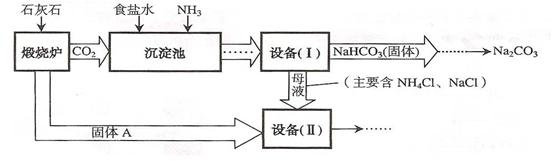
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CuSO4��H2SO4��NaNO3 | B��NaCl��CaCl2��Ba(NO3)2 |
| C��HNO3��H2SO4��NaHCO3 | D��HNO3��BaCl2��Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
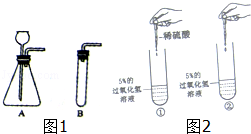
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ѡ�� | ���� | �������� | �����ʵķ��� |
| A | CO | CO2 | ͨ������������������Һ������ |
| B | KCl��Һ | CuSO4 | ��������������������Һ������ |
| C | Cu | Fe | ���������ϡ���ᡢ���ˡ�ϴ�ӡ����� |
| D | CaO | CaCO3 | ����������ϡ���ᡢ���ˡ�ϴ�ӡ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������ˮ |
| B�������Ǽ�������� |
| C������ȿɴ���½�κ���ȡ���ֿ��á����������Ƽ������ |
| D������llt����������С�մ������ϡ�����ȥ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com