
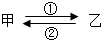
 甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.
甲、乙是初中化学常见的物质,它们在一定条件下能如图所示相互转化.
| ||
| ||


科目:初中化学 来源: 题型:
| A、①② | B、②④ | C、③④ | D、③ |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 现象 | 结论 |
| 取两支试管,分别加入20mL浓度为10%的盐 酸,同时将2g镁粉、2g铁粉放入盐酸中 |
加入镁粉的试管中产生气体速率更快 |
查看答案和解析>>
科目:初中化学 来源: 题型:
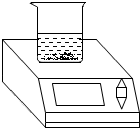 小明同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签.他做了如图实验:称量该溶液34.0g倒入烧杯中,然后向其中加入0.5g二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为32.9g.
小明同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签.他做了如图实验:称量该溶液34.0g倒入烧杯中,然后向其中加入0.5g二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为32.9g.查看答案和解析>>
科目:初中化学 来源: 题型:
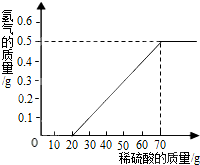 某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).
某兴趣小组用10g镁条与溶质质量分数为49%的稀硫酸反应,测得产生氢气的质量与稀硫酸的质量关系如图(假设镁条中除表面含有氧化镁外,没有其它杂质).查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液 | 现象B |
查看答案和解析>>
科目:初中化学 来源: 题型:
 常温下,过氧化氢分解生成氧气的速率较为缓慢.研究性学习小组选择“过氧化氢分解生成氧气的快慢与什么有关”的课题进行研究,以下是他们的主要过程:
常温下,过氧化氢分解生成氧气的速率较为缓慢.研究性学习小组选择“过氧化氢分解生成氧气的快慢与什么有关”的课题进行研究,以下是他们的主要过程:| 实验编号 | ① | ② |
| 反应物 | 5%过氧化氢50g | 5%过氧化氢50g |
| 加入固体 | 氯化钠固体 | 1g二氧化锰 |
| 收集气体所需时间 | 165s | 46s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com