
【题目】Q同学将装有硫酸镁和硫酸铜废液的烧杯中,放入一定量的铁粉,搅拌,待充分反应后过滤、洗涤,得到固体A和溶液B,操作步骤如图所示。请你与小组同学共同完成以下探究:
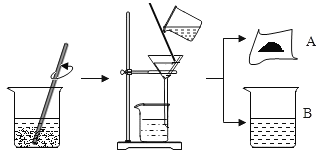
加入铁粉时一定发生反应的化学方程式为___________________________
探究实验1(提出问题)滤液中的溶质成分?
(猜想与假设) 超超同学:MgSO4 楠楠同学:FeSO4、MgSO4 鹍鹍同学:……
(表达交流)若鹍鹍同学猜想合理,则她的猜想是_______________________
(反思评价)请你评价超超同学的猜想_________________________________
(归纳总结)确定合理猜想的方法是:与所加物质反应后生成的溶于水的物质一定存在;与所加物质_________的溶质一定存在;与所加物质发生反应的溶质可能存在。
探究实验2(提出问题)固体A中的成分是什么?
(进行实验)取少量固体于试管中,加入少量稀盐酸,观察到的现象是__________ ; 得出固体成分为Fe、Cu.
(表达交流)在得出固体A的成分后,也确定了溶液B中溶质的成分为(填化学式)______________。
(归纳总结)在此探究实验中:根据上述探究确定固体A成分实验后,也可以确定溶液B合理猜想的对与错,依据原理是合理猜想的溶质成分能与_______________的猜想是错误的,从而确定了溶质的成分。
【答案】![]() CuSO4、FeSO4、MgSO4 不正确,加入铁粉后一定与硫酸铜溶液反应生成可溶于水的硫酸亚铁一定存在,所以错误(或硫酸亚铁是溶于水的生成物一定存在) 不发生反应 固体表面有气泡产生 MgSO4、FeSO4 固体A中物质发生反应
CuSO4、FeSO4、MgSO4 不正确,加入铁粉后一定与硫酸铜溶液反应生成可溶于水的硫酸亚铁一定存在,所以错误(或硫酸亚铁是溶于水的生成物一定存在) 不发生反应 固体表面有气泡产生 MgSO4、FeSO4 固体A中物质发生反应
【解析】
根据铁能与硫酸铜反应生成硫酸亚铁和铜分析;
[猜想与假设]根据滤液中的溶质可能有硫酸镁和硫酸铜、硫酸亚铁分析;
[反思评价]根据铁一定能与硫酸铜反应生成硫酸亚铁,且硫酸亚铁溶于水分析;
[归纳总结]根据确定合理猜想的方法分析;
[进行实验]根据固体成分中有Fe时,一定能与稀盐酸反应生成氢气分析;
[表达交流]根据若铁有剩余时,则溶液中一定不再有硫酸铜分析;
[归纳总结]根据固体A中的成份不能与FeSO4、MgSO4反应分析;
铁能与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:![]() ;
;
[猜想与假设]铁能与硫酸铜反应生成硫酸亚铁和铜,若铁的量不足,则滤液中的溶质有硫酸镁和硫酸铜、硫酸亚铁,若铁的量足够,则硫酸铜完全反应掉,滤液中只会有硫酸镁和硫酸亚铁;由于楠楠同学猜想滤液中有FeSO4、MgSO4;则鹍鹍同学可猜想滤液中的溶质有硫酸镁和硫酸铜、硫酸亚铁;
[反思评价]超超同学的猜想不正确,因为铁一定能与硫酸铜反应生成硫酸亚铁,且硫酸亚铁溶于水;
[归纳总结]确定合理猜想时要注意,一是与所加物质反应后生成的溶于水的物质一定存在;二是与所加物质不发生反应的溶质一定存在;三是与所加物质发生反应的溶质可能存在,根据实验现象分析可能性;
[进行实验]固体成分中有Fe时,一定能与稀盐酸反应生成氢气,所以会在固体表面产生气泡;
[表达交流]确定固体A的成份为Fe、Cu后,可知铁有剩余,则证明硫酸铜完全反应,溶液中一定不再有硫酸铜;
[归纳总结]固体A中的成份为Fe、Cu,它们都不能与FeSO4、MgSO4反应,所以可证明溶液的成份。


科目:初中化学 来源: 题型:
【题目】一定条件下,A、B、C、D四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
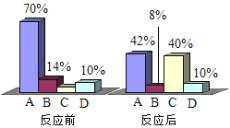
A. D一定是该反应的催化剂B. 该反应的基本类型是分解反应
C. 该反应中B、C的质量比为3:17D. 该反应中A、C的质量比为21:20
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用15 g石灰石样品,把50g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的累计加入量 | 10g | 20g | 30g | 40g | 50g |
剩余固体的质量 | 12g | 9g | 6g | 5g | 5g |
请计算:
(1)石灰石中碳酸钙的质量分数为_______?
(2)最终生成二氧化碳的质量是______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】9月16日我校举办了声势浩大的秋季运动会,在欢乐轻松的氛围中发扬体育精神。田径比赛时发令员使用的发令枪如图所示,下列有关说法不正确的是( )

A. 发令枪使用的无缝钢管是纯铁制作
B. 计时员看到发令枪冒烟开始计时
C. 发令枪子弹弹壳采用的黄铜是铜锌合金
D. 使用后的发令枪要及时清理擦净污垢避免锈蚀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近年来随着人们生活水平的提高,汽车已经成为人们主要的出行工具.

(1)汽车的车圈通常使用铝合金材料,是因为铝合金具有___的物理性质(在A、B、C中选).
A 良好导电性 B 抗腐蚀性能好 C 强度硬度较好
(2)铝合金中的金属铝是一种化学性质比较活泼的金属,它不但能与酸反应,还能与氢氧化钠(NaOH)、水反应,生成偏铝酸钠(NaAlO2)和一种可燃性气体单质,请写出此反应的化学反应方程式___铝元素在反应前后的化合价分别是___.
(3)电动汽车以环保、节能的优势日益受到大家的青睐.电动汽车在行驶过程中的能量转化全过程是___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】广州医学院钟南山院士强调:H7N9禽流感发病5日内使用达菲可显著减少重症,禽流感患者越早治疗效果越好。“达菲”主要有效成分是莽草酸(C7H10O5),下列关于莽草酸说法正确的是( )
A. 属于氧化物
B. 由7个碳元素、10个氢元素、5个氧元素组成
C. 174g莽草酸中含有84g碳元素
D. 一个莽草酸分子中含有5个氧分子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学探究小组为了验证铁、铜、锌、银的金属活动性顺序,设计了如下实验方案:
①将铁片加入到稀盐酸中 ②将铜片加入到硝酸银溶液中 ③将锌片加入到稀盐酸中 ④将金属片X加入到Y中。(所有金属均已打磨,且形状、大小以及稀盐酸浓度均相同)
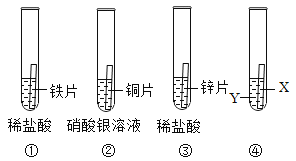
(1)写出①中反应的化学方程式:_____________________;
(2)通过上述实验,可以判断锌的金属活动性比铁强,依据的现象是_______________________;
(3)要得出这四种金属的活动性顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是________。
(4)防止金属腐蚀,特别是钢铁的锈蚀是世界科学研究和技术领域中的重大问题。某同学为了探究铁生锈与哪些因素有关,设计了一个实验(如图所示):该同学找到三个铁钉,经过酸洗除锈、干燥后,分别放入A、B、C三支试管中;再向A、B试管中各注入煮沸后迅速冷却的蒸馏水,A中的铁钉部分浸入水中,B中的铁钉浸没水中,并在水面上注入一层植物油;C中放入一团裹有干燥剂CaO的棉花并塞上橡皮塞。
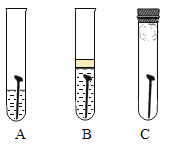
在三支试管中,容易生锈的是_________中的铁钉,因此铁生锈的条件是:___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像对应关系正确的是
A. 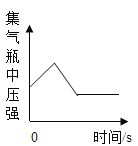 在盛有空气的密闭集气瓶中引燃红磷
在盛有空气的密闭集气瓶中引燃红磷
B. 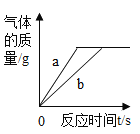 a、b两试管内分别加入等浓度等体积的过氧化氢溶液,其中a试管内有少量二氧化锰
a、b两试管内分别加入等浓度等体积的过氧化氢溶液,其中a试管内有少量二氧化锰
C. 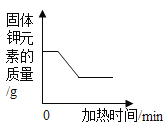 加热一定质量的高锰酸钾制取氧气
加热一定质量的高锰酸钾制取氧气
D. 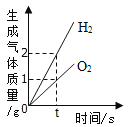 电解水
电解水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“三效催化转换器”可将汽车尾气中有害气体处理为无污染的气体,下图为该反应的微观示意图,其中不同颜色球代表不同种原子。下列说法错误的是
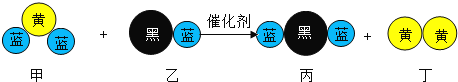
A. 乙和丙中所含元素种类相同B. 甲和丁中同种元素化合价不相等
C. 该反应中共有三种元素D. 化学方程式中乙、丁的化学计量数均为1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com