
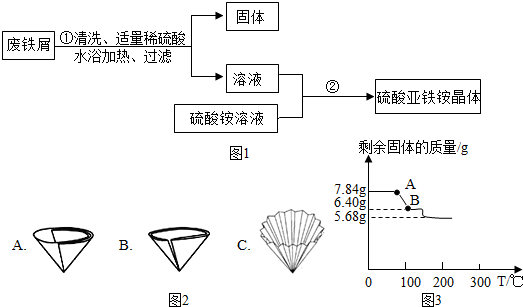
���� ��1������ϴ�Ӽ����黯���÷���ϴ�Ӽ������ã���������ϡ���ᷴӦ��������������������д��Ӧ�ķ���ʽ��
��2�����ݹ��˵IJ��������������Ʒ����
��3�����ݸ���ͭ��������ᷴӦ�����Կ��Թ��˳���������ʵ��IJ������������������ܽ�ȣ�
��4�����������������ܽ�����¶ȵ�Ӱ������ᾧ�ķ�����
��5��������������茶���������ˮ�����ھƾ����ƾ������ʷ������
��6�����ݰ����ܺ�ˮ��Ӧ���ɰ�ˮ����ˮ�ʼ�����ʹʯ�����ɫ����NH4��2SO4��NaOH��Ӧ���������ơ�ˮ�Ͱ������ֽⷴӦ�Ķ�����
��7��֤���Ȼ�������ֻҪ֤����������ʣ�༴�ɣ�������������������ƺͺ��Ȼ����ķ�Ӧ��������x��y�ı�ֵ���ٽ�Ϸ����ķ�Ӧ���x��y��z�ı�ֵ��
��8��A��BʱxFeSO4•y��NH4��2SO4•zH2O�ֽ�õ�������李���������茶����ˮ�Ĺ��̣�
��� �⣺��1��������ˮ��ϴ�Ӽ�����ֽ��裬�Գ�ȥ����м��������ۣ���������ϴ�Ӽ����黯���ã�����ϡ���ᷴӦ����������������������Ӧ�Ļ�ѧ����ʽΪ��Fe+H2SO4=FeSO4+H2����
��2����������IJ����������ձ�����������©�������˲�������ֽ�ж����۷���Ϊ�˼ӿ�������ʣ���ѡ���۷���A��
��3������ϡ����������Ժ����ᷴӦ����������������������ͭ��������ᷴӦ�����ͭ�ͱ����˳��������ԣ����˺�õ��Ĺ�����һ�����е�������ͭ��
��4�������ڵ�Ŀ���ǵõ���������茶��壬������������淋��ܽ�����¶ȵ�Ӱ��ϴ����Ի����������裺����Ũ����Ȼ����ȴ�ᾧ���ٹ��ˣ����ϴ�Ӹ��
��5��������������ˮ�����ھƾ�����A����ϴ����������������ʧ�϶࣬���þƾ�ϴ�ӣ��ƾ����ӷ����ܵõ������Ĵ����������������壬�ʴ𰸣�AB��
��6�������ܺ�ˮ��Ӧ���ɰ�ˮ����ˮ�ʼ�����ʹʯ�����ɫ����NH4��2SO4��NaOH��Ӧ���������ơ�ˮ�Ͱ����� ��Ӧ�ķ���ʽ�ǣ�NH4��2SO4+2NaOH=Na2SO4+2NH3��+2H2O��
��7����������������������ɫ����֤���������Ѳ�����BaCl2����˵�������Ѿ�ϴ�Ӹɾ���
����������茶���������淋�����Ϊx��
��NH4��2SO4+2NaOH=Na2SO4+2NH3��+2H2O
132 34
x 0.68g
$\frac{132}{34}=\frac{x}{0.68g}$ ��ã�x=2.64g
�������立�Ӧ�������ᱵ����������Ϊy
��NH4��2SO4+BaCl2=BaSO4��+2NH4Cl
132 233
2.64g y
$\frac{132}{233}=\frac{2.64g}{y}$ ��ã�y=4.66g y=4.66g
���Ժ�����������Ӧ�������ᱵ����������Ϊ9.32g-4.66g=4.66g��
�������������Ӧ�������ᱵ����������Ϊz
FeSO4+BaCl2=BaSO4��+FeCl2
152 233
z 4.66g
$\frac{152}{233}=\frac{z}{4.66g}$ ��ã�z=3.04g
�����������$\frac{3.04g}{2.64g}$=$\frac{152x}{132y}$��$\frac{x}{y}$=$\frac{1}{1}$���ʴ𰸣�1��1��
��A��B������������������������ɵ�ˮ��������7.84g��������茶�����ˮ������Ϊ7.84g-5.68g=2.16g��$\frac{132y}{18z}$=$\frac{2.64g}{2.16g}$��$\frac{y}{z}$=$\frac{1}{6}$ �ʴ𰸣�1��1��6��
��8����FeSO4•��NH4��2SO4•6H2O$\frac{\underline{\;\;��\;\;}}{\;}$FeSO4+��NH4��2SO4•2H2O+4H2O������FeSO4•��NH4��2SO4•6H2O�ֽ�õ���������������李���ˮ����Ӧ�ķ���ʽ�ǣ�FeSO4•��NH4��2SO4•6H2O$\frac{\underline{\;\;��\;\;}}{\;}$FeSO4+��NH4��2SO4•2H2O+4H2O��
�ʴ�Ϊ����1���黯��Fe+H2SO4=FeSO4+H2������2��©����A����3����Cu����4��c��a����5��AB����6����NH4��2SO4+2NaOH=Na2SO4+2NH3��+2H2O����7��1��1��1��1����8��FeSO4•��NH4��2SO4•6H2O$\frac{\underline{\;\;��\;\;}}{\;}$FeSO4+��NH4��2SO4•2H2O+4H2O��
���� ͨ�����������ѧ���۲���ͼ���������Լ��ȽϷ��������������⿼���˳��������������Լ�ijЩ�ε����ʣ���ɴ��⣬������������ṩ�����ݣ����г�ȡ���õ���Ϣ��������е�֪ʶ���У�������һ��ʵ��̽���⣬�ܽϺõĿ���ѧ�������ͽ������������������˳��������������Լ�ijЩ�ε����ʣ����ʱҪ��������ṩ��Ϣ��������֪ʶϸ�ķ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
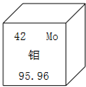 ��Ԫ�����ڱ�����Ԫ�ص������Ϣ��ͼ��ʾ������˵����ȷ����C��
��Ԫ�����ڱ�����Ԫ�ص������Ϣ��ͼ��ʾ������˵����ȷ����C���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
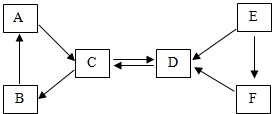 ȡA----F���ֳ������ʣ�����A�����ڸ�������������B�dz��õĹ���������A��B��C���嶼����ͬ�ֽ���Ԫ�أ�E�Ǻ�ɫ���嵥�ʣ�D��E��F������ͬ�ַǽ���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ����ش�
ȡA----F���ֳ������ʣ�����A�����ڸ�������������B�dz��õĹ���������A��B��C���嶼����ͬ�ֽ���Ԫ�أ�E�Ǻ�ɫ���嵥�ʣ�D��E��F������ͬ�ַǽ���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
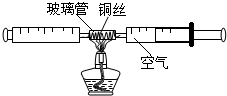 �ڲⶨ����������������ʵ���У�Сǿ��������ͼ��ʾװ�ã���������ע������ɵ��ܱ�ϵͳ������25mL��������װ��ϸͭ˿�IJ����ܼ��ȣ�ͬʱ�����ƶ�����ע�������������������ڵ�ͭ˿�ڽϳ�ʱ������һ���仯ʱֹͣ���ȣ�����ȴ�����£�������ȫ������һ��ע�����ڣ��۲��ܱ�ϵͳ�ڿ�������仯��
�ڲⶨ����������������ʵ���У�Сǿ��������ͼ��ʾװ�ã���������ע������ɵ��ܱ�ϵͳ������25mL��������װ��ϸͭ˿�IJ����ܼ��ȣ�ͬʱ�����ƶ�����ע�������������������ڵ�ͭ˿�ڽϳ�ʱ������һ���仯ʱֹͣ���ȣ�����ȴ�����£�������ȫ������һ��ע�����ڣ��۲��ܱ�ϵͳ�ڿ�������仯��| ��Ӧǰע��������������� | ��Ӧ��ע��������������� |
| 25mL | 22mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com