
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)木炭还原氧化铜生成铜和二氧化碳,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(2)铝在空气中被氧化生成氧化铝,反应的化学方程式为:4Al+3O2═2Al2O3;该反应符合“多变一”的特征,属于化合反应.
(3)酒精在空气中燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
故答案为:(1)C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;置换反应;(2)4Al+3O2═2Al2O3;化合反应;(3)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤1的现象 | 步骤2的结果 | 步骤4的现象 | 结论 |
| 产生大量气泡,带火星的木条复燃 | 固体的质量为 1.2g | 产生大量气泡,带火星的木条复燃 | 猜想A、B不成立,猜想C成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
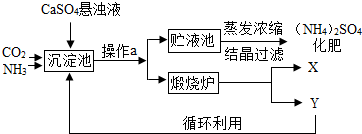 某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
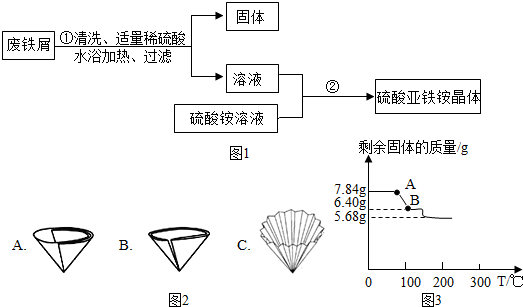
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
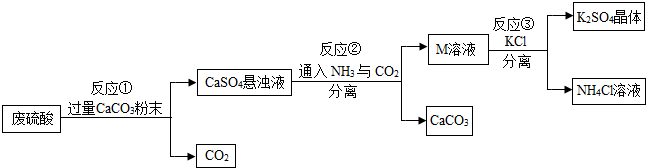
| 物质 | KCL | K2SO4 | NH4Cl | (NH4)2SO4 |
| 溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
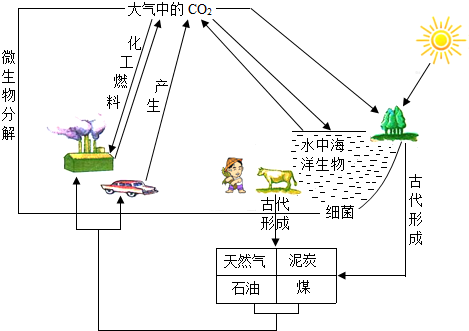
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com