
【题目】金属材料与人类的生产和生活密切相关,请回答:
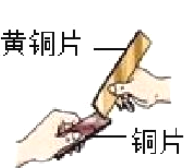
(1)铜片与黄铜片相互刻画,铜片表面留下明显划痕,说明铜片比黄铜片的硬度_______。(填“大”或“小”)
(2)不锈钢、黄铜(铜、锌合金)和碳化钨等是制作圆珠笔“笔头”的主要材料。下列关于这些材料的说法错误的是_______。
a.铁是不锈钢的主要组成元素之一
b.不锈钢与黄铜都具有耐腐蚀的性能
c.黄铜的导电性能比铜更好
d.碳化钨是一种混合物
(3)铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程:![]() _______
_______![]()
【答案】小 cd CO2
【解析】
(1)合金比组成成分金属的硬度大,所以黄铜是铜锌合金,将纯铜片和黄铜片相互刻画(如右图所示),纯铜片上留下明显的划痕,说明黄铜的硬度比纯铜的大;
(2)a.根据不锈钢的组成元素,可知铁是不锈钢的主要组成元素之一,故不符合题意;
b.不锈钢与黄铜都不与酸反应,都具有耐腐蚀的性能,故不符合题意;
c.铜的导电性能比黄铜更好,故符合题意;
d.碳化钨中含有一种物质,是一种纯净物,故符合题意。故选cd。
(3)2Cu+O2+X+H2O═Cu2(OH)2CO3,假设方框内的物质是X,反应前含有2个Cu原子,3个O原子,2个H原子,X,反应后含有2个Cu原子,5个O原子,2个H原子,1个C原子,故X中含有1个C原子和2个O原子,是二氧化碳,故填:CO2。


科目:初中化学 来源: 题型:
【题目】金属在生产生活中应用广泛。
(1)最初输水管材用铸铁,目前多用塑料管和塑料金属复合管,输送热水一般用铜管。下列管材中,属于金属材料的是______![]() 填字母序号
填字母序号![]() 。
。

(2)铁是生活中常用的金属。如图是某“取暖片”外包装的图片。该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会发热。

![]() 发热剂需接触空气才会发热,原因是铁要与______等物质共同作用才会生锈。
发热剂需接触空气才会发热,原因是铁要与______等物质共同作用才会生锈。
![]() 推测发热剂成分中氯化钠的作用______。将生锈的铁片放在盐酸和氯化铜的混合溶液中,可能发生的置换反应的化学方程式是______。
推测发热剂成分中氯化钠的作用______。将生锈的铁片放在盐酸和氯化铜的混合溶液中,可能发生的置换反应的化学方程式是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习二氧化碳性质时,将二氧化碳气体通入紫色石蕊溶液中,观察到紫色石蕊溶液变红,下列是某化学兴趣小组对紫色石蕊溶液变红色原因的实验探究。
(知识储备)浓硫酸可以吸收水分。
(提出问题)是什么物质使紫色石蕊变红色的?
(提出假设)①二氧化碳使紫色石蕊变为红色。②水使紫色石变为红色。③二氧化碳和水反应生成的碳酸使紫色石蕊变为红色。
(设计实验)
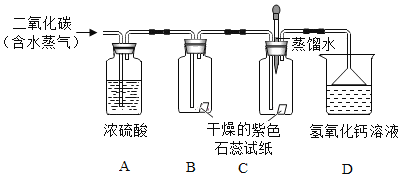
请根据他们的实验,回答下列问题
(1)装置A的作用是_____。
(2)实验过程中,B内试纸的颜色没有变化,这说明_____。
(3)C装置中未通入二氧化碳之前,在紫色石蕊试纸上滴入蒸馏水,未见试纸颜色变化,说明假设_____不成立(填序号,下同),之后通入二氧化碳,看到试纸变红,由此说明假设_____成立,原因是_____(用化学方程式填空)。
(4)D中反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对下列事实的微观解释正确的是![]()
![]()
选项 | 事实 | 解释 |
A | 体温计中的水银 | 分子间间隔随温度改变 |
B | 氧气能压缩在蓝色钢瓶中 | 氧分子大小随压强变大而减小 |
C | 金刚石、石墨性质存在明显差异 | 碳原子的排列方式不同 |
D | 氮气是无色的 | 氮分子是无色的 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取25g粉碎的石灰石样品![]() 杂质不溶于水也不与盐酸反应
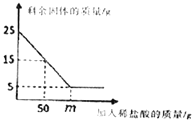
杂质不溶于水也不与盐酸反应![]() ,放入小烧杯中,慢慢加入一定浓度的稀盐酸,测得稀盐酸的用量与固体的质量关系如图所示。请回答下列问题:
,放入小烧杯中,慢慢加入一定浓度的稀盐酸,测得稀盐酸的用量与固体的质量关系如图所示。请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为______。
(2)石灰石样品中碳酸钙的质量分数是______。
(3)根据已知条件列出反应所得气体质量![]() 的比列式______。
的比列式______。
(4)图中![]() ______。
______。
(5)![]() 稀盐酸中含有HCl的质量为______g。
稀盐酸中含有HCl的质量为______g。
(6)用100t此石灰石可制取含杂质![]() 的氧化钙的质量为______。
的氧化钙的质量为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石墨烯是一种革命性材料,具有优异的光学、电学和力学特性。图为金刚石、石墨和石墨烯的结构模型图,图中小球代表碳原子。下列说法正确的是( )
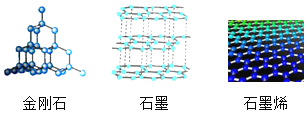
①石墨烯是一种新型化合物
②三种物质分别在足量的氧气中完全燃烧的产物相同
③金刚石和石墨烯是组成相同但结构不同的两种物质
④石墨烯有超强的导电性和导热性,说明石墨烯的化学性质和金属相似
A. ①④ B. ②③ C. ①③ D. ②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定黄铜(Cu﹣Zn合金)中铜的质量分数,某同学将20g该合金放入到盛有100g盐酸的烧杯中,锌与盐酸恰好完全反应。反应停止后,测得烧杯中剩余物的总质量为119.8g。
(1)生成氢气的质量为_____;
(2)计算合金中锌的质量_____;(写出计算过程)
(3)计算合金中铜的质量分数_____;(写出计算过程,精确到0.1%);
(4)计算盐酸中溶质的质量分数_____。(写出计算过程,精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘是人体必需的微量元素之一。下图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。下列说法错误的是
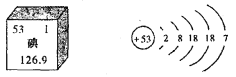
A.碘的相对原子质量为126.9,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘元素属于非金属元素,碘原子在化学反应中易得电子
D.碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为一1价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2;猜想2.CO和H2O。
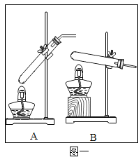
【设计实验】20℃时,甲酸的状态为______;从图一装置中选择合适的装置______(填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。
【实验预测】若猜想l成立,则D中的实验现象应为______。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为______,甲酸分解的化学方程式为______。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com