
【题目】二氧化硫(SO2)在通常情况下是一种无色、有刺激性气味的有毒气体,是造成酸雨的原因之一,它能与氢氧化钠溶液反应生成盐和水。实验室可用亚硫酸钠(Na2SO3)及硫酸制取二氧化硫,某实验小组的同学欲利用下列装置和药品制取二氧化硫,并对二氧化硫与水在通常情况下能否发生化学反应进行实验探究,设计的探究过程如下,请回答有关问题。

(1)A装置中分液漏斗也可用长颈漏斗代替,与长颈漏斗相比,分液漏斗的好处是_____:
(2)写一个实验室用A装置制取密度小于空气的气体化学方程式_____.
(3)I假设:二氧化硫与水在通常情况下能发生化学反应,生成物是一种酸性物质。
Ⅱ设计方案:先验证水能否使蓝色石蕊试纸变色;再验证二氧化硫气体能否使干燥的蓝色石蕊试纸变色;最后验证二氧化硫气体能否使湿润的蓝色石蕊试纸变色。
Ⅲ查阅资料:a.二氧化硫易溶于水;酸能使湿润的蓝色石蕊试纸变红;二氧化硫能被浓硫酸干燥
Ⅳ进行实验:
①请补全B装置中导管位置。_____
②实验过程中,装置C内石蕊试纸的颜色始终没有变化,这说明什么?_____
③装置D中胶头滴管中的蒸馏水在二氧化硫气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有二氧化硫气体通过时发现湿润的蓝色石蕊试纸变红,此现象说明什么?_____
④请写出装置E的作用_____
V结论:原假设_____(填“成立“或“不成立)。
(4)某食用碱的主要成分是碳酸钠,其中含少量氯化钠。向盛有6g食用碱的烧杯内加入足量的水,搅拌后加入过量的氯化钙,充分反应后过滤得到滤渣5.0g。请计算该食用碱中氯化钠的质量分数是多少?_____(计算结果精确至0.1%)
【答案】便于控制反应速率 Zn+H2SO4=ZnSO4+H2↑ 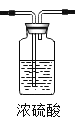 二氧化硫不能使石蕊变色 二氧化硫与水反应生成酸性物质使石蕊变色 尾气处理,防止二氧化硫逸散到空气中导致大气污染 成立 11.7%
二氧化硫不能使石蕊变色 二氧化硫与水反应生成酸性物质使石蕊变色 尾气处理,防止二氧化硫逸散到空气中导致大气污染 成立 11.7%
【解析】
(1)A装置中分液漏斗也可用长颈漏斗代替,与长颈漏斗相比,分液漏斗的好处是:便于控制反应速率;
(2)装置A属于固液混合常温型发生装置,适宜用锌与稀硫酸反应制取氢气,反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(3)①实验室用亚硫酸钠(Na2SO3)及硫酸制取二氧化硫,所得二氧化硫气体是湿润的,需经过浓硫酸进行干燥,故气体应通入浓硫酸,因此二氧化硫气体应“长进短出”,故B装置中导管位置如图: ;
;
②实验过程中,装置C内干燥的石蕊试纸的颜色始终没有变化,这说明:二氧化硫不能使石蕊变色;
③装置D中胶头滴管中的蒸馏水在二氧化硫气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有二氧化硫气体通过时发现湿润的蓝色石蕊试纸变红,此现象说明:二氧化硫与水反应生成酸性物质使石蕊变色;
④装置E中呈碱性的装氢氧化钠溶液,能够与酸性物质反应,而二氧化硫与水反应生成酸性物质,故装置E的作用是:尾气处理,防止二氧化硫逸散到空气中导致大气污染;
V结论:原假设成立;
(4![]() 设要生成5g沉淀需要碳酸钠质量为x。
设要生成5g沉淀需要碳酸钠质量为x。
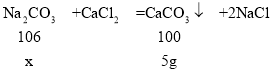
![]()
x=5.3g
所含氯化钠的质量=6g-5.3g=0.7g
该食用碱中氯化钠的质量分数=![]() ×100%=11.7%。
×100%=11.7%。


科目:初中化学 来源: 题型:
【题目】碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为 Fe2O3、SiO2 等)为原料制备碳酸亚铁的生产流程示意图:
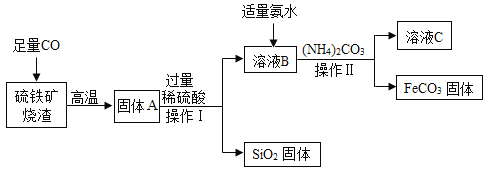
[资料]40℃以上时,(NH4)2CO3 易分解
(1)操作 I 所用到的玻璃仪器有烧杯、玻璃棒和 _____。
(2)加入(NH4)2CO3 后,该反应必须控制的条件是 _____。
(3)从溶液 C 中可回收一种化工产品——(NH4)2SO4,请写出它的一种用途: _____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】试管实验节约药品操作简便现象明显,是课堂教学中研究物质性质与变化的重要方法与手段。下列是初中化学中常见的几组实验:
(1)分别取少量氧化铁粉末和一根生锈铁钉于A、B两支试管中,分别加入等质量的稀盐酸并在酒精灯上微热,观察到两试管中溶液均变黄色,而B试管中还有大量气泡产生。两试管中均发生反应的方程式为_____________,B试管中所得溶液的溶质成分是_____________,一段时间后A试管没有明显变化,B试管中溶液颜色变成浅绿色,这可能是____________之间发生了进一步的反应。
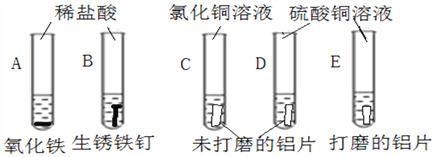
(2)将两片大小、形状相同的未打磨的铝片分别放入C、D两试管中,再分别倒入氯化铜溶液和硫酸铜溶液,结果C试管中产生较多气泡和紫红色固体,D试管中一段时间内无明显现象。将反复打磨了的铝片放入E试管中,加入硫酸铜溶液中产生一些气泡和紫红色固体。对比CD两试管说明_______________会影响铝与铜盐溶液的反应。为了验证这一观点,向D试管中加入下列物质中的_____________,也产生与C试管同样现象。
A.NaCl溶液 B.Na2SO4溶液 C.KCl溶液 D.稀硫酸
对比DE两试管说明________________________会影响了铝与硫酸铜的反应。
(3)向盛有氢氧化钠溶液的G、H两支试管中分别滴入酚酞试液和氯化铁溶液,G中溶液变红色,H中出现_______________________,再分别滴入稀硫酸并充分振荡,G试管中看到____________________________时说明氢氧化钠与稀硫酸恰好完全反应,H试管中则看到____________________,此中和反应有明显现象,请再举一个有明显现象的中和反应实例_________________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~H都是初中化学常见物质。其中A、B的组成元素相同,且常温下都是无色液体;H是蓝色沉淀。X、Y都是氧化物,Y常用作食品干燥剂,Z是红色固体。它们之间有如图转化关系。根据上述信息,回答下列问题:

(1)E的化学式__________。
(2)反应①的化学方程式______________________________。
(3)反应②的化学方程式______________________________。
(4)反应⑤的化学方程式______________________________。
(5)整个转化关系中没有涉及到的基本反应类型是__________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】.X、Y、Z 三种物质的转化关系如图所示,(“→”表示反应可以一步实现)。 下列物质符合 X、Y、Z 要求的有几组( )
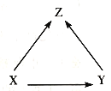
①C、CO、CO2 ②H2O2、H2O、O2 ③Fe2O3、Fe、FeSO4 ④Na2CO3、NaOH、NaCl
A.1 组B.2 组C.3 组D.4 组
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料应用广泛。
(1)生铁和钢是两种常见的铁合金,它们性能差异的主要原因是_____不同。
(2)铜锌合金的外观与黄金极为相似,实验室里可用稀盐酸鉴别,发生反应的化学程式为_____。
(3)下列有关金属的说法不正确的是_____。
A 镁在空气中燃烧,发出耀眼的白光,生成白色固体
B 为防止钢铁生锈,可在其表面涂油或刷漆等
C 通过相互刻画的方法,发现铜片的硬度比黄铜片大
D 金属铝比金属锌更耐腐蚀,说明锌比铝的金属活动性强
(4)用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.镁铝合金mg和足量的盐酸反应生成H20.1g,则m可能是0.8
B.常温下,将5.6g生石灰放入94.4g水中,所得溶液中溶质质量分数小于1%
C.将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为13.6g
D.将铁合金置于氧气中燃烧得到0.44g二氧化碳和29g四氧化三铁,则铁合金是钢
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】李阿姨很喜欢在网上淘宝,昨天她在网上买了一枚金戒指,比市场的价格要便宜很多,她既高兴又担心戒指是假的。于是她邀请你所在的化学兴趣小组的同学帮她测定戒指的真假。 查阅资料可知:假金(俗称黄铜,单纯从颜色、外形上看,与黄金极为相似,所以很难区分)是Zn、Cu合金,真金是Au(不考虑黄铜中的其他杂质)在托盘天平上称量这枚金戒指正好15g,将该金戒指放人烧杯中,用量筒量取75 mL稀盐酸分五次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀盐酸的体积/mL | 15 | 15 | 15 | 15 | 15 |
生成氢气的质量/g | 0. 04 | 0. 04 | 0. 04 | N | 0. 02 |
试求:
(1)由表中的数据我们可知:该金戒指为________(填“真”或“假”)
(2)N的数值为________。
(3)此金戒指中铜的质量分数是多少?_________(写出计算过程)
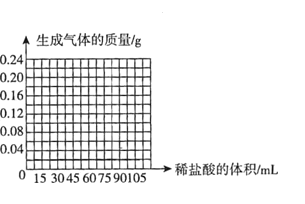
(4)请在下图中画出向这枚15g金戒指中加稀盐酸的体积与产生气体质量变化关系的示意图。______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在如图有关物质转化关系中,各物质均是初中化学常见的物质.其中A是紫红色金属,B、C组成元素相同,I是某建筑材料的主要成分,将F溶液倒入K的乳状物中搅拌后即配成农业上常用的杀菌剂波尔多液(图中反应条件已略去)
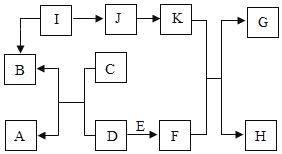
(1)I的化学式_____;
(2)由J转化为K的基本反应类型为_____.
(3)写出C与D反应的化学方程式_____;写出K与F反应的化学方程式_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com