
【题目】下列说法不正确的是( )
A.镁铝合金mg和足量的盐酸反应生成H20.1g,则m可能是0.8
B.常温下,将5.6g生石灰放入94.4g水中,所得溶液中溶质质量分数小于1%
C.将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为13.6g
D.将铁合金置于氧气中燃烧得到0.44g二氧化碳和29g四氧化三铁,则铁合金是钢
【答案】AC
【解析】
A、设生成0.1g氢气需要镁的质量为x,需要铝的质量为y

x=1.2g
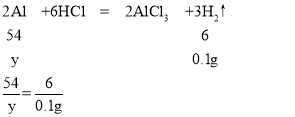
y=0.9g
所以镁铝合金mg和足量的盐酸反应生成H2O.1g,则m在0.9~1.2之间,不可能是0.8,故A不正确;
B、生石灰溶解于水会和水反应:CaO+H2O=Ca(OH)2,Ca(OH)2的溶解度曲线: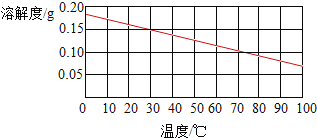
由于Ca(OH)2的溶解度很小,不会超过0.2g,所以质量分数不会大于1%,所以溶液质量分数很小;故B正确;
C、设,7.2g镁与足量氧气反应产生氧化镁的质量为x,7.2g铝与足量氧气反应产生氧化铝的质量为y;
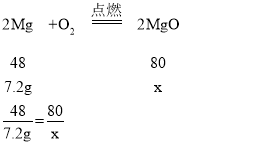
x=12g
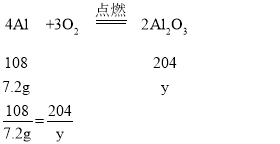
y=13.6g
由此可见,若全部为铝,则得到的氧化物质量13.6g,如果全为镁,得到的氧化物质量12g,由于是混合物,因此混合物得到的氧化物质量应介于12g与13.6g之间,故C不正确;
D、根据质量守恒定律,化学反应前后元素的质量不变,故碳元素的质量为:0.44g×![]() ×100%=0.12g,铁元素的质量为:29g×
×100%=0.12g,铁元素的质量为:29g×![]() ×100%=21g,故合金中碳元素的质量分数为:
×100%=21g,故合金中碳元素的质量分数为:![]() ×100%=0.57%,钢中的含碳量为:0.03%~2%,故属于钢,故D正确。
×100%=0.57%,钢中的含碳量为:0.03%~2%,故属于钢,故D正确。
故选:AC。


 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:初中化学 来源: 题型:
【题目】氨气是一种无色有刺激性气味的气体,密度比空气_____,是氮肥工业的重要原料。
(1)实验室常用浓氨水和氢氧化钠固体混合制取少量氨气,产生氨气的原因有:
①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,化学方程式为:_____![]() NH3↑+H2O。
NH3↑+H2O。
②氢氧化钠固体溶于水放热,使氨气在水中的_____,有利于氨气逸出。
(2)某化学兴趣小组为探究分子的运动情况,在玻璃管两端同时放入蘸有溶液的棉花,做了图1所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端。
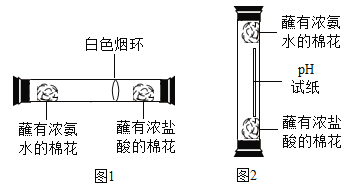
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是_____;
②写出该反应的化学方程式:_____。
(3)为了获得更好的视觉效果,该小组同学设计了图2所示实验。
(实验步骤)从玻璃管顶部将蘸有浓盐酸的棉花投入底部(过程中棉花不接触管壁),pH试纸迅速变为红色;再将蘸有浓氨水的棉花固定在玻璃管顶部,用摄像机记录实验现象。
(查阅资料)图3所示是本实验所用的pH试纸的显色范围。

(现象分析)图4所示是摄像机记录下来的pH试纸每15s的显色情况。
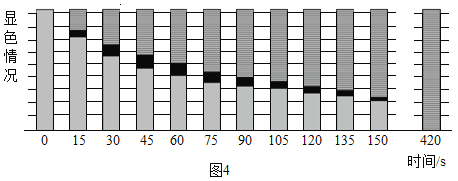
420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、_____和_____。
(拓展探究)上述实验中,若上下棉花颠倒,即玻璃管底部是蘸有浓氨水的棉花,顶部是蘸有浓盐酸的棉花,则pH试纸几乎直接变为绿色,玻璃管内迅速充满白烟,解释产生这种现象的原因:_____。
(4)氯化铵是一种常见的氮肥。某氯化铵化肥的含氮量经测定是25.2%,已知杂质不含氮元素,则此化肥中氯化铵的质量分数为_____(计算结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述正确的是( )

A. t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲
B. t2℃时,20g丙能溶解于50g水中形成70g溶液
C. 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D. t3℃时,将甲、乙、丙三种物质的饱和溶液降温到t2℃,所得溶液溶质量分数的大小关系为乙>甲>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化硫(SO2)在通常情况下是一种无色、有刺激性气味的有毒气体,是造成酸雨的原因之一,它能与氢氧化钠溶液反应生成盐和水。实验室可用亚硫酸钠(Na2SO3)及硫酸制取二氧化硫,某实验小组的同学欲利用下列装置和药品制取二氧化硫,并对二氧化硫与水在通常情况下能否发生化学反应进行实验探究,设计的探究过程如下,请回答有关问题。

(1)A装置中分液漏斗也可用长颈漏斗代替,与长颈漏斗相比,分液漏斗的好处是_____:
(2)写一个实验室用A装置制取密度小于空气的气体化学方程式_____.
(3)I假设:二氧化硫与水在通常情况下能发生化学反应,生成物是一种酸性物质。
Ⅱ设计方案:先验证水能否使蓝色石蕊试纸变色;再验证二氧化硫气体能否使干燥的蓝色石蕊试纸变色;最后验证二氧化硫气体能否使湿润的蓝色石蕊试纸变色。
Ⅲ查阅资料:a.二氧化硫易溶于水;酸能使湿润的蓝色石蕊试纸变红;二氧化硫能被浓硫酸干燥
Ⅳ进行实验:
①请补全B装置中导管位置。_____
②实验过程中,装置C内石蕊试纸的颜色始终没有变化,这说明什么?_____
③装置D中胶头滴管中的蒸馏水在二氧化硫气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有二氧化硫气体通过时发现湿润的蓝色石蕊试纸变红,此现象说明什么?_____
④请写出装置E的作用_____
V结论:原假设_____(填“成立“或“不成立)。
(4)某食用碱的主要成分是碳酸钠,其中含少量氯化钠。向盛有6g食用碱的烧杯内加入足量的水,搅拌后加入过量的氯化钙,充分反应后过滤得到滤渣5.0g。请计算该食用碱中氯化钠的质量分数是多少?_____(计算结果精确至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学中常见的不同类别的物质。它们之间的关系如图所示(“→”表示物质间的转化关系,“—”表示两端的物质间能发生化学反应)。A是使用最广泛的金属,C是常用的食品干燥剂,E是配制波尔多液的主要成分之一,其溶液为蓝色,F是由三种元素组成的化合物,请回答下列问题。
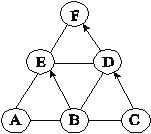
(1)B的化学式是_____。
(2)C所属的物质类别是_____。
(3)D转化为F的化学方程式是_____。
(4)A与E反应的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)为了防止水的污染,下列做法有利于保护水资源的是_____(填编号);
①抑制水中所有动、植物的生长
②不任意排放工业废水
③大量使用化肥农药
④生活污水经过净化处理后再排放
(2)自来水厂净水过程的主要操作流程如图:
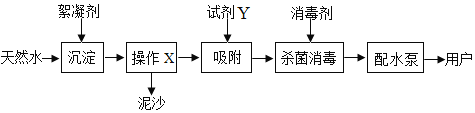
资料:常用的絮凝剂有明矾,消毒剂有液氯(Cl2)
①操作X的名称是_____,试剂Y的名称是_____。
②明矾作絮凝剂是因为明矾溶于水后生成的_____对杂质的吸附,使杂质沉降来达到净水的目的。
③Cl2与水反应生成盐酸和次氯酸(HClO),次氯酸有氧化杀毒作用,写出Cl2与水反应的化学方程式_____,HClO中Cl的化合价为_____价。
④自来水厂的净水过程_____(填“能“或“不能”)将硬水软化成软水,生活中将硬水软化的常用方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年3月22日是第二十六届“世界水日”,3月2228日是第三十一届“中国水周”。联合国确定2018年“世界水日”的宣传主题是"Nature for water”(借自然之力,护绿水青山)。我国纪念2018年“世界水日”“中国水周”活动的宣传主题为“实施国家节水行 动,建设节水型社会”。
(1)下列关于水的说法中,不正确的有_________(填序号)。
① 水是由氢元素和氧元素组成的化合物 ② 清澈、透明的泉水是纯净物
③ 合理施用农药、化肥,以减少水体污染 ④ 将活性炭放入硬水中可使其软化
⑤ 洗菜、洗衣后的水用来浇花、冲洗厕所
(2)自然界中的水一般要净化后才能使用。在吸附、过滤、蒸馏等三种净化水的操作中,能 将硬水变为软水的操作是_________。有的村民打深井取用地下水,你可以用_________帮他们检验地下水是硬水还是软水。
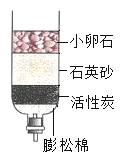
(3)根据所学的化学知识用右图所示的简易净水器净化浑浊的黄河水,其中 小卵石、石英砂的作用是_____。如果将石英砂与小卵石的位置颠倒是否可以,为什么? _________°
(4)下图表示自来水消毒过程中发生反应的微观过程:

其中属于单质的是_________(填化学式,下同),属于氧化物的是________。物质D中氯元素的化合价为_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组利用下列装置进行气体的制取,请分析并填空.
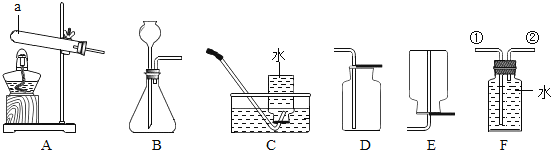
(1)写出图中仪器a的名称______;
(2)实验室用大理石和稀盐酸反应制取二氧化碳的化学方程式为______,应选择的收集装置为______(填字母);
(3)实验室用加热氯酸钾和二氧化锰混合物制取氧气,应选择发生装置为______(填字母);化学方程式为:______若用盛满水的F装置收集氧气,氧气应从导管______(填①或②)处通入F装置.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锰结核是沉淀在大洋底部的一种矿石(如图),其中含有的锰、铜、钴、镍等元素极具开发价值。锰元素的原子序数为25,自然界中存在24种锰原子,其中一种锰原子的相对原子质量为54。下列有关说法不正确的是

A.锰元素属于金属元素
B.该锰原子核外电子数为54
C.锰元素原子核内质子数为25
D.该锰原子核内有29个中子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com