
科目:初中化学 来源:不详 题型:实验题

| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加_____ | 产生大量的气泡 | 猜想②正确 |
| 把产生的气体通入 | | 相关的化学方程式是: |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去氧化钙中碳酸钙 | 加水溶解过滤蒸发 |
| B | 测定溶液的酸碱度 | 紫色石蕊试液 |
| C | 软化硬水 | 煮沸 |
| D | 验证镁铜银的金属活动性 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
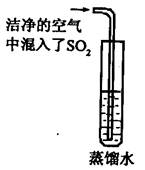
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| | 实验目的 | 实验方案 | |
| 实验 | 实验 | ||
| A | 研究温度对反应剧烈程度的影响 |  |  |
| B | 研究CO2气体是否与水发生反应 |  |  |
| C | 研究SO2是否能形成酸雨 |  |  |
| D | 研究白磷燃烧是否需要O2 |  |  |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
 ,该反应可用于焊接铁轨。某小组取铝粉和氧化铁的混合物,使之充分反应,反应中放出大量的热并发出耀眼的光芒,同时有熔融物生成。该小组对所得熔融物的成分进行了探究。
,该反应可用于焊接铁轨。某小组取铝粉和氧化铁的混合物,使之充分反应,反应中放出大量的热并发出耀眼的光芒,同时有熔融物生成。该小组对所得熔融物的成分进行了探究。
| 步骤 | 现象 | 结论 |
| 取少量的熔融物于试管中,加入过量的 。 | 固体全部溶解,有无色气体逸出, 。 | 熔融物含有铁和铝 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 |
| ① 将几粒白色固体颗粒放在表面皿上,放置一会儿 | |
| ② 将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 | |
| ③ 向操作②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
| 实验操作 | 实验现象 |
①按照下图安装两套装置 | |
| ②向两套装置的试管1中分别依次加入银灰色粉末和稀盐酸、银灰色粉末和 | 都产生无色气体,试管1外壁温度明显升高 |
| ③待导管口有气泡均匀持续冒出时,收集一试管气体,验纯(两套装置操作相同) | 验纯时的操作和现象: |
| ④在导管口点燃气体(两套装置操作相同) | 都产生淡蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com