
【题目】某化学实验室从含少量硝酸锌的硝酸银废液中提取贵金属Ag,其主要操作流程如图所示:
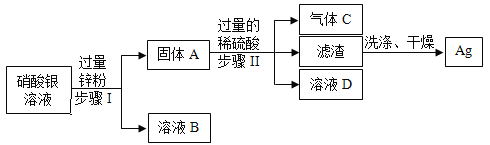
(1)固体A的成分有________________(填化学式)。
(2)写出步骤I中发生反应的化学方程式:_________________。
(3)若往溶液D中加入适量某种物质后,可得到只含一种溶质的溶液,则加入的物质可能是_________________。
科目:初中化学 来源: 题型:
【题目】某实验小组的同学为了测定CaCl2和NaCl的混合物中CaCl2的含量,他们取样品25.8g于烧杯中,加入134.2g水全部溶解,再多次加入某Na2CO3溶液充分反应。加入Na2CO3溶液 与产生沉淀的质量如下表所示:
Na2CO3溶液/g | 10 | 10 | 10 | 10 | 10 | 10 |
沉淀质量/g | 5 | 10 | 15 | 20 | 20 | m |
(1)Na2CO3中钠、碳、氧三种元素的质量比为_____,表中m=_____。
(2)样品中CaCl2的质量是____;恰好完全反应时,所得溶液中溶质的质量分数是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组利用废烧碱(含少量Na2CO3、NaCl、MgCl2、CaCl2等)制Na2CO3·10H2O。
【制取流程】
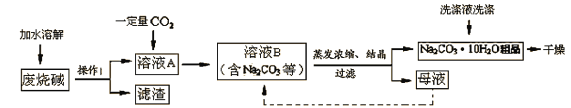
【相关资料】①Na2CO3+H2O+CO2=2NaHCO3
②2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
③在NaHCO3溶液中加入BaCl2溶液,可发生反应:2NaHCO3+BaCl2=BaCO3↓+2NaCl+ H2O+CO2↑
④碳酸钠的饱和溶液在不同温度下析出的晶体如下图所示:
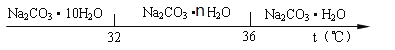
【问题讨论】
(1)滤渣主要成分为Mg(OH)2和 ,产生Mg(OH)2的化学方程式 。
(2)操作Ⅰ需使用的玻璃仪器有:烧杯、 和玻璃棒。
(3)取少量溶液B,加入BaCl2溶液,充分混合,若观察到 (填现象),则溶液B中含NaHCO3。
(4)结晶后,过滤时的温度须低于 ℃。
(5)“母液”不能沿流程中虚线路径循环使用,原因是 (选填序号)。
①“母液”不含Na2CO3
②“母液”多次循环后,NaCl含量增加
【组成确定】
(6)取少量粗产品,加水溶解,加足量 (选填数字序号,下同),充分搅拌,再加少量 ,无沉淀,证明其中不含NaCl。
①AgNO3溶液 ②稀盐酸 ③稀硝酸
(7)兴趣小组同学取32.8g干燥粗产品,用如图所示装置(夹持仪器省略)进行实验:
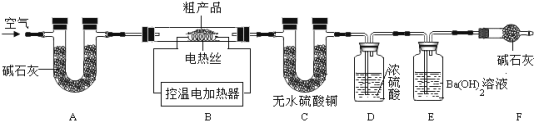
查阅资料1:Na2CO3·10H2O加热至32℃,开始分解失水,充分加热可完全失水;NaHCO350℃时开始分解270℃时完全分解;Na2CO3受热不分解。
查阅资料2:Ba(OH)2溶液能吸收CO2:Ba(OH)2+CO2=BaCO3↓+H2O
①实验前要先 ,再装入粗产品;
装置A的作用是 。
②粗产品加热至270℃,据 (填装置编号及现象),可知粗产品中含NaHCO3。测得C、D共增加m1,E质量增加m2,则m1∶m2 (填“>”、“=”或“<”)9∶22。
实验测得m2=1.1g,则可推算32.8g粗产品中含有NaHCO3的质量为 g。
③当加热至36℃时,测得B中剩余固体27.4g,则该剩余固体是 (填化学式)和NaHCO3的混合物。(此空2分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学实验室从含少量硝酸锌的硝酸银废液中提取贵金属Ag,其主要操作流程如图所示:
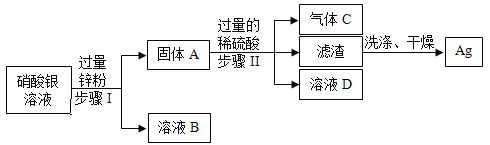
(1)固体A的成分有________________(填化学式)。
(2)写出步骤I中发生反应的化学方程式:_________________。
(3)若往溶液D中加入适量某种物质后,可得到只含一种溶质的溶液,则加入的物质可能是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几种常见微粒结构示意图和元素周期表部分信息。

(1)图中属于金属元素的是_____ (填序号)。
(2)A、B中属于离子结构的是_____ (填序号)。
(3)B元素与D元素形成化合物的化学式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家正致力于将二氧化碳转化为甲烷,其反应的微观示意图如下。下列叙述不正确的是

A. 化学反应前后原子种类不变
B. 丙的化学式H2O
C. 丁的相对分子质量为16
D. 参加反应的乙与生成的丁分子个数比为1︰2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酱油在使用及储藏过程中颜色会变深,逐渐降低品质。实验小组通过实验研究温度、氧气、光照3个因素对酱油颜色的影响。
(查阅资料)① 通过色差仪检测L*值可监控酱油颜色变化,酱油颜色越深,L*值越小。
② 保鲜瓶具有的特点是挤出盛放的物质后,空气不会进入。
(实验准备)
将等量样品(同品牌、同批次、初始L*值为43.82的酱油)分装到500 mL的不同容器中,密封。
(进行实验)
实验1:将装有样品的多个透明玻璃瓶置于不同温度的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。
编号 | 温度 | 15天 | 30天 | 45天 |
1-1 | 5 ℃ | 43.77 | 43.53 | 42.91 |
1-2 | 28 ℃ | 43.71 | 43.19 | 42.85 |
1-3 | 45 ℃ | 43.67 | 42.55 | 40.89 |
实验2:将装有样品的两个容器置于28 ℃的恒温箱中。每15天,分别倒出100 mL酱油,剩余样品放回恒温箱。用色差仪检测倒出样品的L*值,结果如下。
编号 | 容器 | 15天 | 30天 | 45天 |
2-1 | 透明玻璃瓶 | 43.45 | 42.36 | 41.30 |
2-2 | 透明保鲜瓶 | 43.72 | 42.98 | 42.53 |
实验3:将装有样品的多个容器置于28 ℃的恒温箱中。每15天,分别取出未开封样品,用色差仪检测L*值,结果如下。

(解释与结论)
(1)实验1得出的结论是_____。
(2)实验2的目的是_____。
(3)实验3欲研究光照对酱油颜色的影响,应选用的容器是_____。
(4)家庭常使用透明玻璃瓶盛放酱油。解释“在相同时间内,使用过的酱油比未开封的酱油颜色深”可依据的实验是_____(填编号)。
(反思与评价)
(5)结合本实验,你对使用或储藏酱油的建议是_____。
(6)酱油在酿造过程中,有时会产生过量的铵盐(如NH4Cl)影响酱油的口感。可用碳酸钠除去铵盐,原理如下,补全该反应的化学方程式。Na2CO3 + 2NH4Cl === 2NaCl + 2NH3↑ + H2O +_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水与溶液在生产生活中有广泛的用途。请结合所学知识回答下列问题:
(1)因春节期间突发“ 疫情”,小明爸爸在超市购买了一些应急食品, 有自热米饭和瓶装山泉水等
①“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应生成氢氧化钙,放出大量的热,该反应的化学方程式为_______________________。
②小明若要检测瓶装山泉水是否为软水,可取水样后向其中加入___________,生活中,常可采用________的方法来降低水的硬度。
(2)如图为实验室电解水的装置,通电一段时间后,与电源负极相连的一端玻璃管中产生的气体是___________,涉及的化学反应方程式是____________ ; 该反应的基本类型是_______________。
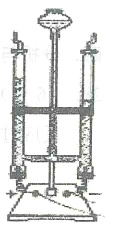
(3)每年的3月22日为“世界水日”,今年我国将3月22-28日定为“中国水周”,为纪念以上活动,2020 年我国将活动主题定为“坚持节水优先,建设幸福河湖”。请列举生活中节约用水的方法____________ (答一条即可) 。
(4)如图是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
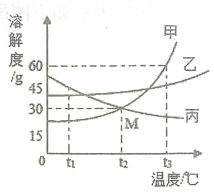
①M点表示的含义是_______________(答一条即可)。
②将丙物质的不饱和溶液变为饱和溶液的方法是___________________ (答一条即可)。
③t3°C时,将40g甲物质加入到50g水中,充分溶解后所得溶液的质量是________________g。
④t3°C时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t2°C,所得溶液中溶剂最多是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种固体物质的溶解度曲线如图所示。
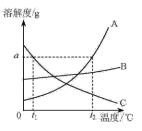
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_______。
(2)t2℃时,完全溶解a gA物质最少需要水的质量是_______g。
(3)一定能使B的不饱和溶液变成饱和溶液的方法是_______。
(4)t2℃时,A的饱和溶液中含有少量B,提纯A的方法是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com