
【题目】现有A~F六种稀溶液,分别是碳酸钠溶液、氢氧化钠溶液、氢氧化钙溶液、稀盐酸、氯化钠溶液、酚酞溶液中的一种,把他们两两混合,其部分现象如下表所示。
B | C | D | E | |
A | 无明显变化 | 白色沉淀 | 无明显变化 | 液体变红色 |
B | 气体逸出 | 无明显变化 | 无明显变化 |
(1)①B、E中的溶液分别是______、______。
②A与C中发生反应的化学方程式为______。
(2)对还没有确定的稀溶液,下列鉴别方法中错误的是______(填序号)。
①分别蒸发溶剂 ②分别滴加适量水 ③分别滴加FeCl3溶液 ④分别测定pH ⑤分别通入CO2后,再滴加稀盐酸
(3)相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸相混合后,滴加紫色石蕊溶液,溶液呈______色。
【答案】氯化氢(HCl) 酚酞 Na2CO3+ Ca(OH)2= CaCO3↓+2NaOH ①② 红
【解析】
碳酸钠溶液、氢氧化钠溶液、氢氧化钙溶液、稀盐酸、氯化钠溶液、酚酞溶液中两两混合,可知碳酸钠和氢氧化钙混合后生成白色碳酸钙沉淀,碳酸钠和稀盐酸混合后有二氧化碳气体生成,碳酸钠、氢氧化钠、氢氧化钙三种溶液都能使酚酞试液变红,稀盐酸和氢氧化钠混合发生中和反应,但是无明显现象, 氯化钠分别和其它五种物质混合都没有明显现象,据此根据题表中AC混合有沉淀生成,说明AC是碳酸钠和氢氧化钙两种物质,AE混合液体变红说明E是酚酞溶液;BC混合有气体生成说明C是碳酸钠,则B是稀盐酸、A是氢氧化钠;不能确定的是氢氧化钠溶液和氯化钠溶液;
(1)
①由上分析可知B中溶质是氯化氢,故填氯化氢(HCl);E中溶质是酚酞,故填酚酞;
②由上分析可知A与C的反应是氢氧化钙溶液和碳酸钠溶液反应,生成碳酸钙沉淀和氢氧化钠,方程式故填Na2CO3+ Ca(OH)2= CaCO3↓+2NaOH;
(2)由上分析可知,不能确定的是氢氧化钠溶液和氯化钠溶液,
①分别蒸发溶剂,氯化钠和氢氧化钠都有白色固体析出,不能确定;
②分别滴加适量水,两种溶液无明显现象,不能确定;
③分别滴加FeCl3溶液,氢氧化钠和氯化铁反应生成红褐色氢氧化铁沉淀,氯化钠和氯化铁不能反应,可以确定;
④分别测定pH,氢氧化钠溶液显碱性,pH值大于7,氯化钠溶液显中性,pH值等于7,可以确定;
⑤分别通入CO2后,再滴加稀盐酸,氢氧化钠和二氧化碳反应生成碳酸钠,碳酸钠和盐酸反应有二氧化碳气体生成,氯化钠则无明显现象,可以确定,符合题意的故填①②;
(3)根据氢氧化钾和氯化氢反应的返学方程式可知,二者反应的质量比是56∶35.5,
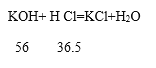
则相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸相混合后,反应后盐酸有剩余,溶液显酸性,能使紫色石蕊溶液变红色,故填红。


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:初中化学 来源: 题型:
【题目】按要求填空:
(1)地壳中含量最多的金属元素是_____(填化学符号)
(2)空气中含量最多的物质_____(填化学符号)
(3)2 个氧分子_____(填化学符号)
(4)+3 价的 Al 元素_____(填化学符号)
(5)饼干在空气中放久了变软,说明空气中含有_____(填化学符号)
(6)保持氧气化学性质的最小微粒是_____(填名称)
(7)二氧化碳的式量_____(相对原子质量:C﹣12,O﹣16)
(8)3OH-表示的意义_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为①KNO3 ②NaCl ③H3BO3 的溶解度曲线,下列说法错误的是
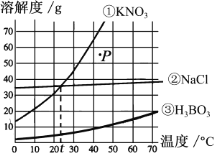
A. 在 10 ℃时,三种物质溶解度的大小顺序为②>①>③
B. 在 t ℃时,三种物质饱和溶液中溶质质量分数的大小顺序为①=②>③
C. 将 P 点处的 KNO3 溶液蒸发适量水可变成饱和溶液
D. 将 P 点处的 KNO3 溶液降温一定会析出 KNO3 晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物质按照甲、乙、丙的顺序符合要求的是
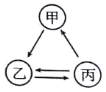
A. C、CO2、COB. H2O2、H2O、O2
C. CuCl2、Cu、CuOD. KOH、K2SO4、KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠是日常生活的必需品,也是重要的化工原料,海水“晒盐”得到的是粗盐。粗盐除含NaCl 外,还含有少量 MgCl2、CaCl2、Na2SO4以及泥沙等杂质
(1)有关粗盐提纯的实验操作合理的是___(填序号)。
A 溶解前用玻璃棒研磨大颗粒粗盐
B 过滤时液体的液面要低于滤纸边缘
C 蒸发时要不断搅拌直至水分全部蒸干
D 实验结束用玻璃棒把固体转移到纸上,称量后,回收到指定容器中
(2)粗盐进行精制,流程如图。

温合液Ⅲ经过“过滤”操作,得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___(填化学式)
(3)加入过量的NaOH溶液的目的为___(用化学方程式表示)。
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。甲和乙反应生成丙和丁的化学方程式用下列微观示意图表示:
物质 | 甲 | 乙 | 丙 | 丁 |
|
微观 示意图 |
| ||||
①请写出丙物质的化学式_____;下列属于丁物质的微观示意图的是_____。

②能保持甲化学性质的微粒是_____(填“分子”或“原子”),四种物质中属于氧化物的有_____(填甲、乙、丙、丁)。
③从上述反应重能获得的信息有_____(填一条即可)。
④上述微观示意图表示的化学方程式是:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种重要的化工产品,可用来改善地表水质、治理赤潮,过氧化钙产品中常含有氧化钙杂质,以下是某学习小组为测定过氧化钙产品纯度设计的实验,实验装置如图;已知:CaO2是一种白色粉末,微溶于水,易溶于稀盐酸,且发生反应: CaO2+2HCl=CaCl2+H2O2

实验步骤:实验前称取产品及二氧化锰共12克,先缓慢通入氮气,一段时间后,加热铜网至红热,再缓慢滴入过量稀盐酸,直至A中样品完全反应。继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止通入氮气,将锥形瓶中的剩余物过滤,洗涤,干燥,得到滤渣2.0克。回答下列问题,
(1)二氧化锰与稀盐酸不反应,A中二氧化锰的作用是______________
(2)样品完全反应后,继续缓慢通入氮气的目的是______________
(3)装置B的作用有,除去气体中的水蒸气、______________
(4)实验测得C装置中铜网增重1.8克,该产品中过氧化钙的质量分数为_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是初中化学的一些基本实验,请根据实验内容回答下列问题.

(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的,可能的原因是 (填一条即可)。
(2)放置一周后,B实验观察到的现象是 。
(3)C实验产生氧气与氢气的体积比约为 。
(4)D实验观察到的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com