
【题目】人类的生产、生活离不开金属材料。
(1)高铁的建成使人们的出行将更加方便快捷。请用所学化学知识回答下列问题:
①高铁列车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈的原理是_____。
②高铁隧道施工中常用氢氧化镁固体作为阻燃剂,其受热分解成水蒸气和耐高温的氧化镁粉末,用氢氧化镁灭火的原理是_______。
③铝热剂是修建铁路时常用的焊接材料,铝热剂在焊接时发生的反应为2Al+X![]() 2Fe+Al2O3则X的化学式为______,此反应的基本反应类型是_____。
2Fe+Al2O3则X的化学式为______,此反应的基本反应类型是_____。
(2)某化学小组用一定量的AgNO3和Zn(NO3)2的混合溶液进行了如图所示的实验。
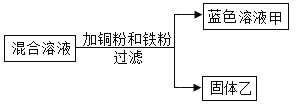
①向固体乙中滴加稀盐酸,_____(填“有”或“没有”)气泡产生。
②蓝色溶液甲中一定含有的溶质除Cu(NO3)2外,还有_____。
【答案】隔绝氧气和水 降温至可燃物的着火点以下(或隔绝空气) Fe2O3 置换反应 没有 Zn(NO3)2、Fe(NO3)2
【解析】
(1)①铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,车身表面喷漆主要是为了防止外壳生锈,其原理是隔绝水和氧气(或空气);
②灭火是阻断燃烧的条件,氢氧化镁发生分解,吸收燃烧物表面的热量,释放出大量水分,水蒸发吸收燃烧物表面的热量降温至可燃物的着火点以下,分解出的氧化镁覆盖在可燃物表面,阻止燃烧的进行;
③反应前后,原子的种类与数目不变,反应前:2个铝原子;反应后:2个铁原子、2个铝原子和3个氧原子,所以每个X分子中含有2个铁原子和3个氧原子,则X的化学式为Fe2O3;由于该反应的反应物生成物均是一种单质和一种化合物,所以该反应是置换反应;
(2)分析实验过程,结合金属活动性的有关知识判断:溶液甲呈蓝色,其中一定含有Cu(NO3)2,那么固体乙中一定没有铁粉,乙中一定含有金属银,还可能含有金属铜,甲中一定还含有Fe(NO3)2、Zn(NO3)2;所以①向乙中滴加盐酸时没有气泡产生;②甲中一定含有的溶质为Zn(NO3)2、Fe(NO3)2、Cu(NO3)2。


 53天天练系列答案
53天天练系列答案科目:初中化学 来源: 题型:
【题目】实验探究:小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
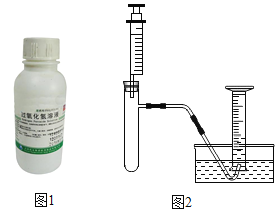
I.小林准备用如图2所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气,记录2分钟收集的气体体积。
(1)请写出过氧化氢分解的化学方程式:,_____
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,_____,说明生成的气体是氧气。
Ⅱ.小林查阅了相关资料,并进行了探究实验
(查阅资料)(1).过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
(2).温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 分两次进行实验,均注入5mL过氧化氢溶液 第一次在常温下进行 第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为5mL | 猜想_____不成立 |
② | 分两次进行实验 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液 第二次_____ | 第一次,量筒中2分钟收集到的气体体积为56mL 第二次,量筒中2分钟收集到的气体体积为5mL | 猜想_____成立 |
(实验反思)
小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶 | 不加过氧化氢酶 | |||||
反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
收集到气体体积/mL | 39 | 56 | 60 | 5 | 5 | 5 |
通过这些数据,你能得出的新结论是_____。
要证明某物质是催化剂,还需要证明的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示四个图像,分别对应四个过程,其中正确的是
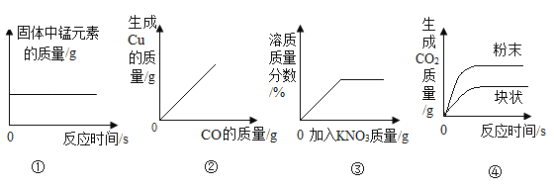
A.①加热一定量的高锰酸钾制取氧气
B.②加热条件下,一氧化碳还原一定量的氧化铜
C.③20℃,向一定量接近饱和的硝酸钾溶液中加入硝酸钾
D.④等质量碳酸钙分别与等质量、等质量分数的稀盐酸(足量)反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀覆盖有一薄层铜的绝缘板,制成印剧电路板。人们为了从废腐蚀液(含有CuCl2、FeCl2和FeCl3)中回收铜,并重新得到FeCl3溶液,设计如下实验流程。(已知:2FeCl3+Fe=3FeCl2)
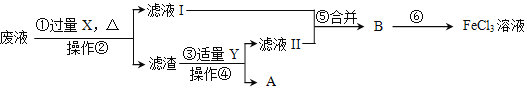
(1)操作②、④的名称是___________。
(2)上述流程中,X的化学式为________,步骤③中有关反应的化学方程式为________。
(3)在工业生产中,步骤⑥的通常做法是向B中通入氯气,而在实验室向B中滴加适量过氧化氢溶液,也可以达到相同的效果。工业完成步骤⑥的反应属于_________(填基本反应类型),实验室完成步骤⑥的化学方程式是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车制造过程中要用到各种各样的材料,如图所示。

(1)用作车门材料的玻璃钢属于__________(填序号)。
a金属材料
b合成材料
c复合材料
(2)将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度___铝的硬度(填“大于”或“小于”)。
(3)车体表面喷漆不仅美观,而且可有效防止钢铁与_______接触而生锈。
(4)汽车电路中的导线大都是铜芯的,这主要是利用了铜的_______性。将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合高温焙烧可得到铜,同时还产生一种可形成酸雨的气体,该反应的化学方程式为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】《鲁滨逊漂流记》中的主人公在荒岛采用下图方法将海水淡化。
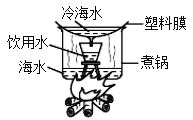
(1)海水经蒸发、冷凝变为饮用水,发生了_____________ (填“物理”或“化学”)变化。
(2)从微观角度分析上述过程,下列说法正确的是_____________(填序号)。
A 蒸发时水分子体积变大
B 冷凝时水分子质量减小
C 蒸发时水分子运动速率加快
D 冷凝时水分子间隔减小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属与我们生活息息相关。
(1)铸造硬币不需要考虑金属的_____ (填字母序号)。
A 硬度
B 抗腐蚀性
C 导电性
(2)铁制品锈蚀的过程,实际上是铁与空气中的__(填化学式)、水蒸气等发生化学反应的过程;铁锈的主要成分为___(填化学式)。
(3)写出氧化铁与一氧化碳在高温条件下发生反应的化学方程式_____。
(4)某钢铁厂每天需消耗5000t含Fe3O4 76%的磁铁矿石,该厂理论上可日产含Fe98%的生铁的质量是___t (结果精确到0.1)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学符号表示
①2个氮分子:______ ②3个钾离子:______ ③碳铵:______
(2)如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子。写出符合该微观示意图的一个具体反应的化学方程式___________________。
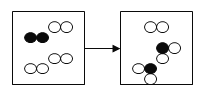
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。
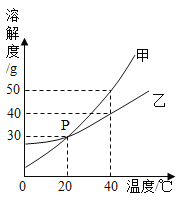
(1)图中P点的含义是_____。
(2)40℃时,饱和溶液中溶质的质量分数:甲_____乙(填“>”、“=”或“<”)。20℃时,将50 g乙物质放入100 g水中,所得溶液中,溶解的溶质与溶剂的质量比为_____(用最简整数比表示)。
(3)20℃时,进行了如下图所示的实验:
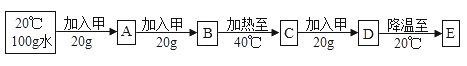
上述实验过程中所得的溶液,属于不饱和溶液的是_____,_____溶液与B溶液中溶质的质量分数相同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com