
A、 用肥皂洗涤衣物 |
B、 小食品包装中填充氮气 |
C、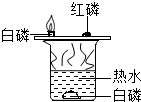 热水中的白磷 |
D、 浓硫酸脱水实验 |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A、①②③④ | B、⑤⑥⑦⑧ |
| C、①④⑤⑧ | D、②③⑥⑦ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 合金的质量 | 烧杯和混合物的质量 |
| 150g | 100g | 249.6g | |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是关于分子性质的实验:
如图是关于分子性质的实验:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com