
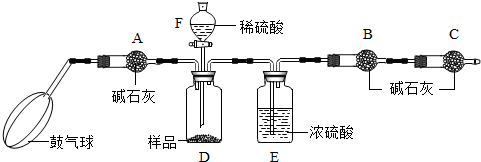
分析 要测定碳酸钠的含量,可以通过与酸反应生成的二氧化碳的质量进行求算,而要测定二氧化碳的质量,需排除空气中二氧化碳和水蒸气对生成的二氧化碳的质量的影响,除去二氧化碳使用的是氢氧化钠溶液,除去水使用的是浓硫酸.
解答 解:(1)干燥管A可以吸收鼓气球中鼓入的空气中的二氧化碳,避免对干燥管B的质量增加造成干扰;干燥管Ⅱ在干燥管I之后,能阻止空气中的二氧化碳和水进入干燥管,E中盛有的是浓硫酸,具有吸水性,能将水分吸除,排除水分对生成二氧化碳质量的影响;步骤③中鼓气的目的是用除去二氧化碳的空气赶走体系中的二氧化碳,步骤⑥鼓入空气是利用压力差使产生的二氧化碳全部被排出,要测定二氧化碳的质量,需排除空气中二氧化碳对生成的二氧化碳的质量的影响;本实验不能同时省略③、⑥两个步骤,否则会给实验带来误差;
(2)当5克样品全部为碳酸钠时,耗硫酸最多,设所需硫酸的质量为x
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 98
5g x
$\frac{106}{5g}$=$\frac{98}{x}$
x=4.6(g)
故至少要盛放10%的稀硫酸(密度为1.07g/mL)的体积为:V=$\frac{\frac{4.6g}{10%}}{1.07g/mL}$≈43.0(ml)
根据所测数据,生成二氧化碳的质量为(m2-m1)=1.98g,设碳酸钠的质量为Y,则有
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 44
y 1.98g
$\frac{106}{y}$=$\frac{44}{1.98g}$
x=4.77(g)
所以纯碱样品纯度为:$\frac{4.77g}{5g}$×100%=95.4%.
故答案为:(1)除去鼓入空气中的二氧化碳,防止空气中的二氧化碳和水进入B中影响实验结果,防止D中的水蒸气进入B中,用除去二氧化碳的空气赶走体系中的二氧化碳,用除去二氧化碳的空气将反应产生的二氧化碳 全部赶入B中,不能,①空气中含少量二氧化碳、②反应后装置中残留二氧化碳均会造成结论偏差;
(2)43.0,95.4%.
点评 本题考查了碳酸钠含量的测定,完成此题,可以依据生成的二氧化碳的质量进行求算,进行实验时,要保证生成的二氧化碳的质量准确.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
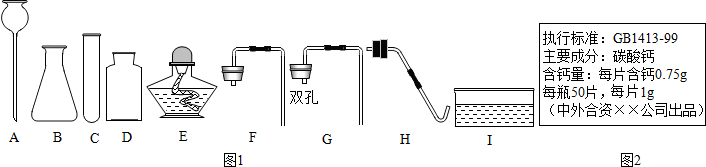
科目:初中化学 来源: 题型:解答题
| 物质的质量 | |
| 反应前:烧杯+盐酸 | 50g |
| 10片钙片 | 10g |
| 反应后:烧杯+剩余物 | 56.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 配制溶液时,搅拌溶液可以增大溶质的溶解度 | |
| B. | 溶液加水稀释前后溶质的质量不变 | |
| C. | 盐酸是氯化氢气体的水溶液,根据气体溶解度变化规律,贮存时要阴凉密封 | |
| D. | 汗水浸湿的衣服晾干后出现白色斑迹,是因为水分蒸发后盐分结晶析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
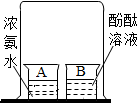 在前两章化学学习后,我们亲身体验了分子探究实验,感受到了化学的无穷魅力.
在前两章化学学习后,我们亲身体验了分子探究实验,感受到了化学的无穷魅力.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
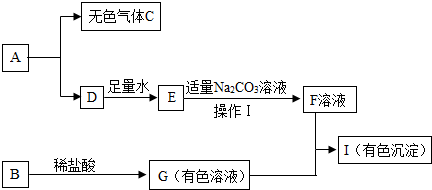
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com