
| ���ʵ����� | |
| ��Ӧǰ���ձ�+���� | 50g |
| 10Ƭ��Ƭ | 10g |
| ��Ӧ���ձ�+ʣ���� | 56.7g |
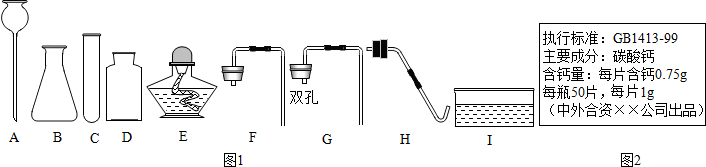
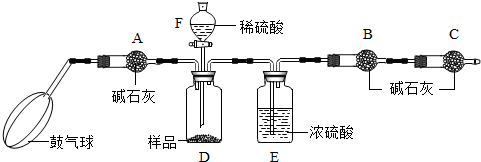
���� ��1������ʵ��������ȡ������̼�ķ�����ѡ��
��2��������̼���Ʒ�ĩ��ϡ��������ȡ������̼�������Ʒ�Ӧ���ʣ�ѡ��������
��3������ʵ��������ȡ������ԭ����������
��4�������ݷ�Ӧǰ�����ʵ����������������ɶ�����̼��������
�����ݶ�����̼����������̼��ƺ����ᷴӦ�ķ���ʽ�������̼��Ƶ�������
������̼��Ƶ������Լ�̼����иƵ������������������Ԫ�ص�������
��� �⣺
��1��ʵ������ȡCO2�����ڳ�����ʯ��ʯ�����ʯ��ȡ�ģ���̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼����˲���Ҫ���ȣ�������̼��һ���ܶȱȿ�����������ˮ�������������ſ������ռ�����ѡ��ABGD����Ӧ�Ļ�ѧ����ʽ��CaCO3+2HCl=CaCl2+H2O+CO2����
��2����Һ©����ע�����ܹ�����Һ��ĵμ����ʣ�
��3�������п����ϡ�����������Ͳ���Ҫ���ȣ�
��4�������ɶ�����̼���������Ϊ��50g+10g-56.7g=3.3g��
����10Ƭ��Ƭ��̼��Ƶ�����Ϊx��
CaCO3+2HCl=CaCl2+H2O+CO2��
100 �� 44
x 3.3g
$\frac{100}{x}=\frac{44}{3.3g}$
x=7.5g��
���ÿƬ�˸�Ƭ��̼��Ƶ�����$\frac{7.5g}{10}$=0.75g
����ÿƬ�˸�Ƭ�ĺ�����Ϊ0.75g��$\frac{40}{40+12+16��3}$100%=0.3g��
��ΪÿƬ��Ƭ�еĺ���Ԫ�ص�����Ϊ0.3g�����Գ���Ӧ�ðѱ�ǩ�еĺ�������Ϊ����������ÿƬ����0.3g��
�𰸣�
��1��ABGD ʯ��ʯ��ϡ���� ʯ��ʯ��ϡ���� CaCO3+2HCl=CaCl2+H2O+CO2����
��2����Һ©����
��3�������� п����ϡ���
��4����3.3g����ÿƬ�˸�Ƭ��̼��Ƶ�����Ϊ0.75g���ۺ�������ÿƬ����0.3g��
���� ���⿼����ʵ������ȡ������ԭ����������װ�õ�ѡ�����ڻ����Ե��ۺ��⣬������ѧ������ʵ�����֪ʶ��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѩ�ڻ� | B�� | ���������� | C�� | ʪ�·����� | D�� | ����˹��ը |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
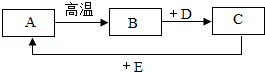
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
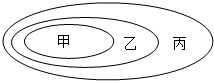 ͼ�мס��ҡ���������Բ�ֱ����ij�������ij�����ʣ������ܹ���ͼʾ��ϵ���ǣ�������
ͼ�мס��ҡ���������Բ�ֱ����ij�������ij�����ʣ������ܹ���ͼʾ��ϵ���ǣ�������| A�� | ���Ǹܸˡ����ǻ��֡����Ǽ�е | |
| B�� | ���Ƕ��ܡ��������ܡ����ǻ�е�� | |
| C�� | ���Ǽ���ǻ�������Ǵ����� | |
| D�� | ���ǻ��Ϸ�Ӧ�����ǷֽⷴӦ�������û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
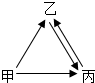 �ס��ҡ����������ʾ�����̼Ԫ�أ����ǵ��ʣ��ҡ��������Ԫ����ȫ��ͬ�����廯������о綾������֮��������ͼ��ʾ��ת����ϵ���������ʺͷ�Ӧ�����Ѿ���ȥ�������Ļ�ѧʽΪCO2���������ҵĻ�ѧ����ʽΪC+CO2$\frac{\underline{\;����\;}}{\;}$2CO��
�ס��ҡ����������ʾ�����̼Ԫ�أ����ǵ��ʣ��ҡ��������Ԫ����ȫ��ͬ�����廯������о綾������֮��������ͼ��ʾ��ת����ϵ���������ʺͷ�Ӧ�����Ѿ���ȥ�������Ļ�ѧʽΪCO2���������ҵĻ�ѧ����ʽΪC+CO2$\frac{\underline{\;����\;}}{\;}$2CO���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʱ����ζ����ѧ�仯�� | B�� | ���������ۻ�����ѧ�仯�� | ||
| C�� | �ô�����ϴ��ˮƿ��ˮ���������仯�� | D�� | ��������Ⱥ��Ϊ���������仯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com