
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 抽气次数 | 42 | 38 | 36 | 44 | 40 |
| 二氧化硫的含量 | 是否超标 |
| 64 |
| 254 |
| x |
| 6.35×10-4mg |
| 二氧化硫的含量 | 是否超标 |
| 0.04mg/m3 | (2分) 超标 |


科目:初中化学 来源: 题型:
| A、7.4g | B、11.1g |
| C、3.7g | D、14.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:
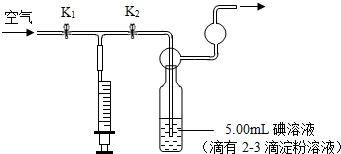
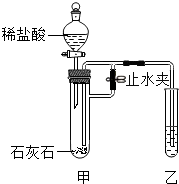 某化学小组在课外活动时利用如图装置进行实验 (图中铁架台等仪器已略去).
某化学小组在课外活动时利用如图装置进行实验 (图中铁架台等仪器已略去).查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
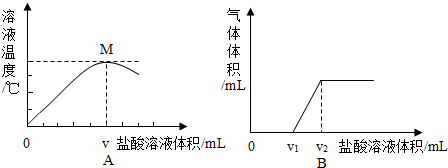
 为测定空气中氧气所占的体积分数,某同学设计了如图实验,在一个透明耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为
为测定空气中氧气所占的体积分数,某同学设计了如图实验,在一个透明耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com