
【题目】如图是探究燃烧条件的实验装置,有关该实验的说法不正确的是( ) 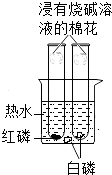
A.只有左侧试管中的红磷能燃烧
B.只有右侧试管中的白磷能燃烧
C.磷燃烧的反应属于氧化反应
D.烧碱溶液的作用是吸收燃烧产物,减轻污染
科目:初中化学 来源: 题型:
【题目】实验室部分装置如图所示,请回答下列问题. 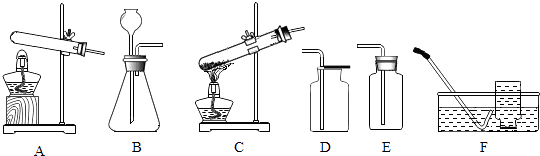
(1)请选择制取氧气的发生装置和收集装置,填写在如表中(填字母).
选用药品 | 发生装置 | 收集装置 |
H2O2溶液、MnO2 | ||
KMnO4 |
(2)实验室用高锰酸钾制取氧气的文字表达式是 .
(3)如果用F装置收集氧气,导管口开始有气泡放出时,不宜立即收集的原因是 , 当气泡地放出时,再收集,验满的方法是 .
(4)实验室用过氧化氢制取氧气的文字表达式是 ,
(5)使用装置B的优点是(答一点).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】KNO3与NaCl的溶解度曲线如图所示.下列说法正确的是( ) 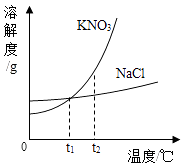
A.KNO3的溶解度大于NaCl的溶解度
B.加水能使NaCl的饱和溶液变为不饱和溶液
C.t1℃时,KNO3溶液与NaCl溶液溶质的质量分数相等
D.用冷却热饱和溶液的方法,能使KNO3从溶液中结晶析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜在纺织、印刷等行业有广泛用途.
(1)工业上可用铜屑、空气与稀硫酸在80℃条件下制备硫酸铜. 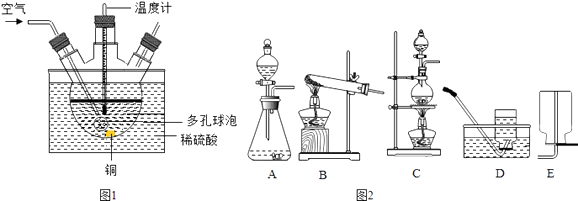
①如图1是实验室模拟工业制备硫酸铜的装置.反应的化学方程式为 , 采用水浴加热的优点是 , 多孔球泡的作用为 .
②工业生产时可用纯氧代替空气.这一措施能加快反应速率外,还具有的优点是③实验室用H2O2溶液和MnO2制备O2 , 反应的化学方程式为 , 在图2中,应选用的发生装置为(填序号,下同),收集装置为 .
(2)以CuSO4为原料制备碱式碳酸铜[Cu2(OH)2CO3]的过程如图3: 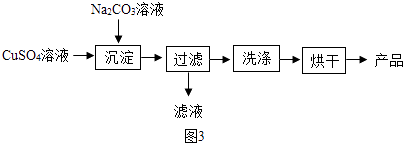
①“沉淀”时的反应为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2+CO2↑
②检验沉淀是否洗涤干净选用的试剂是(填化学式),烘干时产品中出现少量黑色物质,可能的原因为 .
③若所得产品的产率(产率= ![]() ×100%)偏高,其可能的原因为(填序号)
×100%)偏高,其可能的原因为(填序号)
a.反应物为完全沉淀 b.过滤时滤纸破损
c.Cu2(OH)2CO3未洗涤干净 d.Cu2(OH)2CO3为完全烘干
④“沉淀”时若有少量5Cu(OH)22CuCO3生成,则产品中铜元素的质量分数(填“偏大”“不变”或“偏小”)
(3)T℃时加热32.0g硫酸铜,一段时间后得到15.2gCuO和Cu2O的混合物,计算该混合物中CuO的质量(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青苹果汁遇到碘水时显蓝色。在加热条件下,熟苹果汁能与新配的氢氧化铜反应,产生红色的沉淀一下列结论正确的是 ( )
A. 青苹果中含有葡萄糖 B. 熟苹果中一定不含有淀粉
C. 苹果转熟时淀粉变成葡萄糖 D. 苹果转熟时葡萄糖转变成淀粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D四种物质之间的一步转化关系如图所示(部分反应物、生成物及反应条件围标出),它们均含有同种金属元素.A是大理石的主要成分,B是氧化物,C为碱、D由两种元素组成.下列判断错误的是( ) 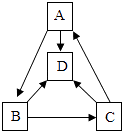
A.A的化学式为CaCO3
B.D物质不属于盐
C.表中未涉及的基本反应类型是置换反应
D.B→C的化学方程式为CaO+H2O═Ca(OH)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是今年无锡市实验操作考查“药品的取用和加热”中部分实验操作示意图.其中正确的是( )
A.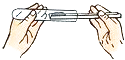 用纸槽将固体粉末送入试管
用纸槽将固体粉末送入试管
B. 倾倒液体
倾倒液体
C.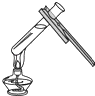 加热试管内液体
加热试管内液体
D. 熄灭酒精灯
熄灭酒精灯
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】莫凡同学完成镁与稀盐酸反应的实验室,观察到有灰白色沉淀生成的“异常”现象,引起了他的兴趣,并进行了以下探究.
(1)【初步探究】出现灰白色沉淀是否为偶然现象. 【实验Ⅰ】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
实验组别 | A | B | C | D |
镁带长度 | 1cm | 2cm | 3cm | 4cm |
沉淀量 | 无沉淀生成 | 少量沉淀 | 沉淀较多 | 沉淀很多 |
【实验结论】并非偶然,据表分析,是实验出现“异常”的主要因素.
【再次探究】该沉淀的成分
【猜想假设】猜想1:Mg;猜想2:MgCl2
【实验Ⅱ】
序号 | 实验操作 | 实验现象 | 实验结论 |
① | 取1g样品,加入足量 | 未见气泡 | 猜想1错误 |
② | 取1g样品,加入5mL蒸馏水,振荡 | 沉淀未溶解 | 猜想2错误 |
③ | 取1g MgCl2固体,加5mL蒸馏水,振荡 | 固体全部溶解 |
(2)【交流讨论】 ①莫凡同学做出猜想Ⅰ的依据是他认为反应物Mg过量,作出猜想2的依据是他认为生成物MgCl2 .
②从实验设计的角度讲,实验③的作用是 .
(3)【深入探究】该沉淀的物质组成 【查阅资料】
灰白色沉淀的成分为碱式氯化镁,它存在多种组成,化学式可表示为Mgx(OH)yClznH2O[即每份Mgx(OH)yClz结合了n份H2O],它受热分解可产生氧化镁、氯化氢和水.
【实验Ⅲ】
洗去沉淀表面杂质并室温晾干,取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验,待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g.
【问题讨论】
①反应停止后,应继续通入N2一段时间,目的是 .
②该沉淀中,镁、氯的离子个数比n(Mg2+):n(Cl﹣)= .
③若沉淀Mgx(OH)yClznH2O中,n=5,则X、Y、Z的数值依次为 . 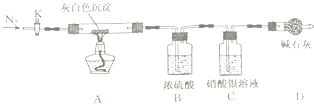
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com