
【题目】(1)早在西汉时期的《淮南万毕术》中就记载“曾青(硫酸铜溶液)得铁则化为铜”,成为现代湿法冶金的先驱,请写出该反应的化学方程式____________;
(2)“千锤百炼出深山”出自明朝于谦的《石灰吟》,诗句表达了石灰石高温分解的过程,请你写出该反应的化学方程式________。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】小明同学在实验结束进行废液处理,将氢氧化钠、石灰水和稀盐酸倒入同一洁净的烧杯中,当他用手接触烧杯外壁时,感觉到“发热”,这一现象引起了他的注意,于是他进行了如下探究。
[提出问题]这三种物质混合后,溶液中溶质的组成有几种可能?这三种物质间发生反应的一个化学方程式为_____。你认为发热的原因是______。
[提出假设]小明对反应后溶液中溶质的组成作出了两种合理的假设。
假设①:溶质为NaCl、CaCl2
假设②:溶质为NaCl、CaCl2、 NaOH、 Ca(OH)2
假设③:溶质为NaCl、CaCl2、NaOH
请你再补充一种合理的假设
假设④:溶质为________。
[实验验证]如果假设④成立,请你设计一个实验方案进行验证。
实验步骤及操作方法 | 实验现象 | 实验结论 |
____ | ____ | 假设④成立 |
[实验反思] (1)比较几种假设,能说明作出假设④的理由是__。
(2)在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
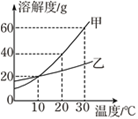
A. 依据溶解度曲线可判断,甲的溶解度比乙大
B. 10℃时,甲、乙饱和溶液溶质的质量相同
C. 20℃时,把30g甲放入50g水中形成的溶液中溶质质量分数为37.5%
D. 将20℃时的甲、乙饱和溶液升温至30℃,甲、乙溶液中溶质的质量分数均不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):
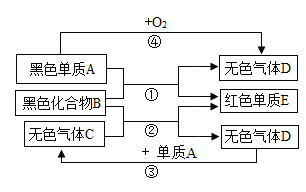
(1)在①②③④中,属于置换反应的是____________(填序号)。
(2)反应③的化学方程式是____________。
(3)在实验室里,反应①选择下图中的___________ (选填甲、乙、丙)。
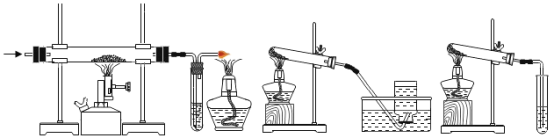
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示:
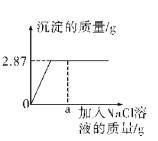
(1)恰好完全反应时生成沉淀质量为 g.
(2)当加入NaCl溶液的质量为ag时,滤液中所含的微粒有 。
(3)计算AgNO3溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国著名化学家侯德榜先生发明的侯氏制碱法,因原料利用率高,并能进行连续生产,从而享誉中外。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下图所示一套实验装置。
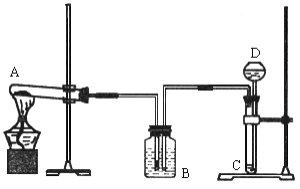
实验室可供选用的药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化
铵、氯化钠。
(1)A、D 中最合适的试剂为:A_______,D_______(填名称)。
(2)本实验在具体操作过程中,应先通______气体,再通______气体,原因是_______。
(3)小红同学认为实验装置中存在某些不足,请指出其中的一处错误_________。
(4)在改进装置后,小丽同学进行了实验,实验所用的饱和氯化钠溶液中含溶质 58.5g,实验最后得到无水碳酸钠 26.0g,针对实验结果,该同学认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜渣中约含![]() 7%、
7%、![]() 31%、
31%、![]() 50%、
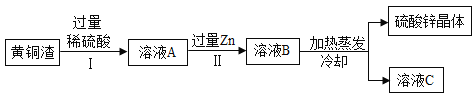
50%、![]() 5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如图所示(杂质不溶于水、不参与反应)。
5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如图所示(杂质不溶于水、不参与反应)。
已知:![]() ;
;![]()
①Ⅱ中反应的化学方程式为________。
②下列说法正确的是________。
a Ⅰ、Ⅱ中的操作均包含过滤 b 溶液A中![]() 的质量大于
的质量大于![]()
c 溶液A的质量小于溶液B d 溶液C中溶质的质量分数小于溶液B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.某化学兴趣小组的同学为了测定某黄铜的组成,取10g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 10 | m |
第2次 | 10 | 7.4 |
第3次 | 10 | 6.1 |
第4次 | 10 | 5.6 |
第5次 | 10 | 5.6 |
试回答下列问题:
(1)从以上数据可知,最后剩余的5.6g固体的成分是 ;表格中,m= .
(2)黄铜样品中锌的质量分数为 .
(3)计算所用稀硫酸中硫酸的质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com