
【题目】利用沉淀法可测定某粗盐样品的纯度(假定粗盐中的杂质全部是MgCl2)。每次取100 g样品配制成溶液,向其中加入质量分数为10%的氢氧化钠溶液,测得生成沉淀的质量与所加氢氧化钠溶液的质量关系如下表所示:
测定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
样品质量/g | 100 | 100 | 100 | 100 |
氢氧化钠溶液质量/g | 32 | 64 | 82 | 90 |
沉淀质量/g | 2.32 | 4.64 | 5.8 | 5.8 |
(1)求粗盐的纯度________。
(2)当样品与所加氢氧化钠溶液恰好完全反应时,求溶液中氯化钠的质量________。(写出解题过程)
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下图表示的实验方案设计,不能达到实验目的的是( )
A.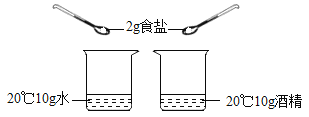 探究溶剂种类对物质溶解性的影响
探究溶剂种类对物质溶解性的影响
B. 探究温度对物质溶解性的影响
探究温度对物质溶解性的影响
C.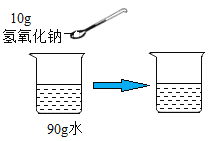 配制10%的氢氧化钙溶液
配制10%的氢氧化钙溶液
D. 区别氯化钠和氢氧化钠固体
区别氯化钠和氢氧化钠固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
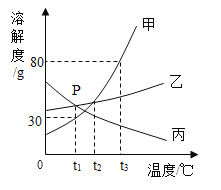
(1)P 点表示的含义是______________。
(2)当甲中含有少量乙时,提纯甲的方法是___________________。
(3)要使接近饱和的丙溶液变为饱和溶液,可采取的措施有(任写一种)_______________。
(4)t1℃时,将 30g 甲物质投入到 50g 水中充分溶解后,所得溶液的质量为_________g;若将温度升至 t3 ℃,使所得溶液的溶质质量分数变为 20%,应该再加水___________g。
(5)t3 ℃时,取等质量的甲、乙、丙三种物质分别配制成饱和溶液,需要水的质量最小的是_________。
(6)t3 ℃时,将等质量的三种物质的饱和溶液降温到 t2℃,对所得溶液的叙述正确的是_______________(填字母)。
A 溶液的质量关系是丙>乙>甲
B 丙溶液的溶质质量分数不变
C 溶剂的质量关系是甲=乙>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与人类生活息息相关。请回答下列问题:
(1)端午节吃粽子是咸宁的传统民俗,制作原料主要有糯米、瘦肉、食盐等,其中富含蛋白质的是 ___________。
(2)医用口罩原料主要是聚丙烯,N95口罩实际上就是用聚丙烯无纺布 SMMMS制作成的能过滤 95%微细颗粒的 5层口罩,聚丙烯属于__________(填“复合材料”、“合成材料”或“无机非金属材料”)。
(3)喝了汽水以后,常常会打嗝,这是因为_____________。
(4)人体每日必须摄入足量的钙,幼儿及青少年缺钙会患_____________和发育不良。
(5)用新制取的蒸馏水配制 50g 溶质质量分数为 5%的氯化钠溶液,配制溶液的正确操作顺序是__________(填序号)。
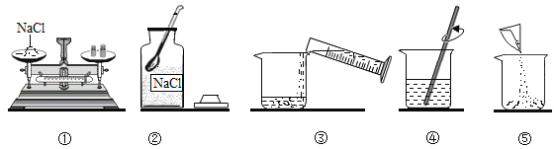
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过下列图示实验得出的结论中正确的是
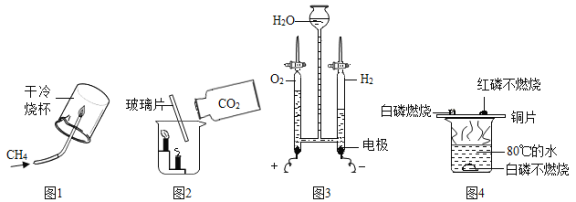
A.图1所示实验既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
B.图2所示实验既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧
C.图3所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的
D.图4所示实验既可探究可燃物的燃烧条件,又说明红磷不是可燃物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源是人类生存和发展的基础,能源及其应用成为日益关注的问题。
(1)煤是北方冬季取暖的主要原料,在氧气充足时燃烧生成CO2,氧气不足时生成_____(填化学式)等物质。为了使煤充分燃烧,有效利用能源,减少污染物的排放,把煤粉制成蜂窝煤以增大_____。
(2)在汽油中加入适量的乙醇可以减少汽车尾气的污染,乙醇燃烧反应的化学方程式为_____。
(3)高效催化剂能把汽车尾气中的有害的CO、NO转化为CO2和一种单质,该单质的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如下:
反应前物质的质量/g | 充分反应后物质的质量/g | |
过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
34.0 | 0.1 | 33.3 |
试计算:
(1)反应后将混合物过滤,所得固体的质量为_____;
(2)该同学所用过氧化氢溶液的溶质质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高氯酸钠晶体(NaClO4· H2O)可用于制备高氯酸。粗盐除去泥沙等不溶性杂质后得到“精盐”(只含 MgCl2、CaCl2 两种杂质)。以“精盐”为原料制备高氯酸钠晶体的流程如下:
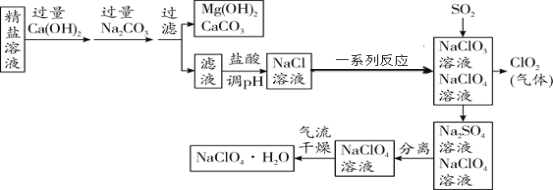
(资料)高氯酸钠在较高温度下易分解。请回答下列问题:
(1)流程中加入过量 Ca(OH)2 和过量 Na2CO3 的顺序能否对调(填能或不能)_______,为什么_______?
(2)写出加入盐酸调 pH 的化学方程式_______(写一个)。
(3)ClO2 的化学名称为______。通入 SO2 是为了除去NaClO4 溶液中少量的 NaClO3,该反应生成两种物质,请写出化学方程式_________。
(4)“气流干燥”时,温度应控制在 75℃~95℃,其原因是______。
(5)NaClO4 溶液中的阴离子是_________(写化学符号),如何检验 NaClO4 溶液中是否还存在Na2SO4_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源、万物之基,是人类宝贵的自然资源。
(1)水的净化河水净化的主要步骤如图所示。有关说法错误的是________
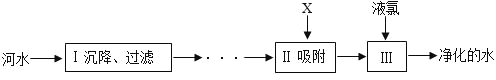
A 步骤Ⅰ可除去难溶性杂质
B X 试剂可以是活性炭
C 步骤Ⅲ可杀菌消毒
D 净化后的水是纯净物
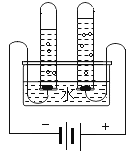
(2)水的组成如图是电解水的实验图,通过电解水的实验得出了水的组成。请写出电解水的化学方程式为________,电解时收集到正极、负极气体的质量比为________。
(3)水的用途(如图)
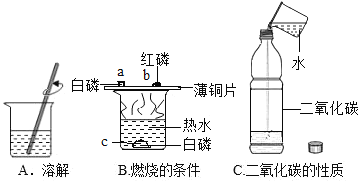
①实验 A 中水作 ____________(填“溶剂”或“溶质”)。
②实验 B 中水的作用是提供热量和 ________。
③实验 C 中的水作反应物,与二氧化碳反应生成________(写名称)。
(4)水的溶液水可以作为溶剂溶解多种物质,如图是甲、乙、丙 三种物质的溶解度曲线。

①图中甲和丙的交点的意义是________________。
②t1℃时,等质量的甲、乙饱和溶液,其中所含溶质的质量:甲________ 乙(填“大于”、“等于”、“小于”)。
③t2℃时,将 20g 丙溶解于 50g 水中,形成________g 溶液,溶液的溶质质量分数为 ____________(保留到 0.1%)。
④分别将 t2℃时甲、乙、丙三种物质的饱和溶液升温至 t3℃,所得 溶液溶质质量分数的大小关系为:____________(从大到小排列)。
⑤M 点代表 t3℃时甲的 ____________溶液(填“饱和”或“不饱和”),若要将组成在 M 点的甲溶液转变为N 点的甲溶液,可采取____________方法。若将甲溶液从状态 A 改变为 N 有多种途径, 试设计并简述一操作最简单、结果最准确的实验途径:先将 A 点的甲的饱和溶液降温到 t2℃,____,再将溶液升温至 t3℃。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com