
【题目】“地沟油”是指将干水道中的油腻漂浮物或者将宾馆、酒楼的剩饭剩菜劣质猪肉猪内脏、猪皮等经过简单加工、提炼出的油,其中含严重超标的黄曲霉素。黄曲霉素是目前发现的化学致癌物中最强的物质之一。请计算黄曲霉素B1(化学式为C17H12O6):
(1)相对分子质量为_____________;
(2)C、H、O三种元素的质量比为_____________;
(3)156 g黄曲霉素B1与_____________g二氧化碳含有相同质量的碳元素。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】硫酸是重要的化工原料,可用于生产化肥农药火药等,硫酸生产厂产生的烟气中含有SO2气体,直接排放会形成酸雨,如图是某硫酸厂除去烟气中SO2的流程图,回答下列问题:
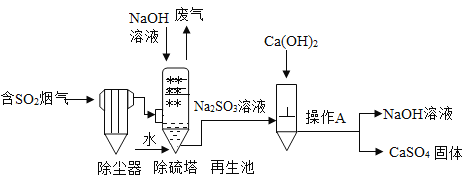
(1)除硫塔内,将NaOH溶液呈雾状向下喷洒,其目的是________;SO2发生反应的化学方程式是________(写一个)。
(2)再生池内加入的氢氧化钙也可用________代替。
(3)图中操作A指的是________,流程中可以循环利用的物质是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】武汉举行首届中国国际钢铁流通博览会,将商讨全球金属流通行业的战略性问题。则回答:
(1)金属材料的生产和使用是人类文明和社会进步的重要标志。常见三种金属铜、铁和铝被先后大规模的发现与使用,则其中的原因是(_____)
A 地壳中金属元素的含量 B 金属的导电性
C 金属的活动性顺序 D 金属的资源与价格
(2)大型钢铁企业常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,相关系列的化学反应过程如下:
![]()
请写出第①②步反应的化学方程式分别为_______________和__________。第③步反应的反应现象为______________________________。
(3)金属矿物的储量有限,而且不能再生。目前世界上已有50%以上的废钢铁得到回收利用,请说明其目的是________(填“合理开采矿物”、“节约金属资源”或“开发出金属的代用品”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌粉笔的成分为碳酸钙、硫酸钙,可能含有少量氧化钙。取37g干燥的粉笔研磨成粉末,加入足量稀盐酸,充分反应后得到8.8g气体。将反应后的固液混合物蒸干,测得其中钙元素质量为13.5g。(说明:硫酸钙与稀盐酸不反应)
(1)根据化学方程式计算37g粉笔中碳酸钙的质量。
(2)推断该粉笔中是否含有氧化钙。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】几位同学在实验室用下列装置制取几种气体。
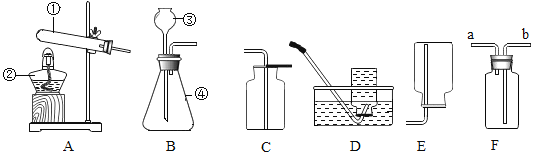
(1)写出图中标号仪器名称:①______;②______;③______;④______。
(2)甲同学欲制取并收集较纯净的氧气,他选择上述装置中的A和______(填装置序号)进行组装。写出该反应的化学方程式:______,试管口略向下倾斜是因为______。
(3)乙同学用过氧化氢和二氧化锰混合制取氧气,他应选的装置组合是______(填装置序号),其中二氧化锰作用是______,写出该反应的化学方程式:______。若用F收集氧气,则气体应从______进。
(4)乙炔又称电石气,是一种无色无味、密度比空气略小、不易溶于水的气体,工业上常用它燃烧产生的高温来切割和焊接金属。实验室用电石(固体)与水反应制取乙炔,你认为应选择的发生装置是______(填字母),为了收集到纯度较高的乙炔,应选择的收集装置是______(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。
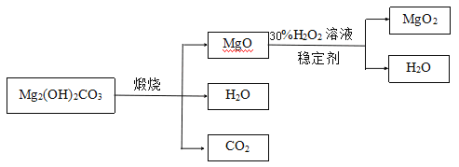
(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
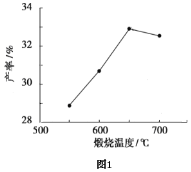
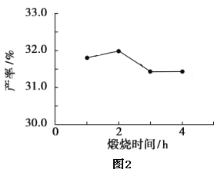
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种固体物质(不含结晶水)在水中的溶解度曲线,请回答下列问题。
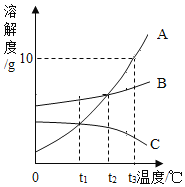
(1)气体的溶解度随温度的变化情况与___________相似(选填 “A”、“B”或“C”)。
(2) t2C时,在25g水中最多溶解1.6gA物质,则A物质在t2°C时的溶解度为_____________。
(3) t3C时,将l0gA物质加入到50g水中,充分溶解后,所得溶液中溶质和溶液的质量比为_____________。
(4)将t3C时的A、B、C三种物质的饱和溶液降温至t2C,析出晶体最多的是_________(选填“A”、“B”、“C”或“不能确定”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“碳足迹”(见图)标示着一个人或者团体的碳耗用量,一般悄况下,人们消耗的能源越多,排放的二氧化碳越多,碳足迹就越大。碳足迹的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗品。下列做法不能有效减小“碳足迹”的是( )

A.减少一次性产品的使用
B.绿色出行,多采用自行车和步行方式
C.大量使用煤、石油等化石燃料
D.将生活垃圾进行分类回收处理
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室提供以下所示的常见仪器,供完成下列气体制取实验时选用。
(1)(4分)写出下列仪器的名称:
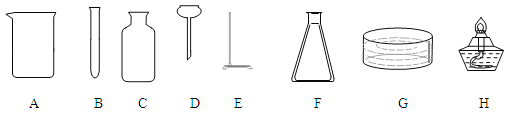
(2)(4分)实验室采用加热高锰酸钾制取O2并用排水法收集O2时,必须选用上述仪器中的 (填序号),反应化学方程式为为 。
(3)(4分)过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体,它在二氧化锰的催化作用下能迅速分解,生成水和氧气。写出该反应的化学方程式 。若实验室采用该反应来制取O2,并且在实验过程中可以随时添加双氧水,则气体发生装置必须选用上述仪器中的 (填序号)。
(4)(4分)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室常用固体NH4Cl和固体Ca(OH)2加热制得NH3,同时得到氯化钙和水,该反应的化学方程式为 ,实验制取和收集NH3必须选用上述仪器中的 (填序号)。
(5)(2分)若直接使用下图所示装置收集O2,
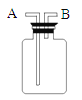
O2由 进入;若在装置中充满水,则O2应由 口进入(填编号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com