

分析 (1)根据盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,第二次加盐酸,滤渣继续减少,说明第一次中盐酸完全反应且碳酸钙有剩余,可知50g盐酸完全消耗5g碳酸钙,而第二次减少的质量为2.9g,说明碳酸钙完全反应,剩余滤渣的质量就是石灰石样品中杂质的质量进行解答;
(2)根据碱石灰能吸收水蒸气和氯化氢气体,B中吸收二氧化碳中带出的水蒸气和氯化氢气体进行解答;
(3)根据二氧化碳体积和密度求出二氧化碳的质量,利用二氧化碳的质量求出碳酸钙的质量,进而求出该石灰石样品中CaCO3的质量分数即可.
(4)根据碳酸钙与盐酸反应的方程式,由5g碳酸钙的质量求出50g盐酸中溶质的质量,再求出稀盐酸溶质质量分数.
解答 解:(1)盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,第二次加盐酸,滤渣继续减少,说明第一次中盐酸完全反应且碳酸钙有剩余,可知50g盐酸完全消耗5g碳酸钙,而第二次减少的质量为2.9g,说明碳酸钙完全反应,剩余滤渣的质量就是石灰石样品中杂质的质量.
的碳酸钙的质量分数=$\frac{10g-2.1g}{10g}$×100%=79%;
(2)碱石灰能吸收水蒸气和氯化氢气体,B中吸收二氧化碳中带出的水蒸气和氯化氢气体,所以算得碳酸钙的质量分数,发现与事实严重不符;
(3)二氧化碳的质量:1.8g/L×0.244L≈0.44g,
设碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 0.44g
$\frac{100}{x}=\frac{44}{0.44g}$
解得:x=1g
该石灰石样品中CaCO3的质量分数=$\frac{1g}{1.25g}$×100%=80%
(4)设50g的盐酸中溶质的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
5g y
$\frac{100}{5g}=\frac{73}{y}$
解得:y=3.65g
所用的稀盐酸溶质质量分数是:$\frac{3.65g}{50g}$×100%=7.3%
故答为:(1)79%;
(2)B中吸收了二氧化碳中带出的水蒸气和氯化氢气体;
(3)该石灰石样品中CaCO3的质量分数为80%;
(4)所用的稀盐酸溶质质量分数是7.3%.
点评 本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源: 题型:选择题
| A. | 提倡使用乙醇汽油 | |
| B. | 改进发动机的燃烧方式,使汽油充分燃烧 | |
| C. | 从植物中提炼燃油 | |
| D. | 寻找新的催化剂使水变汽油 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
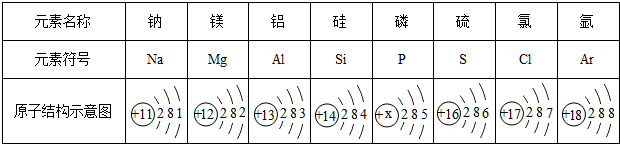
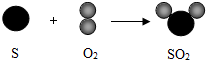
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | ①③ | B. | ②③ | C. | ④⑤ | D. | ②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
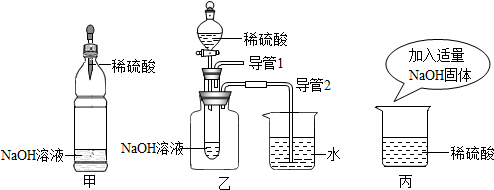
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
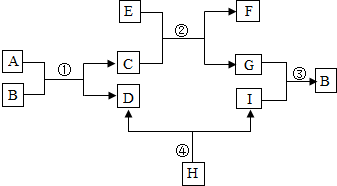
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | 晶体中结晶水质量分数 |
| 12.0g | 22.0g | 18.2g | 38% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com