
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | 晶体中结晶水质量分数 |
| 12.0g | 22.0g | 18.2g | 38% |
分析 研磨硫酸铜晶体应该在研钵中进行;
当两次称量误差小于0.1g时,说明结晶水已经完全失去;
根据提供的数据可以计算硫酸铜晶体中结晶水的质量分数.
解答 解:(1)实验中,需用到的实验仪器有:托盘天平、瓷坩埚、坩埚钳、铁三脚、石棉网、玻璃棒、干燥器、酒精灯、研钵和药匙.
故填:研钵、药匙.
(2)本实验过程中,最少应进行4次称量操作.
故填;4.
(3)判断硫酸铜晶体是否完全失水方法是:最后一次加热前后两次质量数据差不超过0.1g.
故填:最后一次加热前后两次质量数据差不超过0.1g.
(4)晶体中结晶水质量分数为:$\frac{22.0g-18.2g}{22.0g-12.0g}$×100%=38%,
故填:38%.
(5)A.硫酸铜晶体中含有不挥发性杂质时,会导致计算的结晶水质量分数偏小;
B.实验前晶体表面有湿存水时,会导致计算的结晶水质量分数偏高;
C.加热时有晶体飞溅出去时,会导致计算的结晶水质量分数偏高;
D.加热失水后露置在空气中冷却时,会导致计算的结晶水质量分数偏小.
故填:B、C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图,一辆载满电石的货车在雨中行驶时突然燃起大火,并伴有大量黑烟.某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动.
如图,一辆载满电石的货车在雨中行驶时突然燃起大火,并伴有大量黑烟.某化学小组对电石中碳化钙(CaC2)的性质产生了兴趣,进行了下列探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
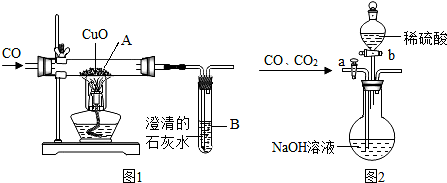
| 实验步骤 | 取少量该红色固体放入盛有稀硫酸的试管中,振荡 |
| 实验现象及结论 | 若溶液变蓝,则含有氧化亚铜,若溶液颜色不变,则不含有氧化亚铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
 表示氮原子
表示氮原子 表示氢原子.下列叙述正确的是( )
表示氢原子.下列叙述正确的是( )
| A. | 此反应有化合物参加 | |
| B. | 分子在化学变化中是可分的 | |
| C. | 符合上述反应过程的顺序是①③② | |
| D. | 对应化学反应方程式为N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
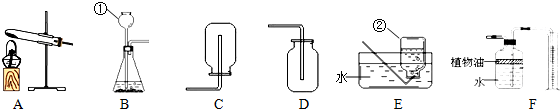
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com