
【题目】A~H都是初中化学常见的物质,它们之间的转化关系如图所示。已知A、B均为黑色粉末;D、F均为红色固体,且D为单质;C能使澄清石灰水变浑浊。请回答:
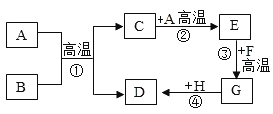
(1)A的化学式为:_____;E的名称为_____:C的固体俗称为_____。
(2)反应①的化学方程式为_____,该反应的现象为_____。
(3)反应②是_____反应(填“放热”或“吸热”),在③中E表现出_____性。
(4)请写出一个能实现反应④的化学方程式:_____。
【答案】C 一氧化碳 干冰 C+2CuO 2Cu+CO2↑ 黑色粉末逐渐变成亮红色 吸热 还原 Fe+CuSO4=FeSO4+Cu
2Cu+CO2↑ 黑色粉末逐渐变成亮红色 吸热 还原 Fe+CuSO4=FeSO4+Cu
【解析】
A﹣H都是初中化学常见的物质,C能使澄清石灰水变浑浊,所以C是二氧化碳,A、B均为黑色粉末,D、F均为红色固体,且D为单质,A、B高温会生成二氧化碳和D,所以D是铜,二氧化碳和A会生成E,所以A是碳,B是氧化铜,E是一氧化碳,一氧化碳和红色固体F反应会生成G,所以F是氧化铁,G是铁,铁和硫酸铜会生成硫酸亚铁和铜,经过验证,推导正确。
(1)A是碳,化学式为是C;E的名称为一氧化碳;C是二氧化碳,俗称为干冰;
(2)反应①是碳和氧化铜在高温的条件下生成铜和二氧化碳,化学方程式为:C+2CuO 2Cu+CO2↑,该反应的现象为:黑色粉末逐渐变成亮红色;
2Cu+CO2↑,该反应的现象为:黑色粉末逐渐变成亮红色;
(3)反应②是和碳在高温的条件下生成一氧化碳,属于吸热反应,在③中是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,E表现出还原性;
(4)反应④可以是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu。
故答案为:(1)C;一氧化碳;干冰;(2)C+2CuO 2Cu+CO2↑;黑色粉末逐渐变成亮红色;(3)吸热;还原;(4)Fe+CuSO4=FeSO4+Cu。
2Cu+CO2↑;黑色粉末逐渐变成亮红色;(3)吸热;还原;(4)Fe+CuSO4=FeSO4+Cu。


科目:初中化学 来源: 题型:
【题目】大自然向人类提供了丰富的金属资源。
(1)探究铁钉锈蚀条件的实验如图所示。
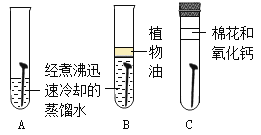
①蒸馏水经过了煮沸,目的是_________________;氯化钙的作用是_________________。
②对比试管_____(填字母,下同)和试管_____,可知铁钉锈蚀需要与水直接接触。
(2)钛铁矿(主要成分为FeTiO3)可用来提取钛,工业流程如下图所示。
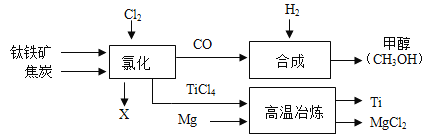
①氯化过程发生反应的化学方程式为2FeTiO3+6C+7Cl2 2TiCl4+2X+6CO,X的化学式为_________。
2TiCl4+2X+6CO,X的化学式为_________。
②高温冶炼过程发生的反应属于基本反应类型中的_________。
③合成过程得到的产物甲醇(CH3OH)是一种重要的燃料,甲醇充分燃烧的化学方程式为_________________________________________。
(3)下列途径能有效保护金属资源的是_________(填字母)。
A 防止金属腐蚀 B 回收利用废旧金属
C 合理有效地开采矿物 D 寻找金属的代用品
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t1℃时,取a、b两种固体物质各25g于两只烧杯中,分别加入100g水,充分溶解后,两种固体均有剩余。升温到t2℃时,a完全溶解,b固体增多。a、b两种物质的溶解度曲线如图所示。以下判断正确的是( )
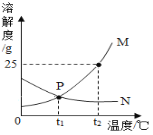
A. 图中曲线M表示b物质的溶解度曲线
B. t1℃时,两只烧杯中剩余物质的质量不相等
C. t2℃时,两只烧杯中的溶液都是饱和溶液
D. t2℃时,两只烧杯中溶液的溶质质量分数相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程如图所示。
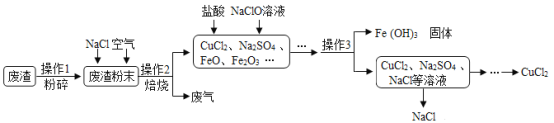
(1)NaClO中氯元素的化合价是____________________。
(2)操作1:粉碎。粉碎的目的是____________________。
(3)操作2:焙烧。高温条件下,通入空气,CuS和NaCl反应生成了CuCl2和Na2SO4,化学方程式为:__________________。
(4)操作3:__________(填操作名称),进行该操作时玻璃棒的作用是_______________。
(5)流程图中能循环利用的物质是______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应变化关系的是
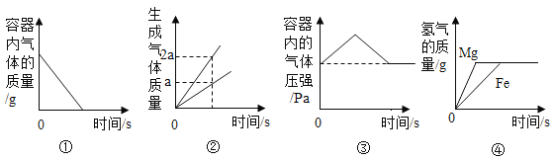
A.图①:足量的碳在盛有氧气的密闭容器内充分燃烧
B.图②:在电解器玻璃管里加满水,用惰性电极进行电解
C.图③:红磷在盛有一定量空气的密闭容器中燃烧至熄灭
D.图④:将稀盐酸分成两等份,分别加入足量的Mg粉、Fe粉
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝元素的相关信息如图所示,下列叙述正确的是( )
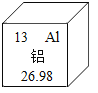
A.铝原子的最外层电子数为 3B.铝原子的核内中子数为 13
C.铝是地壳中含量最高的元素D.自然界中铝主要以单质形式存在
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明利用图 1 装置探究物质在空气中燃烧后氧气浓度变化(已知:白磷的着火点是40℃,红磷的着火点是240℃)。图 2 是用传感器测量整个实验过程中烧瓶内氧气浓度变化情况的曲线。
步骤 1:用激光笔照射燃烧匙中足量的红磷,红磷燃烧,一段时间后熄灭;白磷始终不燃烧。
步骤 2:冷却至室温,将装有白磷的燃烧匙提岀水面,用激光笔照射,白磷燃烧。
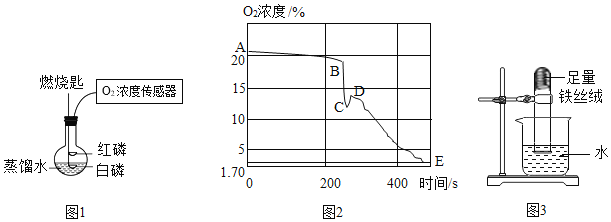
(1)在步骤 1 开始前应进行的操作是__________________;步骤 1 中激光笔的作用是________________;
(2)在步骤 1 中反应的化学方程式为___________________;图 2 表示红磷燃烧的曲线是_____________;该曲线对应装置内压强变化情况是______________;
(3)你认为“测定空气中氧气的含量”,选择______________(填“红磷”或“白磷”)效果会更好;
(4)通过本实验你对物质的燃烧有什么新的认识?________________;
(5)图 2 中 CD 段氧气浓度变化的主要原因是:________________;DE 段氧气浓度变化的主要原因是:____________________;
(6)查阅资料可知,测定空气中氧气含量较好的药品是铁丝绒,利用的原理是铁与氧气、水发生缓慢氧化而生锈,用图 3 所示装置完成实验,最终观察到的现象是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图“黑面包”实验中,蔗糖(C12H22O11)变黑,体积膨胀,变成疏松的炭,放出有刺激性气味的气体。
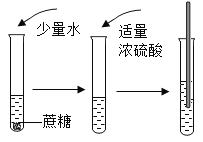
(提出问题)改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?
(进行实验)分别取5g糖粉进行实验,根据前2 min的现象对实验效果进行评分,记录如下:
表1 实验记录
实验 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | 效果得分 |
1 | 蔗糖 | 4 | 5 | 22 | 65 |
2 | 蔗糖 | 5 | 10 | 30 | 81 |
3 | 蔗糖 | 6 | 15 | 50 | 93 |
4 | 冰糖 | 4 | 10 | 50 | 91 |
5 | 冰糖 | 5 | 15 | 22 | 88 |
6 | 冰糖 | a | 5 | 30 | 75 |
7 | 葡萄糖 | 4 | 15 | 30 | 0 |
8 | 葡萄糖 | 5 | 5 | 50 | 0 |
9 | 葡萄糖 | 6 | 10 | 22 | 0 |
(处理数据)分析表1,计算效果得分均值,结果如下:
表2 效果得分均值
因素 | 糖 | 浓硫酸体积/mL | 水的滴数 | 温度/℃ | ||||||||
蔗糖 | 冰糖 | 葡萄糖 | 4 | 5 | 6 | 5 | 10 | 15 | 22 | 30 | 50 | |
均值 | 79.7 | 84.7 | 0 | 52.0 | 56.3 | 56.0 | 46.7 | 57.3 | 60.3 | 51.0 | 52.0 | 61.3 |
依据均值推断最佳实验方案,均值越高,效果越好。
(解释与结论)
(1)推测放出的气体含SO2,从元素守恒角度说明理由_____;
(2)实验6中,a为_____mL;
(3)根据表2推断,“黑面包”实验最好选择5 g冰糖、5 mL浓硫酸、_____滴水和50 ℃;
(反思与评价)
(4)表2中,22 ℃对应的均值为51.0,计算该值所依据的3个数据分别是_____;
(5)综合分析,使实验3的效果得分高于实验4的因素有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是制取饮用水消毒剂二氧化氯的微观过程图。下列说法错误的是
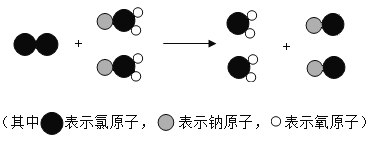
A.二氧化氯的化学式为ClO2
B.二氧化氯中氯元素的化合价为+4
C.反应物和生成物中共有两种氧化物
D.化学反应前后原子的种类不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com