
����Ŀ��ˮ������ɻ�ȱ��һ�����ʡ� ������ʶ��,�����ں����ؽ���ʹ�á�
(1)���ݺܶ�ط�������Ȫ��ȡij����Ȫˮ��,��ȴ�����º����̽���������Ȫˮ����pH=7.4.��֪����Ȫˮ����_______________�ԡ�
(2)��ͼ���ܷ�ӳˮ�ڿ����з���ʱ�����仯����ʾ��ͼ��_______________��(����ĸ���)(ͼ�С�![]() ����ʾ��ԭ��,��
����ʾ��ԭ��,��![]() ����ʾ��ԭ��)
����ʾ��ԭ��)
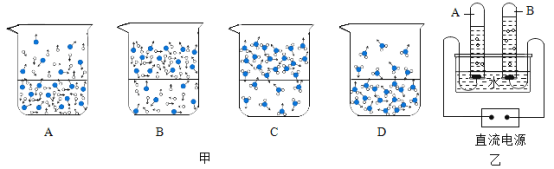
(3)��ͼ�ǵ��ˮ��װ�á�
���뻭ͼ��ʾ�ñ仯���۹���:_______________��
��ͨ����ʵ�飬�ɵó�����ˮ����ɵĽ���:_______________��
���𰸡��� D 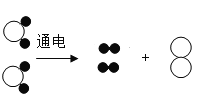 ˮ������Ԫ�غ���Ԫ����ɵ�
ˮ������Ԫ�غ���Ԫ����ɵ�
��������
(1)�����Ȫˮ����pH=7.4��pH����7����֪����Ȫˮ���ʼ��ԡ�
(2)ˮ�ڿ����з���ʱ��ˮ��������ˮ���������仯��ˮ����û�иı䣬�����Ӽ�ļ�����ͼA��B��ʾ���ӷ����ı䣬����ˮ���ӣ����������⣻ͼCˮ�����������С�����������⣻ͼD��ʾˮ��������ˮ���Ӽ����������⡣��ѡD��
(3)��ͼ�ǵ��ˮ��װ�á�
��ˮ��������ˮ���ӷ�Ϊ��ԭ�Ӻ���ԭ�ӣ�ÿ������ԭ�ӽ�ϳ�һ������ӣ�ÿ������ԭ�ӽ�ϳ�һ�������ӣ��ñ仯���۹�����ͼ ��
��
��ͨ����ʵ�飬�ɵó�ˮͨ����������������������������Ԫ����ɵģ�����������Ԫ����ɵģ��⡢��Ԫ�ض�������ˮ�����ˮ������Ԫ�غ���Ԫ����ɵġ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС���ijͭп�Ͻ���Ʒ����̽��ʵ�顣��ȡ��Ʒ10.0�ˣ�����100.0��ϡ������Һ��ε��룬ʵ�������ͼ��ʾ����
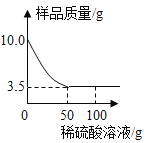
��1��ͭп�Ͻ���У�Zn������������ ��
��2������ϡ������Һ�����ʵ����������Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ��裨Tl������Ͻ�����뵼����ϡ�����5�ֺ���Ԫ�ص�����:Tl��Tl2O��Tl2O3��TlOH��Tl2SO4�������������裨Tl2SO4����ҺΪ��ɫ�����������裨TlOH����Һ�Ի�ɫ����ش��������⣺
��1��Tl2O3����_____��
��2���ڼ��������£��������裨Tl2O����������Ӧ�������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
��3��ȡ������ɫ����������Һ���Թ��У��ٵμ���������������Һ����������ã��۲쵽��ʵ��������______��
��4����֪Fe��Tl��Cu�Ľ��������ǿ������˳��Ϊ��Fe��Tl����H����Cu������˵����ȷ����____��
A ������Tl����ϡ�����У���������������ð��
B ��ͭ˿����Tl2SO4��Һ�У�ͭ˿���渽��һ�����
C ��п����TlCl��Һ�У��ɷ������·�Ӧ��Zn+2TlCl![]() 2Tl+ ZnCl2
2Tl+ ZnCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ÿʱÿ�̶��벻����������ش��������⣺
��1�������ɷ����������ռ78%��������________����������ЧӦ����Ҫ������_______��
��2�������ڿ����еij���ʯ��ˮ��������һ���Ĥ������Ĥ��_____��
��3��С���������ڳ����ڷ��������ù�����������һЩ���⣬��ͨ���������ϵ�֪���������Ҫԭ������������е�________ͬʱ�Ӵ���
��4����ͼΪ�ⶨ�����������ĺ���װ��ͼ��ʵ��ʱ����ˮ�������������ƿ��ԭ���������1/5��ԭ�������_______��
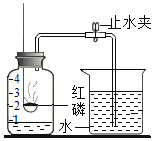
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�����ֹ�������(�������ᾧˮ)���ܽ��������ͼ��ʾ������˵����ȷ����
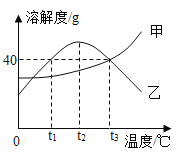
A.�ҵ��ܽ�ȴ��ڼ��ܽ��
B.t2��ʱ���ҵı�����Һ���»��¾�����������
C.����Һ��t3�潵�µ�t1�棬����Һ�е����������������С
D.t3��ʱ,50gˮ�м���40g�ļ����ʳ���ܽ�ɵõ�90g�ı�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ò��͵�������װ�������ʹβ���ŷŴ���ġ������乤��ԭ���ǣ�
(1)��������Һ���������ȵ�β���У����ͷų��������䷴Ӧ����ʽΪ��
CO(NH2)2+X=CO2+2NH3��X�Ļ�ѧʽΪ ��
(2)�ڴ����������£�������NH3��ʹ����β���еĵ����������ת�������ĵ�����ˮ������ˮ����������β���е��̳�������PM2.5�ŷš���д��������N20��Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾʵ����� �в���ȷ����
A. 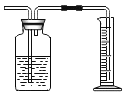 ��ˮ�������������� B.
��ˮ�������������� B. 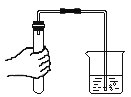 ����װ��������
����װ��������
C. 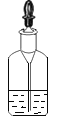 �ι����꼴��� D.
�ι����꼴��� D. 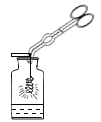 ��˿��������ȼ��
��˿��������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩˮ��ɢ������ζ������������������������������һ����״Һ�壬���ܸ���ˮ���ϡ�������Ҵ���Ũ���ᡢ���ȵ������·�����Ӧ����������������ˮ��ʵ�������ø÷�Ӧ�Ʊ���������������������Ϣ������˵������ȷ����( )
A.���������ӷ�
B.��������������ˮ�����ܶ�С��ˮ
C.Ũ����������Ʊ����������ķ�Ӧ�Ĵ���
D.�÷�Ӧ�����ֱ���ʽΪ������+�Ҵ�![]() ��������+ˮ
��������+ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڢ֣��û�ѧ��������ȡ���������ʣ���ѧ��ȤС��Ӧ���кͷ�Ӧԭ����ȡ�Ȼ��ƹ��塣
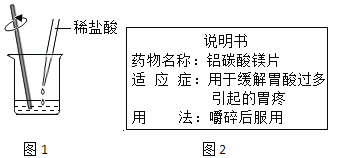
��1����װ������������Һ���ձ��е�����ɫʯ����Һ����Һ��_____ɫ��
��2����ͼ1�������ձ��м�����εμ�ϡ��������Һǡ�ñ�Ϊ��ɫ��������Ӧ�����Һ�м������̿����ֻ�ϣ����˺�õ���ɫ��Һ��
�ټ������̿��Ŀ����_____��
���ڹ��˲����У���������������_____��
��3����pH��ֽ�⣨2������Һ�����ȣ������������ȡpH��ֽ�ڲ���Ƭ�ϣ�_____������ֽ��ʾ����ɫ�����ɫ���Ƚϣ�������Һ��pH��
��4���������ҺpHΪ8����������Һ�μ��Թ��������ᣬĿ����_____����������Һ�Գ�ȥ���������ᣬ�ò������õ������������_____������������Һ�õ�����Ĺ����У��ò��������Ͻ����Ŀ����_____��
�ڢ֣�θ���������ÿ���ҩ��������ᷴӦ������ͼ2Ϊ��̼��þ˵����IJ������ݡ���ȤС��Ը�ҩ�↑չ����̽����
��1����ҩ������õ�̽��
���ϱ�������̼��þ[����Ҫ�ɷֵĻ�ѧʽΪAlMg(OH)3CO3]�����ᷴӦ�Ļ�ѧ����ʽΪ��AlMg(OH)3CO3+5HCl=MgCl2+AlCl3+4H2O+CO2��
�ٽ���Ӧ����������ͨ�����ʯ��ˮ�����۲쵽��������_____���÷�Ӧ�Ļ�ѧ����ʽΪ_____��
�ڸ������к���Al3+��Mg2+��OH����![]() ����ϸ����������ᷴӦ�Ļ�ѧ����ʽ��������ҩ���������ã�����θҺ���ԣ�������_____��_____���������ţ���
����ϸ����������ᷴӦ�Ļ�ѧ����ʽ��������ҩ���������ã�����θҺ���ԣ�������_____��_____���������ţ���
��2�����÷�����̽��
�ÿ���ҩΪʲôҪ����������������С������������������ͬ������ҩƬ���������ã������ĸ����θ������С������Ϊ�������ҩ�ォ��θҺ�е����ᷴӦ������
����Ȼ��С������Ǵ���ġ�ԭ����_____��
��С�����������ʵ����֤���Լ��IJ��룺
��ʵ��1����һƬ������ҩƬ�����Թ��У������м���5mL5%��ϡ���
��ʵ��2����һƬ������ҩƬ���������Թ��У������м���5mL5%��ϡ���ᡣ
�Ա�ʵ��1��ʵ��2��С���۲쵽������Ϊ_____��֤�������IJ�����ȷ��
��3����Ҫ�ɷֺ�����̽������ȤС��ȡ6ƬҩƬ���������Թ��У��������������ϡ���ᣬ��ַ�Ӧ��ų�����0.88g����ͨ�����㣬ÿƬҩ���к���AlMg(OH)3CO3�������Ƕ��٣�____�����������0.1������֪��ҩ�����������ɷֲ���ϡ���ᷴӦ��AlMg(OH)3CO3����Է�������Ϊ162��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com