
 生活中处处有化学,请用所学的化学知识填空.
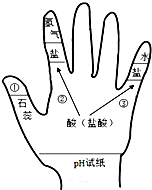
生活中处处有化学,请用所学的化学知识填空.分析 化学式书写的一般规律是:正前负后,然后利用十字交叉法书写;天然气的主要成分是CH4,能用来治疗胃酸过多的盐是NaHCO3,炉具清洁剂中的碱是NaOH,食醋中含有的酸CH3COOH;如图所示:图中①的现象是紫色变红色,若用湿润的PH试纸测定盐酸的PH,则结果会偏大;符合图中②的化学方程式:Mg+2HCl=MgCl2+H2↑;铁锈和适量盐酸反应后溶液呈黄色,因为铁离子是黄色的.
解答 解:(1)化学式书写的一般规律是:正前负后,然后利用十字交叉法书写;天然气的主要成分是CH4,能用来治疗胃酸过多的盐是NaHCO3,炉具清洁剂中的碱是NaOH,食醋中含有的酸CH3COOH;故答案为:①CH4;②NaHCO3;③NaOH;④CH3COOH;
(2)如图所示:图中①的现象是紫色变红色,若用湿润的PH试纸测定盐酸的PH,则结果会偏大;符合图中②的化学方程式:Mg+2HCl=MgCl2+H2↑;铁锈和适量盐酸反应后溶液呈黄色,因为铁离子是黄色的;故答案为:①紫色变红色;②偏大;③Mg+2HCl=MgCl2+H2↑(合理即可);④黄色
点评 本考点考查了化学式和化学方程式的书写、酸的性质等,元素符号、化学式、化学方程式等化学用语的书写是中考的重要考点之一,要加强练习,理解应用.本考点主要出现在选择题和填空题中.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 原溶液可能饱和也可能不饱和 | |
| B. | 析出晶体后的溶液可能是饱和溶液也可能是不饱和溶液 | |
| C. | 析出晶体后的溶液可能是浓溶液,也可能是稀溶液 | |
| D. | 再降温不一定会有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | CuO | Cu | 滴加足量盐酸,然后过滤 |
| B | NaOH溶液 | Na2CO3 | 加适量的稀盐酸 |
| C | Cu(NO3)2溶液 | AgNO3 | 加入足量铜粉,充分反应后过滤 |
| D | C02 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二硫基丙醇是氧化物 | |
| B. | 二硫基丙醇中氢元素的质量分数最大 | |
| C. | 二硫基丙醇中有3个碳原子 | |
| D. | 该物质中C、H、S、O原子的个数比为3:8:2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 “高钙片”是一种常见补钙剂,如图是“高钙片”说明书的一部分.
“高钙片”是一种常见补钙剂,如图是“高钙片”说明书的一部分.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | 氧化铜 | 如果氧化铜溶解,溶液变蓝说明盐酸已经过量 |
| C | 酚酞 | 如果溶液仍为无色,表明盐酸已经过量 |
| D | 碳酸钠粉末 | 如果有气泡产生,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有①CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量②气泡产生,得到浅绿色溶液. | 固体中一定含有③Fe, 一定不含Fe2O3 |

| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色溶液变为黄色、澄清的石灰水变浑浊 澄清的石灰水变浑浊 | 固体中一定含有 ③CaCO3和Fe2O3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验中用到的玻璃仪器只有烧杯和量筒 | |
| B. | 计算得氯化钠的质量为2.5g,水的体积为22.5ml | |
| C. | 量取水时,若俯视读数,会使配得的溶液浓度偏大 | |
| D. | 用天平称取该固体时将砝码和物品放反,会导致配得的溶液浓度偏小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡. | 有气泡冒出. | 氢氧化钠溶液一定变质了. |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀生成. | 说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有氢氧化钠. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com